





人教版 (2019)必修 第一册第一节 原子结构与元素周期表精品课件ppt
展开如上图是碱金属的单质存在形式或元素标识,他们之间有什么相似之处和递变性?完成下列问题你就会明白:
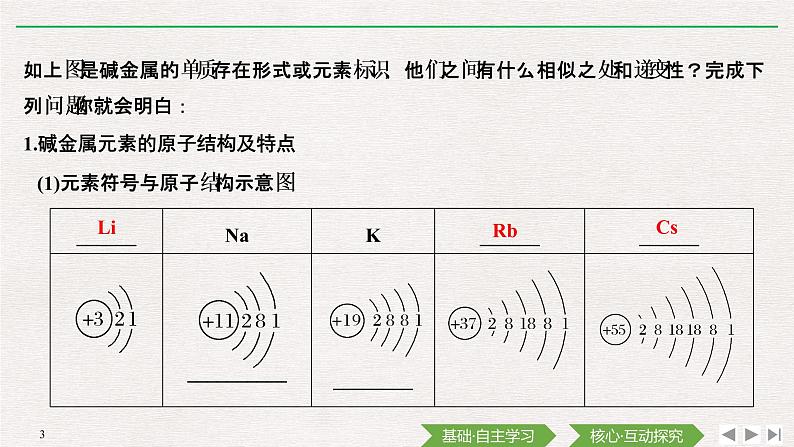
(1)元素符号与原子结构示意图
1.碱金属元素的原子结构及特点
(2)化学性质①与O2反应
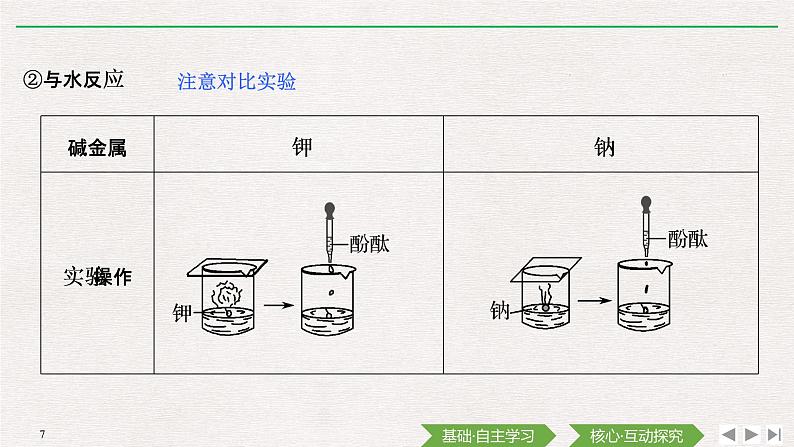
2K+2H2O===2KOH+H2↑
2Na+2H2O===2NaOH+H2↑
如图是卤素单质,他们的颜色越来越深,由气体逐渐变为固体,那么他们的性质有何相似性和递变性?请完成下列知识点:
(2)结构特点①相同点:最外层都有_____个电子。②递变性:从F→I,核电荷数逐渐_______,电子层数逐渐_______,原子半径逐渐_______。
2.卤族元素单质的性质
(2)化学性质①与H2反应
H2+F2===2HF
②卤素单质间的置换反应
2NaBr+Cl2===2NaCl+Br2
2KI+Br2===2KBr+I2
因为F2能与H2O发生反应(2F2+2H2O===4HF+O2),所以F2不能从其他卤化物的盐溶液中置换出卤素单质。
2KI+Cl2===2KCl+I2
知识点三 同主族元素的性质与原子结构的关系1.元素性质的影响因素
元素的性质主要与原子核外电子的排布,特别是与_________________有关。
微判断(1)碱金属元素原子的次外层电子数都是8个。( )(2)化合物中碱金属元素的化合价都为+1价。( )(3)碱金属元素的原子半径随核电荷数的增大而增大。( )(4)碱金属单质的化学性质活泼,易失电子发生还原反应。( )(5)Li在空气中加热生成LiO2。( )
(6)卤素单质与水反应均可用:X2+H2O===HXO+HX表示。( )(7)HX都极易溶于水,它们的热稳定性随核电荷数增加而增强。( )(8)卤素单质的颜色从F2―→I2按相对分子质量增大而加深。( )(9)将F2通入NaCl溶液中可置换出Cl2。( )答案 (1)× (2)√ (3)√ (4)× (5)× (6)× (7)× (8)√ (9)×
微训练1.下列对碱金属的叙述中不正确的是( )
A.碱金属中还原性最弱的是锂B.碱金属的原子半径和离子半径都随核电荷数的增大而增大C.碱金属都易失去1个电子D.从Li到Cs,碱金属的密度越来越大,熔、沸点越来越高解析 随原子序数的递增,碱金属原子半径和离子半径逐渐增大,单质的还原性逐渐增强,A、B正确;碱金属都易失去1个电子形成稳定的阳离子,C正确;从Li到Cs,密度呈增大趋势,但K的密度小于Na,熔、沸点越来越低,D错误。答案 D
2.下列关于卤素的叙述正确的是( )
A.卤素是典型的非金属元素,因此不能与其他非金属元素化合B.卤素单质越活泼,其熔、沸点就越高C.卤素各单质都能与水剧烈反应D.卤素的单质都能与氢气反应,且气态氢化物的稳定性随单质氧化性的增强而增强解析 卤素能与其他非金属元素化合,如H、C等;卤素单质越活泼,其相对分子质量越小,其熔、沸点越低;卤素单质中只有氟气能与水剧烈反应。答案 D
3.已知锂及其化合物的许多性质与碱金属差异较大,却与镁相似。下列有关锂及其化合物的叙述不正确的是( )
A.碳酸锂受强热很难分解B.碳酸锂的溶解度比碳酸氢锂的小C.锂在过量氧气中燃烧,主要产物是氧化锂而不是过氧化锂D.锂可以与氮气化合生成氮化锂(Li3N)解析 解题时充分利用题目信息,锂及其化合物的性质与镁的相似,MgCO3煅烧分解成MgO和CO2,由此可知,Li2CO3也易分解。答案 A
4.下列有关碱金属元素的性质判断正确的是( )
A.K与H2O反应最剧烈B.Rb比Na活泼,故Rb可以从NaCl溶液中置换出NaC.碱金属的阳离子没有还原性,所以有强氧化性D.从Li到Cs都易失去最外层1个电子,且失电子能力逐渐增强解析 A项,在碱金属元素中,K不是最活泼的元素;B项,Rb先与水反应,不会置换出Na;C项,碱金属的阳离子很稳定,不具有强氧化性。答案 D
5.关于卤素X(依次为Cl、Br、I)的下列叙述不正确的是( )
A.卤素单质与水反应均可用X2+H2O===HXO+HX表示B.HX都极易溶于水,它们的热稳定性随核电荷数增加而增强C.卤素单质的颜色随相对分子质量增大而加深D.相对分子质量小的卤素单质可将相对分子质量大的卤素从它的卤化物溶液里置换出来解析 HX的热稳定性随核电荷数的增加而减弱。答案 B
6.下列说法中,不符合ⅦA族元素性质特征的是( )
A.从上到下元素的非金属性增强B.原子易形成-1价阴离子C.从上到下最高价氧化物的水化物酸性减弱(F除外)D.从上到下氢化物的还原性依次增强解析 同主族元素,从上到下元素的非金属性减弱,选项A错误;第ⅦA族元素原子最外层7个电子,易得1个电子形成-1价阴离子,选项B正确;从上到下元素的非金属性逐渐减弱,所以最高价氧化物的水化物酸性逐渐减弱,选项C正确;同主族元素,从上到下元素的非金属性逐渐减弱,所以氢化物的还原性依次增强,选项D正确。答案 A
微思考1.同主族元素的原子结构及性质有何变化规律?
提示 同主族元素随核外电子层数的增加,它们的得电子能力逐渐减弱,非金属性逐渐减弱;失电子能力逐渐增强,金属性逐渐增强。
2.如何比较同主族元素的原子半径、阳离子半径、阴离子半径?
提示 (1)原子半径:同主族元素的原子最外层电子数相同,从上到下电子层数逐渐增多,所以半径逐渐增大。(2)阳离子半径:以碱金属为例,在形成离子时,均失去最外层电子,所以均少一个电子层,电子层数仍然是逐渐增多,所以半径逐渐增大。(3)阴离子半径:以卤族元素为例,在形成离子时,最外层均得到一个电子,所以最外层电子数仍然相同,电子层数仍然是逐渐增多,所以半径逐渐增大。
学习任务1 碱金属元素单质化学性质的相似性和递变性
如图是碱金属单质的存在形式,它们在生活中有不同的应用,结构相似为什么应用不同呢?带着这个问题完成下列讨论:
1.请结合碱金属元素的原子结构的递变性探究其单质化学性质的递变性。
提示 碱金属元素原子的最外层电子数都相等,但从Li到Cs,随着核电荷数的增加,碱金属元素原子的电子层数逐渐增多,原子核对核外电子的吸引能力逐渐减弱;失电子能力逐渐增强,金属性逐渐增强。
2.碱金属元素在性质上具有相似性,根据钠的性质,推断碱金属可能具有的化学性质有哪些?
提示 (1)与O2反应生成相应的氧化物,如Li2O、Na2O等。(2)与Cl2反应生成RCl,如NaCl、KCl等。(3)与H2O反应,能置换出H2O中的氢,反应通式为:2R+2H2O===2ROH+H2↑。(4)与非氧化性酸反应,生成H2,反应通式为:2R+2H+===2R++H2↑。(R表示碱金属元素)
3.根据碱金属元素性质的递变性,判断从Li→Cs,对应阳离子的氧化性强弱以及最高价氧化物对应水化物的碱性强弱的递变性。
提示 从Li到Cs,原子失电子能力逐渐增强,金属性逐渐增强,故对应阳离子的氧化性依次减弱,即Li+>Na+>K+>Rb+>Cs+。最高价氧化物对应水化物的碱性逐渐增强,CsOH的碱性最强。
1.碱金属的相似性(用R表示碱金属元素)
(1)与O2反应从Li→Cs,与O2反应越来越剧烈,产物越来越复杂,如Li与O2反应只能生成Li2O,Na与O2反应还可以生成Na2O2,而K与O2反应能够生成KO2等。(2)与H2O(或酸)的反应从Li→Cs,与H2O(或酸)反应越来越剧烈,如K与H2O反应可能会发生轻微爆炸,Rb和Cs遇水发生剧烈爆炸。(3)最高价氧化物对应水化物的碱性碱性:LiOH
A.锂与水反应不如钠与水反应剧烈B.Rb比Na活泼,故Rb可以从NaCl溶液中置换出NaC.熔、沸点:Li>Na>KD.碱性:LiOH
A.碱金属元素原子最外层都只有1个电子,在化学反应中容易失去B.碱金属单质都是强还原剂C.碱金属单质都能在氧气中燃烧生成过氧化物D.碱金属单质都能与水反应生成碱解析 同一主族元素最外层电子数相同,碱金属元素原子最外层电子数均为1,在化学反应中很容易失去最外层的1个电子,还原性很强,A、B对;Li与O2反应,只生成Li2O,Na在O2中点燃生成Na2O2,K在O2中可生成KO2,C错;碱金属元素的单质都能与水反应生成碱和氢气,D对。答案 C
学习任务2 卤族元素单质化学性质的相似性、递变性和特殊性
如图是卤素原子的核外电子排布和卤素单质的存在形式,请回答下列问题:
1.请结合卤族元素原子结构的相似性与递变性探讨其化学性质的相似性与递变性。
提示 (1)卤族元素原子最外层都有7个电子,都易得1个电子达到8电子稳定结构,所以在化学反应中都表现很强的氧化性。(2)随着原子序数的增加,电子层数依次增多,原子核对最外层电子的吸引能力逐渐减弱,得电子能力依次减弱,氧化性依次减弱。
2.根据卤族元素的性质分析,将F2通入NaCl溶液中得到什么气体?
提示 F2的氧化性大于Cl2,但由于F2与水发生反应:2F2+2H2O===4HF+O2,F2不与溶液中的Cl-反应,故F2通入NaCl溶液中得到的是O2而不是Cl2。
3.已知还原性I->Br->Cl->F-,试从原子结构的角度分析原因。
提示 微粒的还原性即失电子的能力。按I-→Br-→Cl-→F-的顺序,离子半径逐渐减小,原子核对最外层电子的吸引力逐渐增大,失去电子的能力逐渐减弱,故还原性逐渐减弱。
(2)与H2反应的难易程度及对应氢化物稳定性(由F2→I2)①与H2反应越来越难,生成的氢化物的稳定性逐渐减弱,还原性逐渐增强。②氢化物中HCl、HBr、HI的熔、沸点依次升高。(3)卤素单质与变价金属(如Fe)反应2Fe+3X2===2FeX3(X=F、Cl、Br)Fe+I2===FeI2
(1)溴是常温常压下唯一的液态的非金属单质。(2)卤素单质都有毒,溴有很强的腐蚀性,液溴易挥发,保存时要加一些水进行“水封”,碘可升华,遇淀粉溶液变蓝(检验I2)。(3)Cl2、Br2、I2易溶于有机溶剂苯、CCl4、汽油等。(4)F无正化合价。
【例题2】 下列关于卤族元素由上到下性质递变的叙述,正确的是( )
①单质的氧化性增强 ②单质的颜色加深 ③气态氢化物的稳定性增强 ④单质的沸点升高 ⑤阴离子的还原性增强A.①②③ B.②③④C.②④⑤D.④⑤
变式训练2 砹是现知原子序数最大的卤族元素,根据卤素性质的递变规律,对砹及其化合物的叙述,正确的是( )
A.与H2化合能力:At2>I2B.砹在常温下为白色固体C.砹原子的最外电子层上有7个电子D.砹能从NaCl溶液中置换出氯单质解析 从F到At,元素的非金属性逐渐减弱,单质与H2化合能力逐渐减弱,A项不正确;由F2到I2,单质的颜色依次加深,I2是紫黑色固体,则砹为黑色固体,B项不正确;卤族元素的原子,最外层上都有7个电子,C项正确;因氧化性:Cl2>At2,所以At2不能从NaCl溶液中置换出Cl2,D项不正确。答案 C
学习任务3 (核心素养)同主族元素原子结构与元素性质间的关系
一、知识要点1.元素的金属性、非金属性与原子得失电子的关系
(1)元素的金属性是指气态原子失去电子的性质,金属性的强弱取决于原子失去电子能力的强弱,越易失去电子,金属性越强,而与失去电子的多少没有必然联系。(2)元素的非金属性是指气态原子得到电子的性质,非金属性的强弱取决于原子得到电子能力的强弱,越易得到电子,非金属性越强,而与得到电子的多少没有必然联系。(3)同主族元素从上到下,原子半径逐渐增大,失电子能力逐渐增强,而得电子能力逐渐减弱,故金属性逐渐增强,非金属性逐渐减弱。
2.同主族元素性质的递变规律
从碱金属元素和卤素的性质来看,同主族从上至下元素及其典型化合物性质的递变规律如下表所示。
【素养解题】[典例示范] 下列关于主族元素的说法错误的是( )
A.同主族元素随着原子序数递增,元素金属性逐渐增强B.同主族元素随着原子序数递增,元素单质的熔、沸点逐渐升高 C.同主族元素原子最外层电子数都相同D.同主族元素随着原子序数递增其最高价氧化物对应水化物的酸性逐渐减弱,碱性逐渐增强
注意金属、非金属的区别
[主族元素性质判断题的解题思路]
三、对点训练1.下列叙述中能说明A金属比B金属活泼性强的是( )
A.A原子的最外层电子数比B原子的最外层电子数少B.A原子电子层数比B原子的电子层数多C.1 ml A从酸中置换H+生成的H2比1 ml B从酸中置换H+生成的H2多D.常温时,A能从水中置换出氢气,而B不能
解析 比较金属的活泼性不能根据最外层电子数的多少,如Li的最外层电子数比Ca少,但不如Ca活泼,故A错误;比较金属的活泼性不能根据原子电子层数的多少,如Na的电子层数比Cu少,但Na比Cu活泼,故B错误;比较金属的活泼性不能根据生成氢气的多少来判断,例如1 ml Al从酸中置换H+生成的H2比1 ml Mg从酸中置换H+生成的H2多,但Mg的活泼性强,故C错误;常温时,A能从水中置换出氢,而B不能,说明A易失去电子,则A的活泼性肯定比金属B的活泼性强,故D正确。答案 D
2.下列说法正确的是( )
A.F、Cl、Br原子的最外层电子数都是7,次外层电子数都是8B.从HF、HCl、HBr、HI酸性递增的事实,推出F、Cl、Br、I的非金属性递增规律C.卤素按F、Cl、Br、I的顺序,其非金属性逐渐减弱的原因是随着核电荷数增加电子层数增大起主要作用D.砹是原子序数最大的卤族元素,根据卤素性质的递变规律,砹易溶于水,难溶于CCl4
解析 F的次外层电子数为2,Br的次外层电子数为18,A项错误;元素的非金属性强弱可以根据其最高价氧化物对应水化物的酸性强弱比较,不能根据氢化物的酸性强弱比较,B项错误;由碘微溶于水、易溶于四氯化碳可推知,砹微溶于水,易溶于CCl4,D项错误。答案 C
3.在1961年,本生和基尔霍夫发现了一种新的碱金属元素,根据已学知识解答下列问题,帮助这两位科学家研究该元素。
(1)该元素单质的密度比水的密度大,则该元素可能是________。(2)该元素的单质与水反应比钾与水反应剧烈,但没有铯与水反应剧烈,由此可确定该元素是________。其确定依据是______________。(3)人类制备出该元素的单质比钠单质要晚得多,分析其中的原因:________________。
解析 (1)在碱金属元素形成的单质中,Li、Na、K的密度都小于水的密度,Rb、Cs、Fr的密度都大于水的密度,故该元素可能是Rb、Cs、Fr。(2)碱金属元素的单质按Li、Na、K、Rb、Cs的顺序活动性逐渐增强,因此可以根据单质与水反应的剧烈程度,得出该元素为Rb。(3)Rb和Na在自然界中全部以化合物形态存在,因此要制备它们的单质,需要把Rb+和Na+从其化合物中还原。由于金属单质还原性越强,其阳离子氧化性就越弱,越不易被还原,因此单质Rb比单质Na制备的晚。答案 (1)Rb、Cs、Fr(2)Rb 碱金属元素的单质按Li、Na、K、Rb、Cs的顺序活动性逐渐增强(3)Rb+的氧化性比Na+的弱,不易被还原
4.(1)常见卤素氢化物中最不稳定的是__________(写化学式)。
(2)下列单质熔、沸点随原子序数递增而升高的是_________________________(填字母,下同)。A.碱金属元素B.卤族元素(3)下列反应中,更剧烈的是__________。A.钠与水反应B.钾与水反应(4)取下列溶液分装两试管,再分别依次加入少量氯水和少量四氯化碳,用力振荡、静置后,四氯化碳层显紫红色的是__________。A.溴化钠溶液B.碘化钾溶液
解析 卤素中碘元素的非金属性最弱,氢化物中最不稳定的是HI;碱金属元素的单质熔、沸点随原子序数递增而降低,卤素单质熔、沸点随原子序数递增而升高;钾比钠活泼,与水反应更剧烈;氯水与NaBr、KI溶液分别生成Br2、I2,而二者的四氯化碳溶液分别为橙色、紫红色。答案 (1)HI (2)B (3)B (4)B
5.用A.质子数、B.中子数、C.核外电子数、D.最外层电子数、E.电子层数,填写下列空格:
(1)同位素种类由________决定。(2)元素种类由________决定。(3)某元素有无同位素由________决定。(4)核素相对原子质量由________决定。(5)主族元素的化学性质主要由________决定。(6)核电荷数由________决定。(7)碱金属元素原子失电子能力相对强弱由________决定。(8)原子得失电子能力相对强弱主要由________决定。
解析 (1)同位素种类的确定,既要确定元素(质子数),又要确定核素(中子数)。(2)确定元素种类只需确定质子数。(3)某元素有无同位素,已经确定了元素,只要由中子数确定同位素即可。注意跟(1)的区别。(4)核素相对原子质量的近似整数值等于该核素的质量数,则由质子数和中子数决定。(5)主族元素最外层电子数决定元素原子得失电子的能力,即化学性质。(6)核电荷数=质子数。
(7)碱金属元素原子电子层数越多,失电子能力越强,故决定碱金属元素原子失电子能力相对强弱的因素是电子层数。(8)电子层数相同时原子的最外层电子数越少,失电子能力越强,最外层电子数越多,得电子能力越强;最外层电子数相同,电子层数越多,失电子能力越强,得电子能力越弱,故原子得失电子能力的相对强弱主要由最外层电子数和电子层数决定。答案 (1)AB (2)A (3)B (4)AB (5)D (6)A (7)E (8)DE
高中化学人教版 (2019)必修 第一册第一节 原子结构与元素周期表一等奖ppt课件: 这是一份高中化学人教版 (2019)必修 第一册<a href="/hx/tb_c161996_t3/?tag_id=26" target="_blank">第一节 原子结构与元素周期表一等奖ppt课件</a>,共24页。PPT课件主要包含了不稳定,过渡元素过渡金属,碱金属元素,卤族元素,稀有气体元素,还原性,钾的反应更为剧烈,原子最外层电子相同,原子半径较大,失电子能力更强等内容,欢迎下载使用。
人教版 (2019)必修 第一册第一节 原子结构与元素周期表试讲课课件ppt: 这是一份人教版 (2019)必修 第一册第一节 原子结构与元素周期表试讲课课件ppt,共17页。
高中化学人教版 (2019)选择性必修2第二节 原子结构与元素的性质获奖课件ppt: 这是一份高中化学人教版 (2019)选择性必修2第二节 原子结构与元素的性质获奖课件ppt,共30页。PPT课件主要包含了元素周期律,原子半径,同主族元素从上到下,电子能层数增多,原子半径增大,核电荷数增大,原子半径减小,电离能,电离能的递变规律,电负性等内容,欢迎下载使用。













