



科粤版(2024)九年级下册(2024)物质溶解的量说课课件ppt
展开 这是一份科粤版(2024)九年级下册(2024)物质溶解的量说课课件ppt,共25页。PPT课件主要包含了固体的溶解度S,溶解度曲线的意义,如氯化钠NaCl,“线”,饱和溶液,溶解性,溶解度,不饱和溶液,相互转化,课堂小结等内容,欢迎下载使用。
在一定温度下,某固态物质在100g溶剂中达到饱和状态时所溶解的质量,叫作这种物质在这种溶剂中的溶解度。
在 100g 溶剂里(一般指水)
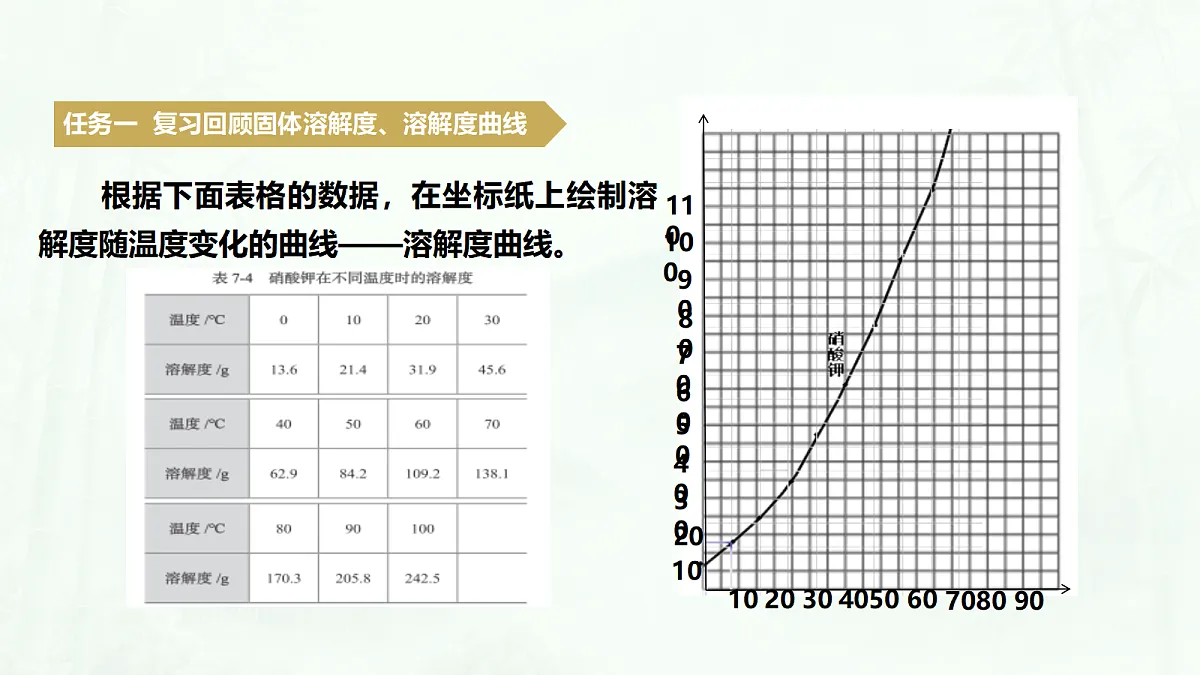
任务一 复习回顾固体溶解度、溶解度曲线
根据下面表格的数据,在坐标纸上绘制溶解度随温度变化的曲线——溶解度曲线。
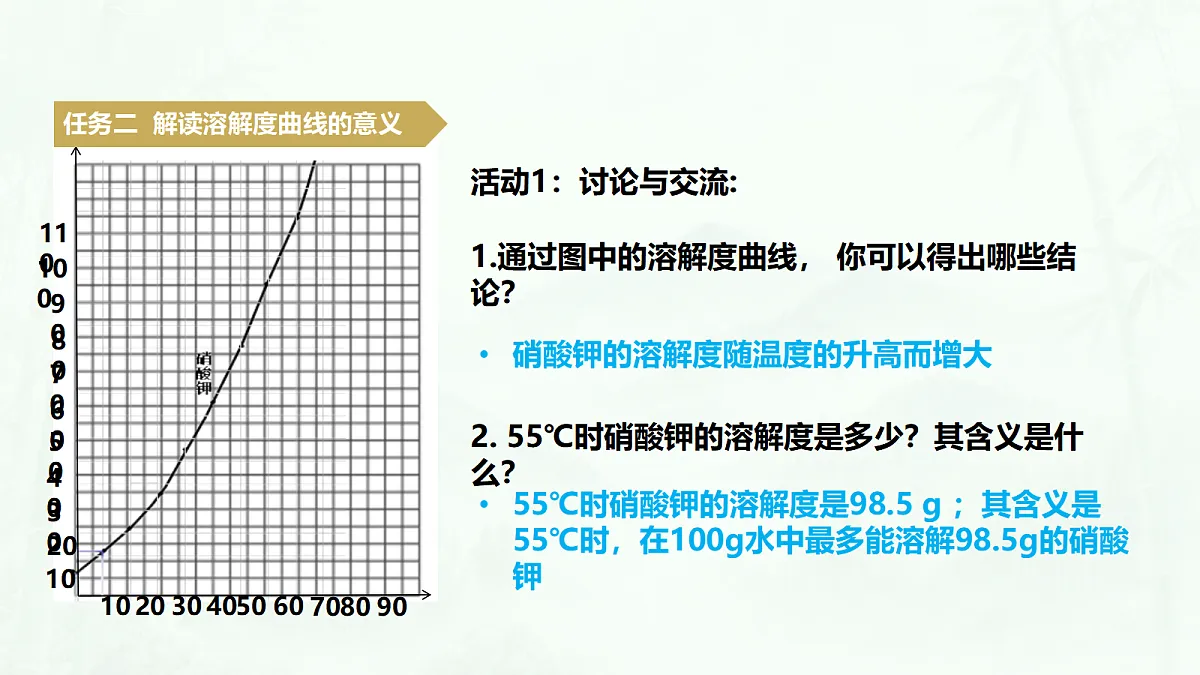
活动1:讨论与交流:1.通过图中的溶解度曲线, 你可以得出哪些结论?2. 55℃时硝酸钾的溶解度是多少?其含义是什么?
任务二 解读溶解度曲线的意义
硝酸钾的溶解度随温度的升高而增大
55℃时硝酸钾的溶解度是98.5 g ;其含义是55℃时,在100g水中最多能溶解98.5g的硝酸钾
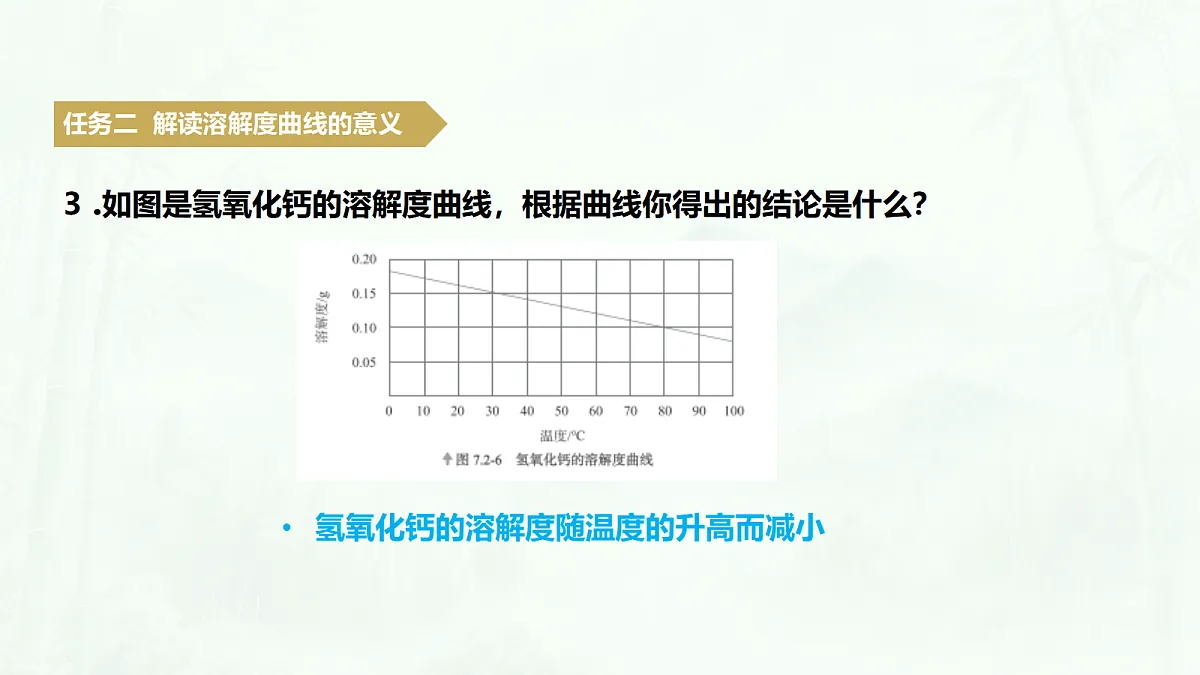
3 .如图是氢氧化钙的溶解度曲线,根据曲线你得出的结论是什么?
氢氧化钙的溶解度随温度的升高而减小
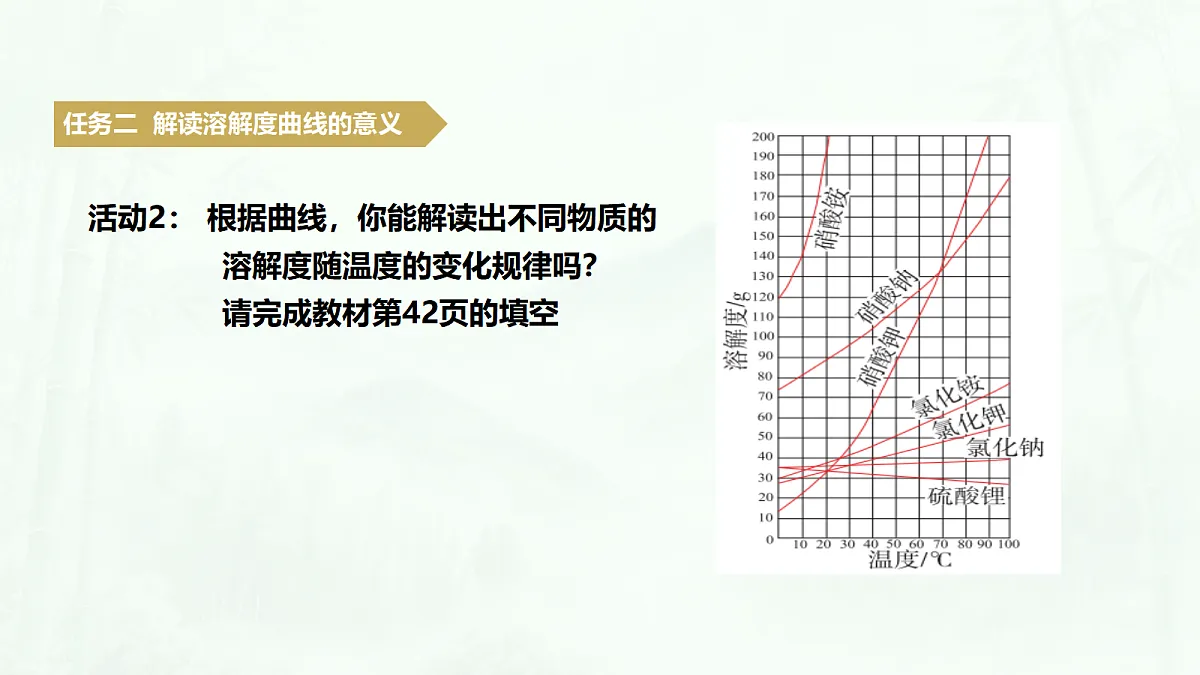
活动2: 根据曲线,你能解读出不同物质的 溶解度随温度的变化规律吗? 请完成教材第42页的填空
(1)多数固体溶解度随温度的升高而增大
(2)少数固体溶解度受温度的影响很小
(3)极少数固体溶解度随温度的升高而减小
如:氢氧化钙Ca(OH)2 、硫酸锂
如:硝酸钾 KNO3
活动3:全面解读溶解度曲线,请回答以下问题:
1.a的含义: 。2.60 ℃时,采取哪些措施能将近饱和的硝酸钾溶液转化为饱和溶液?
3.将60℃时硝酸钾的饱和的溶液降温到40℃,溶液的状态是 (“饱和状态”、“不饱和状态”或“无法判断”)。
4.将60℃时硝酸钾的饱和的溶液升温到70℃,溶液的状态是 。
任务三 应用溶解度曲线图
活动3:全面解读溶解度曲线,并回答以下问题:
1. 请解读硝酸钾溶解度曲线上a点的 含义: 。
60℃时,硝酸钾的溶解度为110g
2. 60 ℃时,采取哪些措施能将近饱和的硝酸钾溶液 转化为饱和溶液?
增加溶质/蒸发溶剂/降低温度
3. 将60℃时硝酸钾的饱和的溶液降温到20℃,此时溶液的状态是 (“饱和状态”、“不饱和状态”或“无法判断”)。
4. 试确定一份60℃时硝酸钾的饱和溶液中, 溶质和溶剂的质量比是 。
1.根据右图信息判断,下列叙述不正确的是( ) A. 硝酸钾的溶解度随温度升高而增大 B. t1℃时,氯化钠和硝酸钾的溶解度相同 C. 将t2℃时的硝酸钾饱和溶液降温到t1℃,有晶体析出 D. t2℃时,80g硝酸钾溶于100g水中可制得饱和溶液
2.“天气瓶”内含有的硝酸钾和氯化铵可以控制在晶体高速生长过程中的连续成核。某兴趣小组的同学进行了如图2所示实验,R是硝酸钾、氯化铵中的一种物质。硝酸钾和氯化铵的溶解度曲线如图1所示。
(1)硝酸钾和氯化铵两种物质的溶解度均随温度的升高而 (2)图1可知:t1℃时,氯化铵饱和溶液中溶质与溶液的质量比为 (3)结合图1和图2判断:烧杯内物质R是 ①、②、③三种情况下,一定是饱和溶液的有 (填序号)
3. 20℃时,氯化钠的溶解度为36g。下列说法正确的是( )A. 20℃时,100g水中溶解36g氯化钠形成饱和溶液B. 20℃时,50g水中最多溶解18g氯化钠C. 20℃时,136g氯化钠溶液中溶质质量为36gD. 升温至30℃,氯化钠溶解度一定增大
答案:AB解析:A正确,符合溶解度定义的四要素(一定温度、100g溶剂、饱和状态、质量单位为g)。B正确,50g水最多溶解18g氯化钠(36g × 0.5)。C错误,136g溶液包含溶质36g和溶剂100g,但溶液质量应为136g(36g+100g)。D错误,氯化钠溶解度受温度影响较小,但并非一定增大,需根据实际曲线判断。
4. 将60℃的硝酸钾饱和溶液冷却至20℃,析出晶体后过滤。下列说法正确的是( )A. 滤液为不饱和溶液B. 滤液中溶质质量分数减小C. 析出晶体后的溶液仍为饱和溶液D. 硝酸钾溶解度随温度降低而增大
答案:BC解析:C正确,降温析晶后的溶液仍为20℃时的饱和溶液。B正确,降温后溶解度降低,溶质质量分数减小。
5. 配制10%的氯化钠溶液时,量取水时俯视量筒刻度线,会导致溶液浓度( )A. 偏大B. 偏小C. 不变D. 无法判断
答案:A解析:俯视导致量取的水体积偏少,溶质质量分数偏大。
6. 下列关于溶解度的说法,正确的是( )A. 100g水中溶解20g某物质刚好饱和,则该物质的溶解度为20gB. 20℃时,100g水中溶解了10g某物质,则20℃时该物质的溶解度为10gC. 20℃时,100g水中溶解32g KNO₃刚好饱和,则20℃时KNO₃的溶解度为32g
答案:A解析:A错误:t₁℃时,NaCl溶解度曲线高于KNO₃(交点左侧),实际NaCl溶解度更大。B正确:KNO₃曲线呈上升趋势,受温度影响显著。C正确:KNO₃溶解度随温度变化大,降温时析出晶体更多。
7. 从KNO₃和NaCl的混合溶液中提纯KNO₃,应采用的方法是( )A. 蒸发结晶 B. 降温结晶
答案:B解析:KNO₃溶解度受温度影响大,NaCl则较小。降温结晶:适用于溶解度随温度显著增大的物质(如KNO₃),冷却热饱和溶液析出晶体。蒸发结晶:适用于溶解度受温度影响小的物质(如NaCl)。
8. 关于溶解度的定义,下列说法正确的是( )A. 20℃时,100g水中溶解了30g NaCl,则NaCl的溶解度为30gB. 40℃时,KNO₃在100g水中达到饱和状态时溶解度为63.9gC. 溶解度与溶剂种类无关D. 饱和溶液中溶质质量一定等于溶解度
答案:B解析:溶解度需满足四要素:一定温度、100g溶剂、饱和状态、质量(g)。A未说明是否饱和;C错误,溶解度受溶剂影响(如碘易溶于酒精难溶于水);D错误,溶解度是质量值,溶液中的溶质质量可能小于溶解度(如未饱和溶液)。
9. 下列现象与气体溶解度无关的是( )A. 打开汽水瓶盖时液体喷出B. 鱼类在夏季常浮头呼吸C. 加热冷水至沸腾前有气泡逸出D. 氢氧化钠固体溶于水放热
答案:D解析:A、B、C均与气体溶解度随压强减小或温度升高而降低有关;D是固体溶解的能量变化,与气体无关。
10. 从KNO₃和NaCl混合物中提纯KNO₃,操作正确的是( )A. 蒸发结晶→过滤B. 溶解→降温结晶→过滤C. 溶解→蒸发浓缩→趁热过滤D. 加入足量水搅拌→过滤
答案:B解析:KNO₃溶解度随温度变化大(陡升型),适用降温结晶;NaCl溶解度受温度影响小(缓升型),适用蒸发结晶。
相关课件
这是一份科粤版(2024)九年级下册(2024)物质溶解的量说课课件ppt,共25页。PPT课件主要包含了固体的溶解度S,溶解度曲线的意义,如氯化钠NaCl,“线”,饱和溶液,溶解性,溶解度,不饱和溶液,相互转化,课堂小结等内容,欢迎下载使用。
这是一份初中化学科粤版(2024)九年级下册(2024)物质溶解的量课文课件ppt,共25页。PPT课件主要包含了固体的溶解度S,溶解度与溶解性的关系,学以致用,问题探讨,课堂小结,溶解性,溶解度,评价检测,评价检测综合实践等内容,欢迎下载使用。
这是一份科粤版(2024)九年级下册(2024)物质溶解的量课堂教学课件ppt,共25页。PPT课件主要包含了光照营养液,饱和溶液和不饱和溶液,固体又溶解,固体又析出,固体有剩余,可能不饱和溶液,饱和溶液,不饱和溶液,①增加溶剂,①增加溶质等内容,欢迎下载使用。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)




