

所属成套资源:中考化学一轮复习专项巩固练习 三(含答案解析)
中考化学一轮复习专项巩固练习 溶解度曲线问题汇总(六)(含答案解析)
展开 这是一份中考化学一轮复习专项巩固练习 溶解度曲线问题汇总(六)(含答案解析),共26页。
A.甲的溶解度比乙大
B.t℃时,甲溶液的浓度等于乙溶液的浓度
C.冷却甲的热饱和溶液可获得甲的晶体
D.t℃时,在50g水里加入25g固体乙,充分溶解,可得到75g溶液
2.如图为KCl和Na2CO3的溶解度曲线,下列说法不正确的是
A.T2℃时,Na2CO3饱和溶液质量分数为49.0%
B.将两物质的饱和溶液由T1℃升温至T3℃,均无固体析出
C.T4℃时,分别将等质量的KCl和Na2CO3溶于水配成饱和溶液,所得溶液的质量前者小于后者
D.若KCl溶液中含有少量Na2CO3,可采取蒸发浓缩、降温至T2℃结晶、过滤等操作提纯
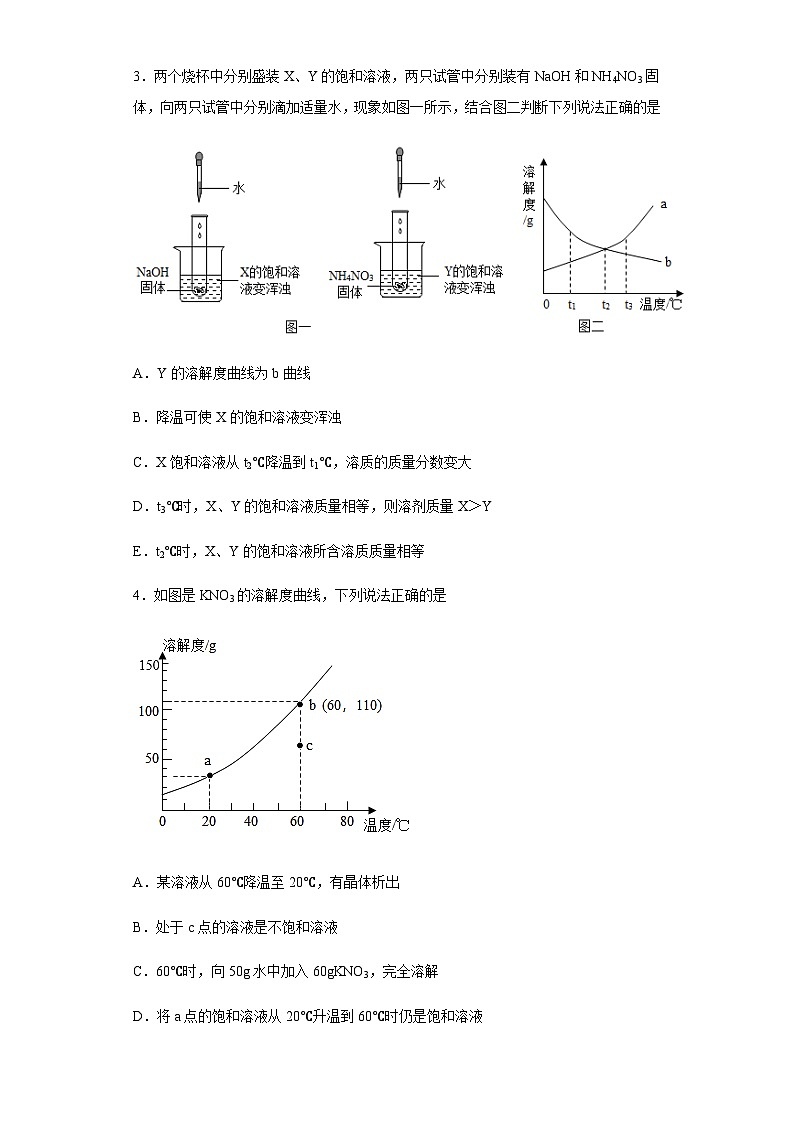
3.两个烧杯中分别盛装X、Y的饱和溶液,两只试管中分别装有NaOH和NH4NO3固体,向两只试管中分别滴加适量水,现象如图一所示,结合图二判断下列说法正确的是
A.Y的溶解度曲线为b曲线
B.降温可使X的饱和溶液变浑浊
C.X饱和溶液从t2℃降温到t1℃,溶质的质量分数变大
D.t3℃时,X、Y的饱和溶液质量相等,则溶剂质量X>Y
E.t2℃时,X、Y的饱和溶液所含溶质质量相等
4.如图是KNO3的溶解度曲线,下列说法正确的是
A.某溶液从60℃降温至20℃,有晶体析出
B.处于c点的溶液是不饱和溶液
C.60℃时,向50g水中加入60gKNO3,完全溶解
D.将a点的饱和溶液从20℃升温到60℃时仍是饱和溶液
5.如图为 A、B、C 三种物质的溶解度曲线,下列叙述中错误的是
A.t1℃时,50g 水中加入 25g B 形成的溶液质量为 70g
B.t2℃时,三种物质的溶解度由大到小的顺序为:A>B>C
C.要使A 从其浓溶液中析出,可采用冷却热饱和溶液法
D.要将C 的不饱和溶液转化为饱和溶液可以采取降温的方法
6.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是
A.甲物质可能是Ca(OH)2固体
B.20℃时,甲、乙溶液中溶质质量分数一定相等
C.从乙的饱和溶液中析出晶体,可用降温结晶的方法
D.30℃时,向甲的饱和溶液中加入100g水,甲的溶解度不变
7.低钠盐是以碘盐为原料,再添加了一定量的氯化钾等物质。如图是氯化钠和氯化钾的溶解度曲线,下列说法正确的是
A.20℃时,氯化钾溶液比氯化钠溶液的溶质质量分数大
B.氯化钠和氯化钾都属于易溶物
C.80℃时,将等质量的两种物质的饱和溶液降温到20℃,氯化钾析出晶体少
D.80℃时,氯化钾饱和溶液中溶质质量分数为50%
8.如图是甲、乙、丙三种物质的溶解度曲线,下列说法不正确的是
A.30℃时,把10g丙溶解在50g水中,得到丙的饱和溶液,此时溶液中丙的质量分数约为9%
B.60℃时,把等质量的甲、乙、丙三种饱和溶液降温至0℃,析出晶体的质量由大到小的顺序:甲>乙>丙
C.将甲的饱和溶液变为不饱和溶液,可采用升高温度的方法
D.30℃时,甲溶液的溶质质量分数为30%
9.如图为氯化铵和硫酸钠的溶解度曲线。下列说法错误的是
A.氯化铵的溶解度随着温度的升高而升高
B.30℃时,氯化铵和硫酸钠的溶解度相同
C.将60℃的硫酸钠饱和溶液降温至40℃,有晶体析出
D.在30℃到60℃范围内,硫酸钠饱和溶液在40℃时溶质质量分数最大
10.如图,图一是 A、B 两种物质的溶解度曲线。t1℃时,将等质量的 A 和 B 分别加入盛有 100g 水的两只烧杯中,充分搅拌并恢复至原温度后,现象如图二所示。下列说法正确的是
A.烧杯甲中加入的是 A,烧杯乙中加入的是 B
B.烧杯甲中溶液溶质的质量分数小于烧杯乙中溶液溶质的质量分数
C.将两个烧杯中的溶液混合,充分搅拌后,烧杯中一定还有剩余固体
D.将温度升高到 t2℃,两烧杯内溶液中溶质的质量分数相等(不考虑水的蒸发)
11.20℃时,将等质量ab两种固体分别放入100克水中充分溶解,如图甲,然后升温到50℃,如图乙,图丙是ab两种固体的溶解度曲线,下列说法正确的是
A.图甲中a、b形成的两溶液中溶质的质量相等
B.乙中a、b形成的两溶液一定都是不饱和溶液
C.丙中N表示a物质的溶解度曲线
D.30℃时,要配制等质量ab各自的饱和溶液,需水的质量b>a
12.如图是a、b、c三种固体物质的溶解度曲线。下列说法中正确的是
A.a的溶解度大于c的溶解度
B.在tl℃时,a、c两种饱和溶液中溶质的质量相同
C.c的不饱和溶液由t2℃降温至t1℃时,变成饱和溶液
D.要从b溶液中得到b,通常可采用蒸发结晶的方法
13.如图所示是不含结晶水的甲、乙、丙三种固体物质的溶解度曲线,下列说法中正确的是
A.t2℃时,甲、丙两溶液的溶质质量分数一定相等
B.t1℃时,取12.5g乙加入50g水中,可得到饱和溶液
C.取相同质量的甲、乙、丙配制t3℃时的饱和溶液,所得溶液的质量由大到小的关系是丙>乙=甲
D.要使t1℃时的甲、丙的饱和溶液均析出晶体,可采用升高温度的方法
14.如图是甲、乙两种物质(不含结晶水)的溶解度曲线。下列说法中正确的是
A.甲的溶解度大于乙的溶解度
B.t2℃时,甲和乙两者的饱和溶液浓度相同
C.t1℃时,100克水中加入25克甲物质形成饱和溶液
D.t2℃时将甲、乙的饱和溶液降温至t1℃,甲析出的晶体多
15.如图是甲、乙、丙三种固体物质的溶解度曲线,下列说法正确的是
A.t1℃时,三种固体物质的溶解度关系为乙<甲=丙
B.t2℃100g甲物质饱和溶液中含有60g甲
C.将丙物质饱和溶液变为不饱和溶液,可采用升温的方法
D.t2℃时,分别用100g水配制甲、乙的饱和溶液,再降温到t1℃,析出无水晶体的质量:甲>乙
16.t2℃时,将甲、乙两种固体物质各80g分别放到盛有100g水的烧杯中,充分溶解后,恢复到t2℃,现象如图I。甲和乙的溶解度曲线如图Ⅱ。下列说法错误的是
A.固体甲对应的溶解度曲线是b
B.M点表示在t1℃时,甲和乙两种物质的溶解度相等
C.t2℃时,向烧杯①的溶液中继续加入15g甲物质,充分搅拌后,所得溶液是饱和溶液
D.将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,两溶液中溶质质量分数甲>乙
17.如图为甲、乙、丙三种固体物质的溶解度曲线。下列说法正确的是
A.甲、乙、丙三种物质中溶解度最小的是丙
B.20℃时,甲和乙的溶液溶质质量分数一定相等
C.若甲中含有少量乙时,可用降温结晶的方法提纯甲
D.将甲、乙、丙饱和溶液由50℃降温到10℃时,所得溶液中溶质质量由大到小的顺序为丙>乙>甲
18.甲、乙、丙三种固体物质(均不含结晶水)的溶解度曲线如图所示。下列说法正确的是
A.t1℃时,10克甲放入50克水中可得到60克溶液
B.t1℃时,甲和丙的饱和溶液中溶质质量相同
C.等质量甲、乙两种物质的溶液从t2℃降到t1℃时,析出晶体最多的是甲
D.三种物质的饱和溶液从t2℃降到t1℃,所得溶液溶质质量分数:乙>甲>丙
19.甲、乙两种物质的溶解度曲线如图所示,下列说法正确的是
A.甲物质的溶解度大于乙物质的溶解度
B.甲中含有少量的乙,可以用蒸发溶剂的方法提纯甲
C.t2℃时,将等质量的甲、乙两种物质的饱和溶液分别降温至t1℃,析出晶体的质量甲一定大于乙
D.t2℃时,乙溶液中溶质的质量分数一定小于甲溶液中溶质的质量分数
20.硝酸钠的溶解度曲线如图所示,下列说法正确的是
A.25℃时,NaNO3饱和溶液的溶质质量分数为92%
B.将60℃时的NaNO3饱和溶液降温至25℃,有32g晶体析出
C.25℃时,将48gNaNO3加入50g水中充分溶解,所得溶液质量为98g
D.将25℃时的NaNO3饱和溶液升温至60℃,硝酸钠的溶解度变大
21.NaCl和KNO3的溶解度曲线如图所示。下列说法正确的是
A.20℃时,KNO3饱和溶液溶质质量分数为31.6%
B.二者的溶解度都随温度升高而增大
C.40℃时,KNO3饱和溶液中溶质质量63.9g
D.60℃时KNO3溶液的浓度比20℃大
22.如图是甲、乙两种固体物质(不含结晶水)在水中的溶解度曲线,下列说法正确的是
A.甲物质的溶解度大于乙物质的溶解度
B.t2℃时,100g乙的饱和溶液中溶质质量为20g
C.将t2℃时的甲、乙两种物质的饱和溶液降温至t1℃时,都会析出晶体
D.甲物质含有少量乙,可用冷却热的饱和溶液的方法提纯甲
23.如图是甲、乙、丙三种固体物质的溶解度曲线。下列叙述正确的是
A.甲的溶解度大于乙的溶解度
B.t2℃时,20g丙能溶解于50g水中形成70g溶液
C.若要将N点的甲溶液转变为M点的甲溶液,可采取恒温蒸发溶剂的方法
D.t3℃时,将甲、乙、丙三种物质的饱和溶液降温至t2℃,所得溶液溶质质量分数的大小关系为甲=丙乙,而丙的饱和溶液降温后,溶解度增大,溶液变为不饱和溶液,没有晶体析出,因此降温至0℃,析出晶体的质量由大到小的顺序:甲>乙>丙,故选项说法正确;
C、将甲的饱和溶液变为不饱和溶液,甲物质溶解度是随温度的升高而增大,可采用升高温度的方法,故选项说法正确;
D、30℃时,甲物质的溶解度是30g,甲的饱和溶液的溶质质量分数为×100%≈23.1%,故选项说法不正确。
故选D。
9.C
【详解】A、在溶解度曲线图上,横坐标是温度,纵坐标是溶解度。由图可知:氯化铵的溶解度随温度的升高而增大,故说法正确;
B、30℃时,氯化铵、硫酸钠的溶解度曲线交于一点,所以30℃时,氯化 铵、硫酸钠的溶解度相等,故说法正确;
C、将60℃的硫酸钠饱和溶液降温至40℃的过程中,硫酸钠的溶解度变大,溶液由饱和状态变成不饱和溶液,不会有晶体析出,故说法错误;
D、溶解度是一定温度下,100g溶剂里达到饱和时,所溶解的溶质的质量;饱和溶液溶质的质量分数,在30℃ ~60℃范围内,硫酸钠饱和溶液在40℃时溶解度最大,其饱和溶液溶质质量分数最大,故说法正确;
故选C。
10.D
【详解】A、根据溶解度曲线可知,t1℃时,B的溶解度大于A的溶解度,将等质量的A和B分别加入盛有100g水的两只烧杯中,物质B溶解的比物质A多,甲中固体全部溶解,乙中有固体剩余,所以,乙是A物质的饱和溶液,甲是B物质的溶液;故说法错误;
B、等质量的A和B分别加入盛有100g水的两只烧杯中,根据,甲烧杯中全部溶解,乙烧杯中有部分未溶解的固体,故烧杯甲中溶液溶质的质量分数大于烧杯乙中溶液溶质的质量分数,故说法错误;
C、将两个烧杯中的溶液混合,充分搅拌后,烧杯中不一定有剩余固体,混合后溶剂的质量增加至200g,由于不知道加入固体A的质量,所以乙烧杯中剩余未溶解的物质可能全部溶解,也可能有剩余,故说法错误;
D、A、B两种物质的溶解度曲线随温度的升高而增大,将温度升高到t2℃,A、B的溶解度都增大,烧杯甲中不会有固体析出;因为t2℃时,A和B的溶解度相等,即两种物质在此温度下,在相同质量水中的溶解能力相同,由于甲中固体全部溶解,则乙中剩余固体也会全部溶解,此时甲中溶质质量与乙中溶质质量相等,根据可知,则两烧杯内溶液中溶质的质量分数一定相等,故说法正确。
故选D。
11.B
【分析】根据固体的溶解度表中的数据,可以查出某物质在一定温度下的溶解度,从而确定物质溶解度曲线;可以比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小;可以判断物质的溶解度随温度变化的变化情况,从而判断饱和溶液和不饱和溶液相互转化的方法。
【详解】A、根据图示,甲中a有未溶解的固体,甲中a、b形成的两溶液中溶质的质量不相等,该选项说法错误;
B、20℃时,N的溶解度大于M,结合甲中信息可知,丙中N表示b物质的溶解度曲线,乙中a、b形成的两溶液一定都是不饱和溶液,是因为50℃b是不饱和溶液,a的溶解度比b大,更是不饱和溶液,该选项说法正确;
C、20℃时,N的溶解度大于M,结合甲中信息可知,丙中N表示b物质的溶解度曲线,该选项说法错误;
D、30℃时a、b溶解度相等,要配制等质量a、b各自的饱和溶液,需要水的质量:b=a,该选项说法错误。
故选:B。
12.D
【详解】A、由于没有说明温度,说法错误;
B、由于在tl℃时,a和c的溶解度相等,即它们的饱和溶液中溶质的质量分数相等,因为没有溶液质量,无法计算溶质质量,说法错误;
C、由于的溶解度随温度的降低而增大,因此的不饱和溶液由t2℃降温至t1℃时,不饱和溶液不可能会变成饱和溶液,说法错误;
D、由于B的溶解度受温度的影响很小,因此应采取蒸发溶剂的方法使溶质从溶液中结晶析出,说法正确;
故选D项。
13.C
【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性,②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质的质量分数的大小,③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
【详解】A、t2℃时,甲、丙两溶液的状态不能确定,所以溶质质量分数不能确定,故选项错误;
B、t1℃时,乙物质的溶解度大于25g,取12. 5g乙加入50g水中,可得到不饱和溶液,故选项错误;
C、t3℃时,甲、乙物质的溶解度相等,大于丙物质的溶解度,所以取相同质量的甲、乙、丙配制t3℃时的饱和溶液,所得溶液的质量由大到小的关系是丙>乙=甲,故选项正确;
D、甲物质的溶解度随温度的升高而增大,丙物质的溶解度随温度的升高而减小,所以要使此时的甲、丙的饱和溶液均析出晶体,可采用蒸发溶剂的方法,故选项错误。
故选:C。
14.B
【详解】A、比较溶解度需要指明温度,否则无法比较,选项错误;
B、t2℃时,甲和乙的溶解度曲线交于一点说明该温度下甲和乙的溶解度相等,则该温度下甲和乙两者的饱和溶液浓度相同,选项正确;
C、t1℃时,甲的溶解度是30g,说明该温度下,100g水中最多能溶30g甲,则该温度下,100克水中加入25克甲物质形成的是不饱和溶液,选项错误;
D、t2℃时将甲、乙的饱和溶液降温至t1℃,如图所示,虽甲的溶解度受温度影响较乙大,但未指明原溶液的质量,则无法判断析出溶质的多少,故无法判断甲析出的晶体多,选项错误;
答案为:B。
15.D
【详解】A、通过分析溶解度曲线可知,t1℃时,三种固体物质的溶解度关系为乙>甲=丙;故A错误;
B、t2℃,甲物质的溶解度是60g,即为100g水中最多溶解甲物质为60g,所以100g+60g=160g甲物质饱和溶液中含有60g甲,故B错误;
C、丙物质的溶解度随温度的升高而减小,所以将丙物质饱和溶液变为不饱和溶液,可采用降温的方法,故C错误;
D、t2℃时,甲的溶解度大于乙的溶解度,故分别用100g水配制甲、乙的饱和溶液,此时溶解甲的质量>溶解乙的质量,降温后溶剂质量不变,溶液仍为饱和溶液,t1℃,乙的溶解度大于甲的溶解度,故100g水中达到饱和溶解乙的质量>溶解甲的质量。所以降温后析出无水晶体的质量:甲﹥乙。故D正确;
故选D。
16.A
【详解】A、t2℃时,a物质的溶解度为90g,b物质的溶解度小于65g;t2℃时将甲、乙两种固体物质各80g分别放到盛有100g水的烧杯中,充分溶解后,恢复到t2℃,加入甲物质的烧杯底部没有固体剩余,加入乙物质的烧杯底部有固体剩余,所以固体甲对应的溶解度曲线是a,说法错误;
B、溶解度曲线的交点表示该温度下物质的溶解度相等,M点的含义是在t1℃时,甲和乙两种物质的溶解度相等,说法正确;
C、t2℃时,a物质(甲物质)的溶解度是90g,向烧杯①的溶液中继续加入15g甲物质,则烧杯中一共有95g甲物质,充分搅拌后,甲物质不能完全溶解,所得溶液是t2℃时的饱和溶液,说法正确;
D、甲物质的溶解度随温度的降低而减小,乙物质的溶解度随温度的降低而增大,所以将t2℃等质量的甲、乙饱和溶液分别降温到t1℃时,甲溶液有固体析出,其溶质质量分数依据t1℃时的溶解度计算,乙溶液的溶质质量分数依据t2℃时的溶解度计算,而甲物质t1℃时的溶解度大于乙物质t2℃时的溶解度,所以两溶液中溶质质量分数甲>乙,说法正确;
故选A。
17.C
【详解】A、溶解度大小跟温度密切相关,温度不确定时,甲、乙、丙的溶解度大小关系不能确定,故A不符合题意;
B、20℃时,甲和乙溶解度相等,此时的甲、乙饱和溶液溶质质量分数一定相等,但是二者的不饱和溶液溶质质量分数的大小关系不确定,故B不符合题意;
C、由图知,甲物质的溶解度随温度的升高而增大且受温度的影响较大,乙物质的溶解度也随温度的升高而增大但受温度的影响不大,所以若甲中含有少量乙时,可用降温结晶的方法提纯甲,故C符合题意;
D、将甲、乙、丙饱和溶液由50℃降温到10℃时,所得溶液中溶质质量无法比较,因为甲、乙、丙饱和溶液的质量不确定,故D不符合题意。
故选C。
18.D
【详解】A、由图可知,t1℃时,甲的溶解度是10g,即100g水中最多溶解10g的甲,故10克甲放入50克水中只能溶解5g的甲物质,故可得到50g+5g=55g溶液,故A错误,不符合题意;
B、图可知,t1℃时,甲和丙的溶解度相等,故其饱和溶液中溶质质量分数相同,但是不确定其饱和溶液的质量,故无法判断两者饱和溶液中溶质的质量,故B错误,不符合题意;
C、等质量甲、乙两种物质的溶液从t2℃降到t1℃,由于没有确定是否为饱和溶液,故不能确定两物质哪个析出的晶体多,故C错误,不符合题意;
D、三种物质的饱和溶液从t2℃降到t1℃,由图中可以看出,甲、乙的溶解度都下降,而丙的溶解度升高,在t1℃时,溶解度为 乙>甲=丙,但丙的溶解度升高,变为了不饱和溶液,溶质质量分数要按t2℃时的溶解度计算,故此时的溶质质量分数乙>甲>丙,故D正确,符合题意;
故选D。
19.C
【详解】A、比较溶解度需指明温度,否则无法比较,选项错误;
B、如图所示,甲的溶解度随温度影响大,乙的溶解度随温度影响小,甲中含有少量的乙,可以用降温结晶的方法提纯甲,选项错误;
C、如图所示,甲的溶解度随温度影响大,随温度的降低明显减小,乙的溶解度随温度影响小,随温度降低减小的量比甲少,因此t2℃时,将等质量的甲、乙两种物质的饱和溶液分别降温至t1℃,析出晶体的质量甲一定大于乙,选项正确;
D、如图所示,t2℃时,甲的溶解度比乙大,说明该温度下甲的饱和溶液溶质质量分数比乙的饱和溶液溶质质量分数大,但若不能确定是否饱和则无法比较,选项错误;
答案为:C。
20.D
【分析】根据固体的溶解度曲线可以:①查出某物质在一定温度下的溶解度,从而确定物质的溶解性;②比较不同物质在同一温度下的溶解度大小,从而判断饱和溶液中溶质质量分数的大小;③判断物质的溶解度随温度变化的变化情况,从而判断通过降温结晶还是蒸发结晶的方法达到提纯物质的目的。
【详解】A、25℃时,NaNO3饱和溶液的溶质质量分数为: ,故A错误;
B、没说明饱和溶液的质量,不能判断将60℃时的NaNO3饱和溶液降温至25℃,析出晶体的多少,故B错误;
C、25℃时,NaNO3的溶解度是92g,即在该温度下,100g水中最多溶解92g,则50g水中最多溶解46g,所以25℃时,将48gNaNO3加入50g水中充分溶解,所得溶液质量为96g,故C错误;
D、由溶解度曲线可知:将25℃时的NaNO3饱和溶液升温至60℃,硝酸钠的溶解度变大,故D正确。
故选D。
【点睛】本题难度不是很大,主要考查了固体的溶解度曲线所表示的意义,及根据固体的溶解度来解决相关的问题,从而培养分析问题、解决问题的能力。
21.B
【详解】A、由图可知,20℃时,KNO3的溶解度为31.6g,此时其饱和溶液的溶质质量分数=×100%≈24.0%,选项错误;
B、由图可知,随温度的升高,两种物质的溶解度曲线都逐渐升高,说明二者的溶解度都随温度升高而增大,选项正确;
C、40℃时,KNO3的溶解度为63.9g,但题文中没有指明饱和溶液的质量,所以不能明确饱和溶液中溶质的质量,选项错误;
D、由图可知,60℃时KNO3的溶解度为110.0g,20℃时KNO3的溶解度为31.6g,则60℃时KNO3饱和溶液的浓度比20℃时KNO3的饱和溶液的浓度大,题文中没有明确两种温度下溶液的状态,所以不能比较两种温度下两种物质的溶液的浓度关系,选项错误,故选B。
22.D
【详解】A、根据溶解度曲线可知,当温度低于t1℃时,乙的溶解度高于甲的溶解度,当温度高于t1℃时,乙的溶解度低于甲的溶解度,不符合题意;
B、根据图示可知t2℃时,乙物质的溶解度是20g,即100g水中最多溶解20g乙物质达到饱和状态,溶液质量为120g,不符合题意;
C、乙物质的溶解度随温度的降低而增大,故将t2℃时的甲、乙两种物质的饱和溶液降温至t1℃时,乙溶液会变成不饱和溶液,不会析出晶体,不符合题意;
D、甲物质的溶解度随温度的升高而增大,乙物质的溶解度随温度的升高而下降,故甲物质含有少量乙,可用冷却热的饱和溶液的方法提纯甲,符合题意;
故选D。
23.C
【详解】A、对比物质的溶解度需要说明温度,A选项没有说明温度,无法对比溶解度,叙述错误,不符合题意;
B、t2℃时丙物质的溶解度是30g,即100g水中最多溶解30g,故将20g丙加入50g水中只能溶解15g,则形成溶液的质量为15g+50g=65g,叙述错误,不符合题意;
C、N点是t3℃时甲的不饱和溶液,M点是t3℃时甲的饱和溶液,则由N点的甲溶液转变为M点的甲溶液就是由不饱和溶液变为饱和溶液,可以采取的方法有恒温蒸发溶剂或加溶质,叙述正确,符合题意;
D、t3℃时,将甲、乙、丙三种物质的饱和溶液降温到t2℃时,甲乙的溶解度减小,析出晶体,但依然是饱和溶液,溶质质量分数减小,而丙的溶解度增大,溶质、溶剂质量均不变,溶质的质量分数与t3℃时一样,而t2℃时乙的溶解度大于甲的溶解度大于t3℃时丙的溶解度,故所得溶液中溶质质量分数大小关系是乙>甲>丙,叙述错误,不符合题意。
故选C。
24.D
【详解】A、没有指明温度,无法比较溶解度大小,故选项说法错误;
B、根据图示溶解度曲线图可知,NaCl的溶解度受温度影响的程度比KNO3小,故选项说法错误;
C、20℃时,KNO3的溶解度为31.6g,KNO3饱和溶液的溶质质量分数为≈24.01%,故选项说法错误;
D、60℃时硝酸钾的溶解度为110g,则此温度下210g KNO3饱和溶液中含有110g KNO3与100g水,40℃时,KNO3的溶解度为63.9g,则将60℃时210g KNO3饱和溶液降温至40℃,析出KNO3晶体的质量为110g-63.9g =46.1g,故选项说法正确。
故选D。
25.D
【详解】A、t2℃时甲、乙两物质的溶解度交于一点,故该温度下它们的溶解度相等,故正确,不符合题意;
B、温度大于t2℃时,由三种物质的位置关系可以看出,甲、乙、丙三种固体物质溶解度大小关系是甲>乙>丙,故正确,不符合题意;
C、甲的溶解度受温度的影响变化较大,乙的溶解度随温度的变化影响小,故可用冷却热饱和溶液的方法得到较纯净的甲,故正确,不符合题意;
D、丙的溶解度随着温度的降低而增大,故其它条件不变,升高温度可使丙的饱和溶液仍为饱和溶液,故错误,符合题意。
故选D。
相关试卷
这是一份中考化学一轮复习专项巩固练习 溶解度曲线问题汇总(六)(含答案解析),共26页。
这是一份中考化学一轮复习专项巩固练习 溶解度曲线问题汇总(一)(含答案解析),共27页。
这是一份中考化学一轮复习专项巩固练习 溶解度曲线问题汇总(五)(含答案解析),共25页。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)
.png)



