所属成套资源:2026年新高考化学小题训练
2026年新高考化学小题训练考点19化学平衡图象(原卷版+解析)
展开 这是一份2026年新高考化学小题训练考点19化学平衡图象(原卷版+解析),共27页。试卷主要包含了一定条件下热解制取H2等内容,欢迎下载使用。
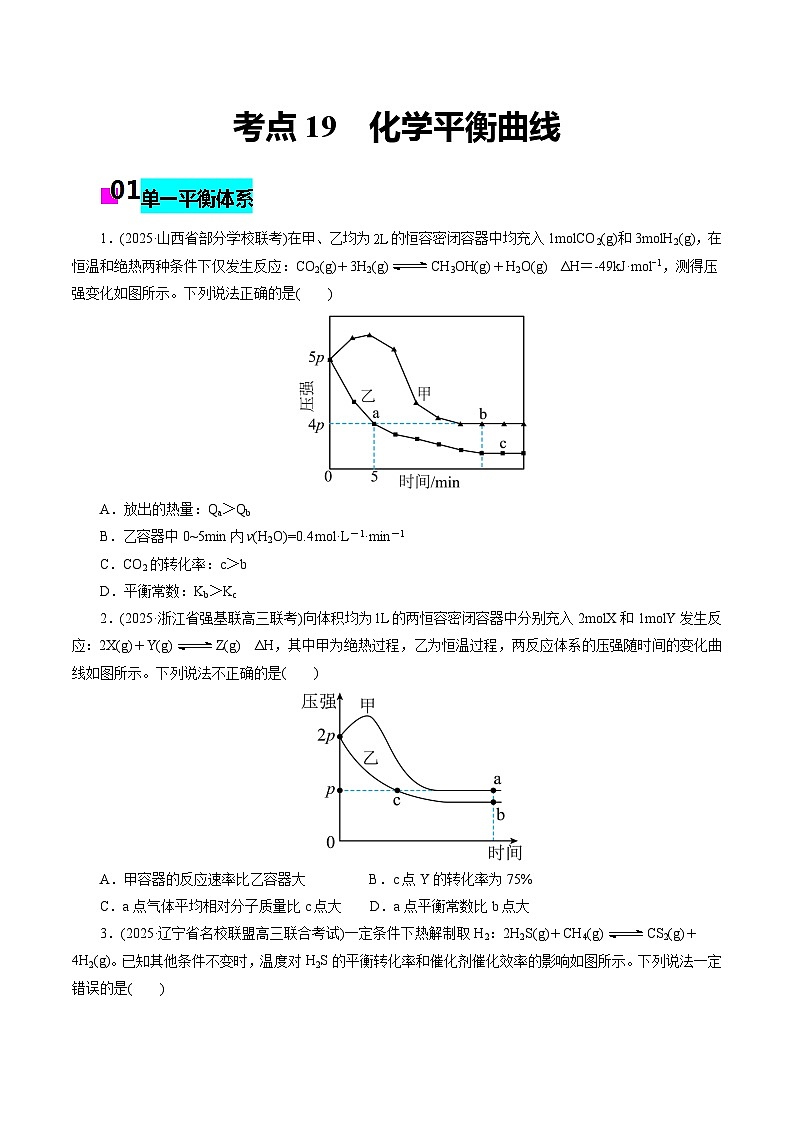
1.(2025·山西省部分学校联考)在甲、乙均为的恒容密闭容器中均充入1mlCO2(g)和3mlH2(g),在恒温和绝热两种条件下仅发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH=-49kJ·ml−1,测得压强变化如图所示。下列说法正确的是( )
A.放出的热量:Qa>Qb
B.乙容器中0~5min内v(H2O)=0.4 ml·L-1·min-1
C.CO2的转化率:c>b
D.平衡常数:Kb>Kc
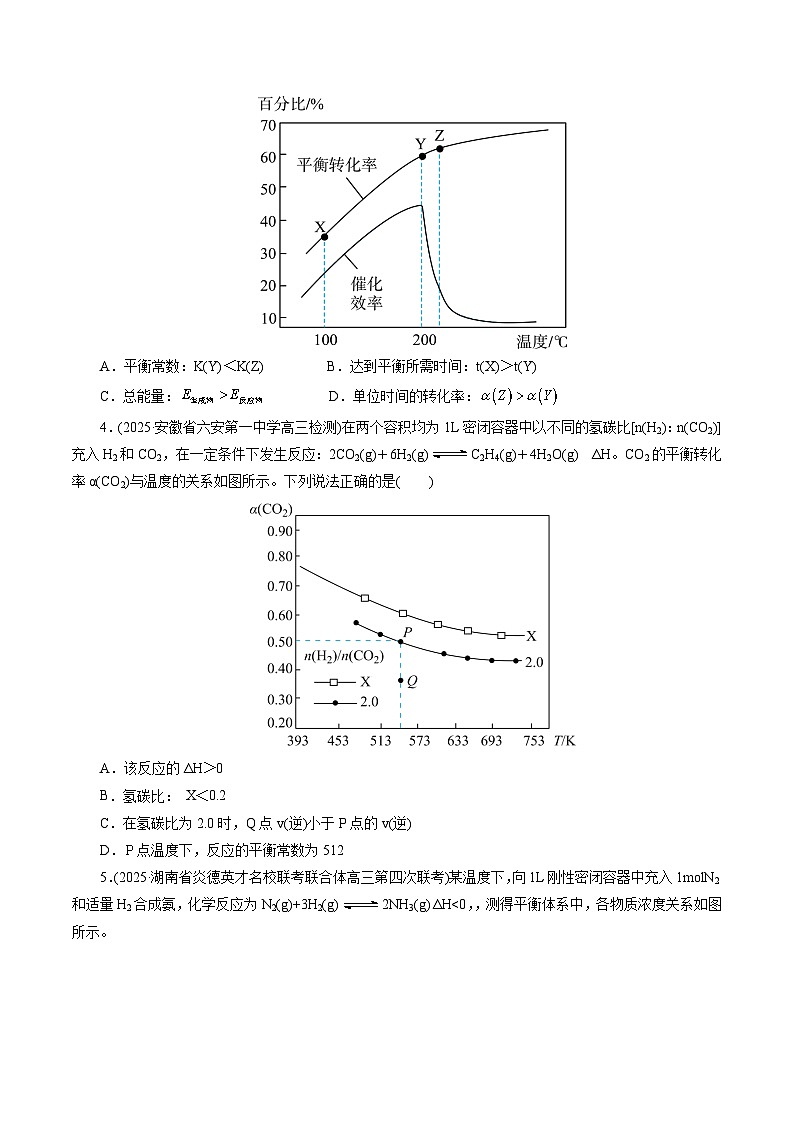
2.(2025·浙江省强基联高三联考)向体积均为的两恒容密闭容器中分别充入2mlX和1mlY发生反应:2X(g)+Y(g)Z(g) ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法不正确的是( )
A.甲容器的反应速率比乙容器大 B.c点Y的转化率为75%
C.a点气体平均相对分子质量比c点大 D.a点平衡常数比b点大
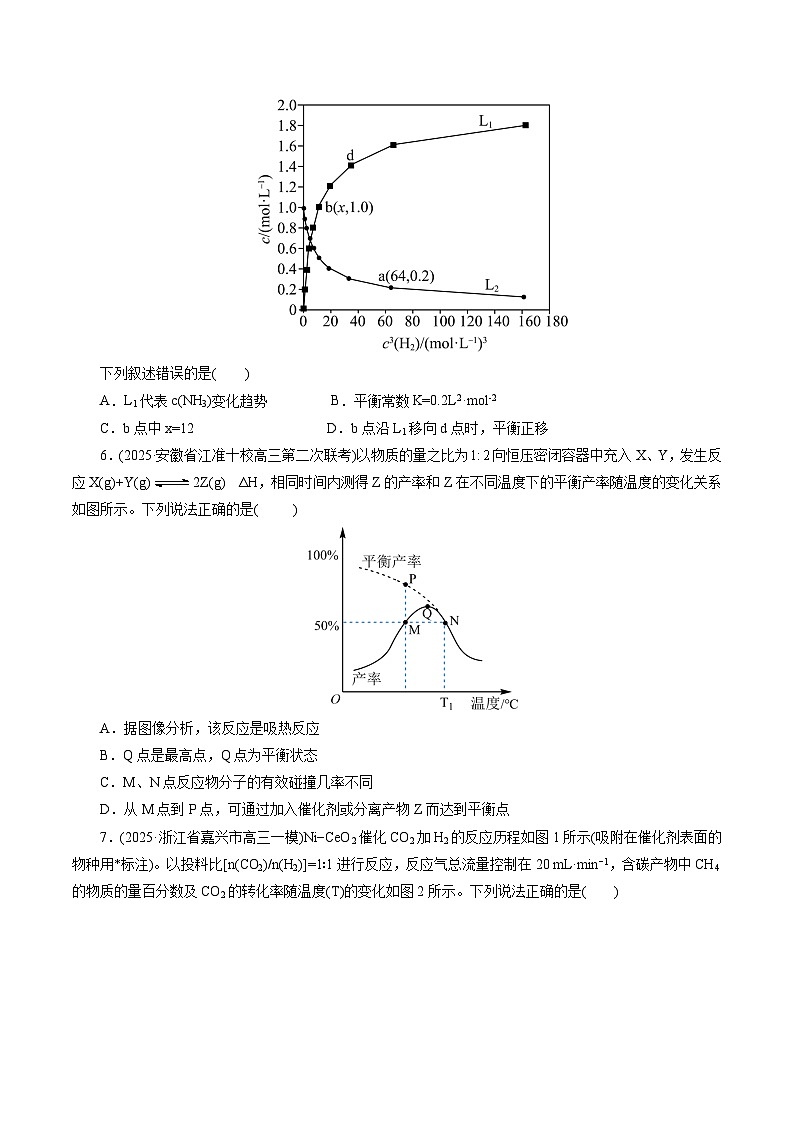
3.(2025·辽宁省名校联盟高三联合考试)一定条件下热解制取H2:2H2S(g)+CH4(g)CS2(g)+4H2(g)。已知其他条件不变时,温度对H2S的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定错误的是( )
A.平衡常数:K(Y)<K(Z) B.达到平衡所需时间:t(X)>t(Y)
C.总能量: D.单位时间的转化率:
4.(2025·安徽省六安第一中学高三检测)在两个容积均为1L密闭容器中以不同的氢碳比[n(H2):n(CO2)]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)C2H4(g)+4H2O(g) ΔH。CO2的平衡转化率α(CO2)与温度的关系如图所示。下列说法正确的是( )
A.该反应的ΔH>0
B.氢碳比: X<0.2
C.在氢碳比为2.0时,Q点v(逆)小于P点的v(逆)
D.点温度下,反应的平衡常数为512
5.(2025·湖南省炎德英才名校联考联合体高三第四次联考)某温度下,向1L刚性密闭容器中充入1mlN2和适量H2合成氨,化学反应为N2(g)+3H2(g)2NH3(g) ΔH逆反应活化能
B.点对应条件下,甲醛速率:v正>v逆
C.高于600℃,催化剂对副反应的选择性可能提高
D.700℃,H2的平衡浓度为0.4ml/L (甲醛选择性值近似取1/3)
11.(2025·山西省高三质量检测)氢气是一种清洁能源,乙醇—水催化重整可获得H2。主要反应有:
I.C2H5OH(g)+3H2O(g)2CO2(g)+6H2(g) ΔH>0
Ⅱ.CO2(g)+H2O(g)CO(g)+H2O(g) ΔH>0
一定条件下,向恒容密闭容器中充入2mlC2H5OH(g)和6ml H2O(g),C2H5OH和H2O的平衡转化率随温度的变化如图所示。下列说法错误的是( )
A.L1表示C2H5OH的平衡转化率
B.点对应反应I的平衡常数:
C.一定温度下选用高效催化剂,能提高平衡时H2的产率
D.500℃时,反应Ⅱ的平衡常数
12.(2025·安徽省六安第一中高三检测)在两个容积均为1L密闭容器中以不同的氢碳比[]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)C2H4(g)+4H2O(g) ΔH。CO2的平衡转化率与温度的关系如图所示。下列说法正确的是( )
A.该反应的ΔH>0
B.氢碳比:X<2.0
C.在氢碳比为2.0时,Q点v(逆)小于P点的v(逆)
D.点温度下,反应的平衡常数为512
13.(2025·江苏省丹阳高级中学高三期中)基于单簇催化剂(SCC)的NO还原反应(NORR)的主要反应如下:
(Ⅰ)2NO(g)+2H2(g)N2(g)+2H2O(g) ΔH1
(Ⅱ)2NO(g)+5H2(g)2NH3(g)+2H2O(g) ΔH2
(Ⅲ) N2(g)+3H2(g)2NH3(g) ΔH3
在T℃、100kPa反应条件下,向密闭容器中充入2mlNO和6mlH2,发生上述反应,测得含氮元素占比[如N2的含氮元素占比]与时间的关系如图所示。
已知:反应Ⅱ为快速平衡,可认为不受慢反应Ⅰ、Ⅲ的影响;K为用物质的量分数表示的平衡常数。下列有关说法正确的是( )
A.反应Ⅱ的ΔH2>0
B.曲线c表示的是氨气的含氮元素占比
C.若选择对反应Ⅱ催化效果更好的催化剂,则F点将平移至E点
D.若95min时达到平衡,则反应Ⅲ的平衡常数K的计算式为
14.(2025·江苏省南通市海门中学高三第二次调研)在催化剂作用下,以CO2催化加氢其主要反应有:
反应1:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH1
反应2:CO2(g)+H2(g)CO(g)+H2O(g) ΔH2
在恒温恒压密闭容器中通入3mlH2、1mlCO2气体,CO2的平衡转化率及CH3OH的平衡产率随温度变化的关系如图所示。
已知CH3OH的产率,下列说法正确的是( )
A.ΔH1<0,ΔH2<0
B.从350~600K,H2O的物质的量随温度升高先升后降
C.350~400K之间,n(H2)与n(CO2)的比值一直保持3:1
D.550K~600K之间,当容器的体积不变时,说明反应到达平衡
15.(2025·安徽省A10联盟高三质检)中南民族大学课题组在合成气直接制低碳烯烃方面取得了丰硕的成果。其主要反应如下:
反应Ⅰ:2CO(g)+4H2(g)C2H4(g)+2H2O(g) ΔH1= -332.0kJ·ml−1
反应Ⅱ:CO(g)+H2O(g)CO2(g)+H2(g) ΔH2=-42kJ·ml−1
在2L的密闭容器中充入6mlCO和6mlH2发生上述反应,平衡时CO、H2和C2H4的物质的量随温度的变化如下图所示:
已知从起始到温度为T1℃时反应经过的时间为10s,下列有关说法正确的是( )
A.P曲线表示CO的物质的量随温度的变化
B.T1℃时,反应Ⅱ的平衡常数为
C.由图像知,为提高乙烯的选择性,温度应控制在T2℃以上
D.在恒温恒压条件下,提高H2和CO的物质的量,一定能提高乙烯的产量
16.(2025·重庆市西南大学附属中学校高三阶段性监测)碘甲烷(CH3I)在一定条件下可裂解制取低碳烯烃,发生如下反应:
反应1:2CH3I(g)C2H4(g)+2HI(g) ΔH=+80.2kJ·ml−1
反应2:3C2H4(g)2C3H6(g) ΔH=-108.1kJ·ml−1
反应3:2C2H4(g)C4H8(g) ΔH=-120.6kJ·ml−1
向密闭容器中充入一定量的碘甲烷,维持容器内P0=0.1MPa,平衡时C2H4、C3H6和C4H8的物质的量分数与温度的关系如图所示。下列说法错误的是( )
A.图中物质表示的是C2H4
B.T1K时,碘甲烷的平衡转化率为
C.T1K时,容器中
D.随着温度升高,反应2的选择性先增大后减小
17.(2025·浙江省湖州、衢州、丽水高三三地市一模)利用CO2和H2可制得甲烷,实现资源综合利用。已知:
I.CO2(g)+H2(g)CO(g)+H2O(g) ΔH1=+41.2kJ·ml−1
Ⅱ.CO2(g)+4H2(g)CH4(g)+2H2O(g) ΔH2=-165.0kJ·ml−1
在一定的温度和压强下,将按一定比例混合的CO2和H2混合气体通过装有催化剂的反应器,反应相同时间,CO2转化率和CH4选择性随温度变化关系如图所示。
,下列说法不正确的是( )
A.反应I的
B.240℃时,其他条件不变,增大压强,CO2的转化率增大
C.在260~300℃间,其他条件不变,升高温度,CH4的产率增大
D.320℃时CO2的转化率最大,可能的原因是反应I和反应IⅡ达到了平衡状态
18.(2025·河北省沧州市高三调研)脱除汽车尾气中的NO和CO包括以下两个反应:
I. 2NO(g)+CO(g)CO2(g)+N2O(g) ΔH1=-381.2kJ·ml−1
Ⅱ.N2O(g)+CO(g)CO2(g)+N2(g) ΔH2=-364.5kJ·ml−1
将恒定组成的NO和CO混合气通入不同温度的反应器,相同时间内检测物质浓度,结果如图所示。
下列说法正确的是( )
A.使用合适的催化剂,能提高NO的平衡转化率
B.其他条件不变,增大体系的压强,NO的平衡转化率减小
C.350~420℃范围内,温度升高,反应I速率增大的幅度大于反应Ⅱ速率增大的幅度
D.450℃时,该时间段内NO的脱除率约为
考点19 化学平衡曲线
单一平衡体系
1.(2025·山西省部分学校联考)在甲、乙均为的恒容密闭容器中均充入1mlCO2(g)和3mlH2(g),在恒温和绝热两种条件下仅发生反应:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH=-49kJ·ml−1,测得压强变化如图所示。下列说法正确的是( )
A.放出的热量:Qa>Qb
B.乙容器中0~5min内v(H2O)=0.4 ml·L-1·min-1
C.CO2的转化率:c>b
D.平衡常数:Kb>Kc
【答案】C
【解析】A项,该反应为放热反应,甲容器内压强先增大,则甲容器一定是绝热容器,乙容器为恒温容器;a、b两点对应压强相同,b点对应的温度高,则b点气体的总物质的量少,反应物转化率高,放热多,A错误;B项,利用三段法可表示出乙容器反应5min时各组分的物质的量,设生成n(H2O)为x,则:
乙容器反应到5min时,压强为4p,此时,解得,所以乙容器中0~5min内,B错误;C项,b、c两点均达到平衡状态,甲为绝热容器,容器内温度高,反应物的转化率低,C正确;D项,甲容器的温度高,该反应是放热反应,升高温度则平衡逆向移动,平衡常数减小,D错误;故选C。
2.(2025·浙江省强基联高三联考)向体积均为的两恒容密闭容器中分别充入2mlX和1mlY发生反应:2X(g)+Y(g)Z(g) ΔH,其中甲为绝热过程,乙为恒温过程,两反应体系的压强随时间的变化曲线如图所示。下列说法不正确的是( )
A.甲容器的反应速率比乙容器大 B.c点Y的转化率为75%
C.a点气体平均相对分子质量比c点大 D.a点平衡常数比b点大
【答案】D
【解析】甲容器在绝热条件下,随着反应的进行,压强先增大后减小,刚开始压强增大的原因是因为容器温度升高,则说明上述反应过程放热,即ΔH<0。A项,甲容器温度高于乙容器,而起始浓度相同,故甲容器的反应速率比乙容器大,A正确;B项,乙容器恒温恒容,c点的总压为p,气体的压强之比等于气体的物质的量(物质的量浓度)之比,所以可设Y转化的物质的量浓度为,则列出三段式如下:
则有,计算得到x=0.75,Y的转化率为75%,B正确;C项,图中a点和c点的压强相等,而a点温度高于c点,若两者气体物质的量相等,则甲容器压强大于乙容器压强,则说明甲容器中气体的总物质的量此时相比乙容器在减小即气体总物质的量:,气体质量相等,故a点气体平均摩尔质量比c点大,即a点气体平均相对分子质量比c点大,C正确; D项,ΔH<0,甲容器温度高于乙容器,故a点相当于b点升高温度,平衡逆向移动平衡常数减小,D错误;故选D。
3.(2025·辽宁省名校联盟高三联合考试)一定条件下热解制取H2:2H2S(g)+CH4(g)CS2(g)+4H2(g)。已知其他条件不变时,温度对H2S的平衡转化率和催化剂催化效率的影响如图所示。下列说法一定错误的是( )
A.平衡常数:K(Y)<K(Z) B.达到平衡所需时间:t(X)>t(Y)
C.总能量: D.单位时间的转化率:
【答案】D
【解析】由图可知,升高温度,H2S的平衡转化率增大,说明反应2H2S(g)+CH4(g)CS2(g)+4H2(g)吸热,总能量:。A项,温度越高,平衡常数越大,温度:Z>Y,平衡常数:K(Y)<K(Z),A正确;B项,200℃之前温度越高,催化效率越强,反应速率越快,则Y点的反应速率大于X点的反应速率,则达到平衡所需时间可能为t(X)>t(Y),B正确;C项,正反应吸热,总能量:,C正确;D项,Z点和Y点温度差别不大,但Z点的催化效率远低于Y点,说明Y的反应速率大于Z点的反应速率,则单位时间H2S的转化率:,D错误;故选D。
4.(2025·安徽省六安第一中学高三检测)在两个容积均为1L密闭容器中以不同的氢碳比[n(H2):n(CO2)]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)C2H4(g)+4H2O(g) ΔH。CO2的平衡转化率α(CO2)与温度的关系如图所示。下列说法正确的是( )
A.该反应的ΔH>0
B.氢碳比: X<0.2
C.在氢碳比为2.0时,Q点v(逆)小于P点的v(逆)
D.点温度下,反应的平衡常数为512
【答案】C
【解析】A项,由图可知,随温度升高CO2的平衡转化率减小,说明升高温度平衡逆向移动,升高温度平衡向吸热反应方向移动,则正反应为放热反应,故ΔH<0,A错误;B项,氢碳比越大,二氧化碳的转化率越大,故氢碳比:X>2.0,B错误;C项,相同温度下,Q点二氧化碳转化率小于平衡时的转化率,说明Q点未到达平衡,反应向正反应方向进行,逆反应速率增大到平衡状态P,故在氢碳比为2.0时,Q点v(逆)小于P点的v(逆),C正确;D项,由图可知,P点平衡时二氧化碳转化率为0.5,氢碳比,设起始时氢气为2a ml·L-1、二氧化碳为aml·L-1,则二氧化碳浓度变化量为0.5a ml·L-1,则:
平衡常数,D错误。故选C。
5.(2025·湖南省炎德英才名校联考联合体高三第四次联考)某温度下,向1L刚性密闭容器中充入1mlN2和适量H2合成氨,化学反应为N2(g)+3H2(g)2NH3(g) ΔH逆反应活化能
B.点对应条件下,甲醛速率:v正>v逆
C.高于600℃,催化剂对副反应的选择性可能提高
D.700℃,H2的平衡浓度为0.4ml/L (甲醛选择性值近似取1/3)
【答案】D
【解析】A项,主反应为吸热反应,吸热反应正反应的活化能较大,A项正确;B项,根据题意可知,温度为700°C时,反应恰好达到首次平衡,则X 点还未达到平衡,因此甲醛的正反应速率较大,B项正确;C项,温度高于600°C,甲醛的选择性降低,故推测高于600°C,催化剂对副反应 的选择性可能提高,C 项正确;D项,根据题中数据可知,主反应消耗的甲醇为0.5ml/L×60%0.1ml/L, 副反应消耗的甲醇为0.5ml/L×60%-0.1ml/L=0.2ml/L,据此列出各物质浓度的变化量如下:
,平衡时,c(H2)=0.1ml/L+0.4ml/L=0.5ml/L,D项错误;故选D。
11.(2025·山西省高三质量检测)氢气是一种清洁能源,乙醇—水催化重整可获得H2。主要反应有:
I.C2H5OH(g)+3H2O(g)2CO2(g)+6H2(g) ΔH>0
Ⅱ.CO2(g)+H2O(g)CO(g)+H2O(g) ΔH>0
一定条件下,向恒容密闭容器中充入2mlC2H5OH(g)和6ml H2O(g),C2H5OH和H2O的平衡转化率随温度的变化如图所示。下列说法错误的是( )
A.L1表示C2H5OH的平衡转化率
B.点对应反应I的平衡常数:
C.一定温度下选用高效催化剂,能提高平衡时H2的产率
D.500℃时,反应Ⅱ的平衡常数
【答案】C
【解析】A项,反应I、Ⅱ均为吸热反应,随着温度升高,反应I平衡正向移动,C2H5OH的转化率始终增大;随着温度升高,反应Ⅱ平衡也正向移动,不断生成水,使水的转化率降低,故L1代表C2H5OH的平衡转化率,L2代表H2O的平衡转化率,A正确;B项,对于吸热反应来说,温度越高,平衡常数越大,故a、b点对应反应I的平衡常数:,B正确;C项,催化剂不能使平衡移动,选用高效催化剂,不能提高平衡时H2的产率,C错误;D项,由图可知,500℃时,C2H5OH的平衡转化率为95%,水的平衡转化率为70%,列出转化关系式:
,,解得。平衡时,H2、CO2、CO、H2O的物质的量分别为9.9ml、2.3ml、1.5ml、1.8ml。500℃时,对于反应前后气体分子数不变的反应Ⅱ来说,平衡常数,D正确;故选C。
12.(2025·安徽省六安第一中高三检测)在两个容积均为1L密闭容器中以不同的氢碳比[]充入H2和CO2,在一定条件下发生反应:2CO2(g)+6H2(g)C2H4(g)+4H2O(g) ΔH。CO2的平衡转化率与温度的关系如图所示。下列说法正确的是( )
A.该反应的ΔH>0
B.氢碳比:X<2.0
C.在氢碳比为2.0时,Q点v(逆)小于P点的v(逆)
D.点温度下,反应的平衡常数为512
【答案】C
【解析】A项,由图可知,随温度升高CO2的平衡转化率减小,说明升高温度平衡逆向移动,升高温度平衡向吸热反应方向移动,则正反应为放热反应,故ΔH<0,A错误;B项,氢碳比越大,二氧化碳的转化率越大,故氢碳比:X>2.0,B错误;C项,相同温度下,Q点二氧化碳转化率小于平衡时的转化率,说明Q点未到达平衡,反应向正反应方向进行,逆反应速率增大到平衡状态P,故在氢碳比为2.0时,Q点v(逆)小于P点的v(逆),C正确;D项,由图可知,P点平衡时二氧化碳转化率为0.5,氢碳比,设起始时氢气为、二氧化碳为,则二氧化碳浓度变化量为,则:
平衡常数,D错误。故选C。
13.(2025·江苏省丹阳高级中学高三期中)基于单簇催化剂(SCC)的NO还原反应(NORR)的主要反应如下:
(Ⅰ)2NO(g)+2H2(g)N2(g)+2H2O(g) ΔH1
(Ⅱ)2NO(g)+5H2(g)2NH3(g)+2H2O(g) ΔH2
(Ⅲ) N2(g)+3H2(g)2NH3(g) ΔH3
在T℃、100kPa反应条件下,向密闭容器中充入2mlNO和6mlH2,发生上述反应,测得含氮元素占比[如N2的含氮元素占比]与时间的关系如图所示。
已知:反应Ⅱ为快速平衡,可认为不受慢反应Ⅰ、Ⅲ的影响;K为用物质的量分数表示的平衡常数。下列有关说法正确的是( )
A.反应Ⅱ的ΔH2>0
B.曲线c表示的是氨气的含氮元素占比
C.若选择对反应Ⅱ催化效果更好的催化剂,则F点将平移至E点
D.若95min时达到平衡,则反应Ⅲ的平衡常数K的计算式为
【答案】D
【解析】A项,反应Ⅱ是气体量减少的反应,ΔS<0,反应快速自发进行ΔG=ΔH2-TΔS<0,故该反应的ΔH2<0,A错误;B项,起始的含氮物质只有一氧化氮,反应ii为快反应,曲线a表示物质快速减少,故曲线a表示NO,NH3快速增加,故曲线b表示氨气,曲线表示c氮气,B错误;C项,若选择对反应Ⅱ催化效果更好的催化剂,反应Ⅱ会更快,生成NH3达到最高点所用时间短,NH3的占比更大,因此F点可能移向E点上方的某个点,C错误;D项,起始时,2 ml NO、6 ml H2,若95 min时达到平衡,则由图知,NO的含氮元素占比为6%,n(NO)=2ml×6%=0.12ml,N2的含氮元素占比为86%,n(N2)=,NH3的含氮元素占比为100%-6%-86%=8%,n(NH3)=2ml×8%=0.16ml,由氧原子守恒得,n(H2O)=2ml-0.12ml=1.88ml,由氢原子守恒得,n(H2)=,此时总物质的量为(0.12+0.86+0.16+1.88+3.88)=6.9ml,N2的物质的量分数为,H2的物质的量分数为:,NH3的物质的量分数为:,则反应Ⅲ的平衡常数Kx=,D正确;故选D。
14.(2025·江苏省南通市海门中学高三第二次调研)在催化剂作用下,以CO2催化加氢其主要反应有:
反应1:CO2(g)+3H2(g)CH3OH(g)+H2O(g) ΔH1
反应2:CO2(g)+H2(g)CO(g)+H2O(g) ΔH2
在恒温恒压密闭容器中通入3mlH2、1mlCO2气体,CO2的平衡转化率及CH3OH的平衡产率随温度变化的关系如图所示。
已知CH3OH的产率,下列说法正确的是( )
A.ΔH1<0,ΔH2<0
B.从350~600K,H2O的物质的量随温度升高先升后降
C.350~400K之间,n(H2)与n(CO2)的比值一直保持3:1
D.550K~600K之间,当容器的体积不变时,说明反应到达平衡
【答案】C
【解析】A项,由图可知,升高温度,甲醇的平衡产率下降,说明反应①平衡逆向移动,△H1 < 0,而500K左右过后再升高温度,二氧化碳的平衡转化率增大,说明升高温度,反应②占主导,升温平衡正向移动,△H2> 0,A错误;B项,由图可知,从350~600K,随着温度的升高,二氧化碳的转化率先降低,再升高,两个反应都会生成水,且n(CO2):n(H2O)=1:1,则H2O的物质的量随温度升高先降后升,B错误;C项,由图可知,350~400K之间时,甲醇的产率和二氧化碳的转化率相同,则此时只发生反应1,此时反应物的投料比等于系数比,则n(H2)与n(CO2)的比值一直保持3:1,C正确;D项,550K~600K之间时,二氧化碳的转化率在增大,而甲醇的产率几乎为0,则此时发生的反应主要是反应2,该反应是气体分子数不变的反应,则当容器的体积不变时,不能说明反应到达平衡,D错误;故选C。
15.(2025·安徽省A10联盟高三质检)中南民族大学课题组在合成气直接制低碳烯烃方面取得了丰硕的成果。其主要反应如下:
反应Ⅰ:2CO(g)+4H2(g)C2H4(g)+2H2O(g) ΔH1= -332.0kJ·ml−1
反应Ⅱ:CO(g)+H2O(g)CO2(g)+H2(g) ΔH2=-42kJ·ml−1
在2L的密闭容器中充入6mlCO和6mlH2发生上述反应,平衡时CO、H2和C2H4的物质的量随温度的变化如下图所示:
已知从起始到温度为T1℃时反应经过的时间为10s,下列有关说法正确的是( )
A.P曲线表示CO的物质的量随温度的变化
B.T1℃时,反应Ⅱ的平衡常数为
C.由图像知,为提高乙烯的选择性,温度应控制在T2℃以上
D.在恒温恒压条件下,提高H2和CO的物质的量,一定能提高乙烯的产量
【答案】B
【解析】两反应均为放热反应,升高温度两平衡均向逆反应方向移动,CO的物质的量增多,故曲线M表示CO的物质的量,反应I向逆反应方向移动,故C2H4的物质的量减小,故曲线Q表示C2H4的物质的量,则曲线P表示H2的物质的量。A项,曲线P表示H2的物质的量,A错误;B项,由图知,温度T1℃时,,,所以反应Ⅰ消耗的CO为2ml,生成的H2O为2ml,则反应Ⅱ消耗的CO为0.5ml,消耗水0.5ml,则,。经计算可得反应II的平衡常数为=,B正确;C项,由图像知,H2的物质的量先增大后减小,由方程式知升高温度,两平衡向逆反应方向移动,反应I逆向移动H2的物质的量增大,反应II逆向移动,H2的物质的量减小,H2的物质的量先增大,故说明温度小于T2℃以反应I为主,故为提高乙烯的选择性,温度应控制在T2℃以下,C错误;D项,在恒温恒压条件下,如果同等程度提高H2和CO的物质的量,容器的体积也相应扩大,不一定有利于提高乙烯的产量,D错误;故选B。
16.(2025·重庆市西南大学附属中学校高三阶段性监测)碘甲烷(CH3I)在一定条件下可裂解制取低碳烯烃,发生如下反应:
反应1:2CH3I(g)C2H4(g)+2HI(g) ΔH=+80.2kJ·ml−1
反应2:3C2H4(g)2C3H6(g) ΔH=-108.1kJ·ml−1
反应3:2C2H4(g)C4H8(g) ΔH=-120.6kJ·ml−1
向密闭容器中充入一定量的碘甲烷,维持容器内P0=0.1MPa,平衡时C2H4、C3H6和C4H8的物质的量分数与温度的关系如图所示。下列说法错误的是( )
A.图中物质表示的是C2H4
B.T1K时,碘甲烷的平衡转化率为
C.T1K时,容器中
D.随着温度升高,反应2的选择性先增大后减小
【答案】B
【解析】A项,反应1吸热,反应2放热,升温反应1正向移动,反应2逆向移动,故随温度升高φ(C2H4)增加,物质Y表示的是C2H4,物质X表示的是C3H6,A正确;B项,由图可知,T1K,平衡时n(C2H4)= 4%n总,n(C3H6)=n(C4H8)= 8%n总,故反应2,3消耗n(C2H4)耗=8%×n总+8%×2n总= 28%n总,故容器中n(HI)= 2×(4%n总+28%n总)= 64%n总,n(CH3I)剩余=(1-4%-8%×2-64%)n总=16% n总,因为n(CH3I)消耗=n(HI)=64%n总,所以CH3I转化率为,B错误;C项,由图可知,T1K时,,由选项B分析知,,则, C正确;D项,由图可知,随着温度升高,φ(C3H6)先增大后减小,故可说明反应2的选择性先增大后减小,D正确;故选B。
17.(2025·浙江省湖州、衢州、丽水高三三地市一模)利用CO2和H2可制得甲烷,实现资源综合利用。已知:
I.CO2(g)+H2(g)CO(g)+H2O(g) ΔH1=+41.2kJ·ml−1
Ⅱ.CO2(g)+4H2(g)CH4(g)+2H2O(g) ΔH2=-165.0kJ·ml−1
在一定的温度和压强下,将按一定比例混合的CO2和H2混合气体通过装有催化剂的反应器,反应相同时间,CO2转化率和CH4选择性随温度变化关系如图所示。
,下列说法不正确的是( )
A.反应I的
B.240℃时,其他条件不变,增大压强,CO2的转化率增大
C.在260~300℃间,其他条件不变,升高温度,CH4的产率增大
D.320℃时CO2的转化率最大,可能的原因是反应I和反应IⅡ达到了平衡状态
【答案】A
【解析】A项,反应I为等体积的吸热反应ΔH1>0,当ΔG=ΔH-TΔS<0时反应可自发进行,故该反应ΔS>0,A项错误;B项,240℃时,其他条件不变,增大压强,反应I平衡不移动,反应Ⅱ平衡正向移动,CO2的转化率增大,B项正确;C项,在260~300℃间,其他条件不变,升高温度,CH4选择性变化不大,CO2的转化率逐渐增大,说明反应Ⅱ平衡正向移动,CH4的产率增大,C项正确;D项,320℃时CO2的转化率最大,随后转化率降低,可能的原因是温度过高,导致催化剂失去活性,也可能是反应达到了平衡状态,D项正确;故选A。
18.(2025·河北省沧州市高三调研)脱除汽车尾气中的NO和CO包括以下两个反应:
I. 2NO(g)+CO(g)CO2(g)+N2O(g) ΔH1=-381.2kJ·ml−1
Ⅱ.N2O(g)+CO(g)CO2(g)+N2(g) ΔH2=-364.5kJ·ml−1
将恒定组成的NO和CO混合气通入不同温度的反应器,相同时间内检测物质浓度,结果如图所示。
下列说法正确的是( )
A.使用合适的催化剂,能提高NO的平衡转化率
B.其他条件不变,增大体系的压强,NO的平衡转化率减小
C.350~420℃范围内,温度升高,反应I速率增大的幅度大于反应Ⅱ速率增大的幅度
D.450℃时,该时间段内NO的脱除率约为
【答案】D
【解析】A项,催化剂不能改变化学反应限度,因此使用催化剂不能提高NO的平衡转化率,A错误;B项,反应I的反应前后气体体积减小,反应Ⅱ的反应前后气体体积不变,增大压强对反应Ⅱ的平衡无影响,使反应I的平衡正向移动,因此增大压强,NO的平衡转化率增大,B错误;C项,从图中可知,350~420℃范围内升高温度,CO2和N2的浓度增大,而N2O的浓度减小,说明此时升高温度,以反应Ⅱ为主,则反应I速率增大的幅度小于反应Ⅱ速率增大的幅度,C错误;D项,450℃时,NO的初始浓度是,转化为N2的NO浓度为,故该时间段内NO的脱除率为,D正确;故选D。
相关试卷
这是一份2026年新高考化学小题训练考点19化学平衡图象(原卷版+解析),共27页。试卷主要包含了一定条件下热解制取H2等内容,欢迎下载使用。
这是一份2026年新高考化学小题训练考点18化学平衡常数(原卷版+解析),共16页。试卷主要包含了甲醇重整制氢涉及三个反应等内容,欢迎下载使用。
这是一份2026年新高考化学小题训练考点17化学平衡及影响因素(原卷版+解析),共17页。试卷主要包含了YbN有很好的加氢催化性能等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)

.png)


