





第一单元 含硫化合物的性质 第2课时(教学课件)-2025-2026学年高中化学必修第一册(苏教版2019)
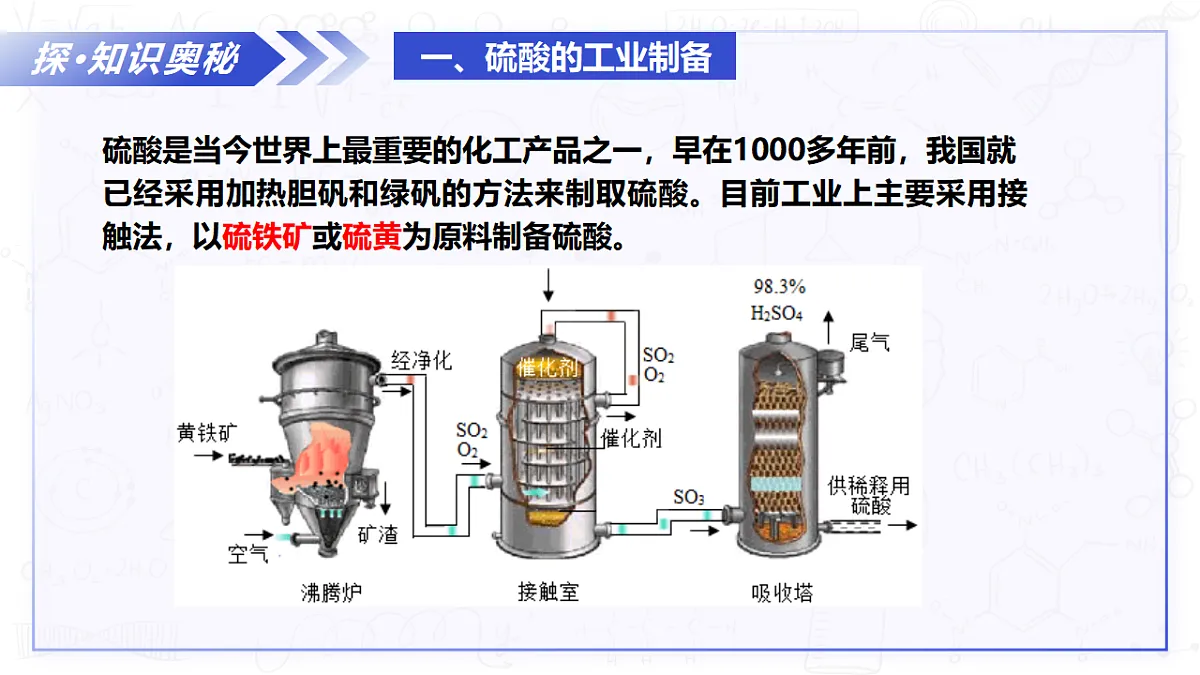
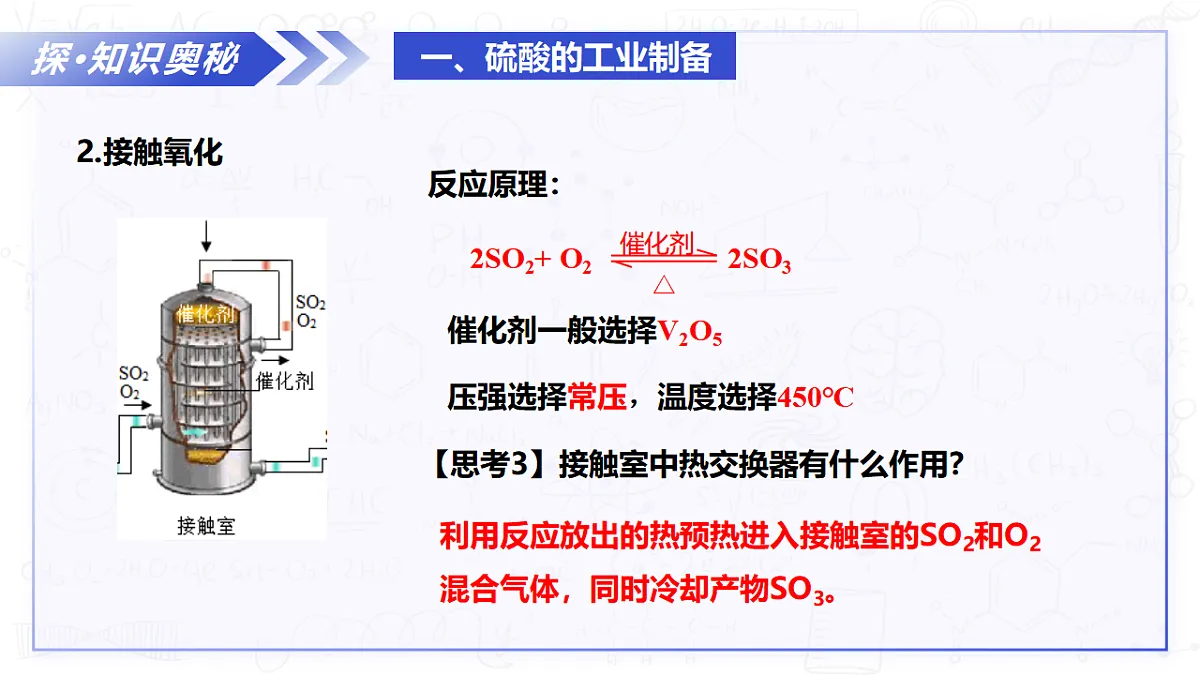
展开专题4 硫与环境保护第一单元 含硫化合物的性质第2课时 硫酸的工业制备浓硫酸的性质苏教版2019必修第一册知识导航明·学习目标 1.了解硫酸工业制备的装置和原理;2.通过实验探究浓硫酸的性质,提升观察、分析实验现象及归纳总结的能力。引·新课导入生产电池、肥料、塑料都会用到一个化工明星,那就是硫酸。硫酸是现代工业的“血液”,是产量最大、用途最广的化工基础原料之一。那么工业上是如何制备硫酸呢?01硫酸的工业制备探·知识奥秘硫酸是当今世界上最重要的化工产品之一,早在1000多年前,我国就已经采用加热胆矾和绿矾的方法来制取硫酸。目前工业上主要采用接触法,以硫铁矿或硫黄为原料制备硫酸。探·知识奥秘1.产气(生成SO2)反应原理:【思考1】将矿石粉碎有何作用?增大接触面积,加快反应速率【思考2】出来的气体为什么会净化?除去杂质和矿尘的目的是防止催化剂中毒探·知识奥秘2.接触氧化反应原理:催化剂一般选择V2O5压强选择常压,温度选择450℃【思考3】接触室中热交换器有什么作用?利用反应放出的热预热进入接触室的SO2和O2混合气体,同时冷却产物SO3。探·知识奥秘3. SO3的吸收SO3 +H2O===H2SO4 反应原理:【思考4】为什么不用水或稀硫酸吸收SO3?SO3与水化合时,放出大量热,会形成大量酸雾,降低吸收效率。【思考5】为什么浓硫酸要从上向下喷洒?使SO3被浓H2SO4充分吸收。探·知识奥秘【思考与讨论】以硫铁矿或硫黄为原料都可以制备硫酸,如果你是化工厂的厂长,应该如何选择呢?硫铁矿中FeS2的质量分数一般为20%~50%,杂质较多,制酸工艺过程中所产生的矿渣和废气使生产装置变得较为复杂。因此,硫铁矿制酸投资几乎是同等规模硫黄制酸设备的两倍。采用硫黄制酸法,工艺流程和设备相对简易。硫黄含杂质少,燃烧生成的气体含杂质少,可免去气体净化的过程,制备过程也不产生矿渣,但硫黄原料价格高于硫铁矿。具体选用何种硫酸制备工艺,应根据实际条件和要求进行决策。探·知识奥秘化学工业制备的要求(1)原料廉价且稳定,降低运输成本。(2)从环保、成本等角度选择合适的化学反应,保证在反应中能充分接触。(3)制备流程简单高效,能耗低,反应放出的热量尽可能加以循环利用,生成的副产物较少。(4)制备过程绿色环保,不使用或生成对环境有害的物质。1.在硫酸工业生产中,SO3的吸收过程是在吸收塔(如右图)中进行的,吸收塔里还装入了大量瓷环。下列有关说法不正确的是( )析·典型范例CA.从①处通入SO3,整个吸收操作采取逆流的形式B.从②处喷下98.3%的硫酸,瓷环的作用是增大接触面积C.从③处导出的气体只含有少量SO2,可直接排入大气D.从④处流出的是浓硫酸析·典型范例2.硫酸是重要化工原料,工业生产制取硫酸的原理示意图如图。下列说法不正确的是( )A.Ⅰ的化学方程式:3FeS2+8O2 Fe3O4+6SO2B.将Ⅱ中反应条件的温度升高至1000℃,更利于反应的进行C.将黄铁矿换成硫黄可以减少废渣的产生D.生产过程中产生的尾气可用碱液吸收B02浓硫酸的性质探·知识奥秘(1)物理性质无色、黏稠的油状液体高密度酸大于水高沸点(338℃ ),难挥发极易溶于水,溶解时放出大量的热色态:密度:沸点:溶解性:【思考】如何稀释浓硫酸?将浓硫酸沿烧杯内壁缓缓倒入水中,并用玻璃棒不断搅拌。探·知识奥秘(2)化学性质实验一:向试管中加入少量胆矾,再加入约3mL浓硫酸,观察实验现象。实验现象蓝色晶体颜色变浅实验结论胆矾部分失水探·知识奥秘(2)化学性质1. 吸水性浓硫酸能吸收存在于周围环境中的水分及固体中的结晶水。化学变化浓硫酸可干燥酸性气体(CO2、SO2、HCl等)和中性气体(N2、O2、H2等)浓硫酸不能干燥碱性气体(NH3)和某些还原性气体(H2S、HBr、HI)注意:浓硫酸可以干燥SO2、H2、CO等还原性气体。吸水性的应用:可作干燥剂探·知识奥秘(2)化学性质实验二:向烧杯中加入约四分之一体积的蔗糖,加入少量的蒸馏水,再向试管中加入15mL浓硫酸,搅拌,观察现象。实验现象蔗糖变黑,体积膨胀 呈疏松海绵状放出有刺激性气味的气体【思考】为什么会出现如此奇特的实验现象呢?探·知识奥秘(2)化学性质2. 脱水性【思考1】为什么蔗糖会变黑呢?浓硫酸能将有机物中的H、O个数比以2:1脱去生成水蔗糖脱水后变成了黑色的单质碳【思考2】刺激性气味的气体是什么呢?如果将该气体通入盛有品红溶液的试管中,发现品红溶液会褪色SO2浓硫酸和蔗糖反应:体现出浓硫酸的脱水性和强氧化性。探·知识奥秘(2)化学性质实验三:将一小片铜片放入试管中,然后加入2mL浓硫酸,加热,观察实验现象。实验现象铜丝表面变黑,产生气泡,有无色刺激性气体生成品红溶液褪色溶液变成灰黑色,停止加热后,将溶液倒入蒸馏水中,溶液变蓝。探·知识奥秘(2)化学性质3. 强氧化性 Cu + 2H2SO4 = CuSO4 + SO2 + 2H2O△0+6+6+4+22e-请用单线桥标出电子的转移情况n(氧化剂):n(还原剂)=1 :1该反应体现了浓硫酸的 性和 性强氧化酸有酸根保留,化合价未变注意:反应条件加热,浓硫酸变稀不反应。铜和浓硫酸反应原理:探·知识奥秘(2)化学性质3. 强氧化性 浓硫酸参与的反应,大多数是氧化还原反应,反应中浓硫酸作氧化剂。加热时,浓H2SO4能氧化大多数金属(除Au、Pt),一般不产生H2,产生SO2气体① 与金属反应浓H2SO4与金属反应,表现酸性和氧化性【思考】浓硫酸与活泼金属(如锌)反应时,会产生哪些气体?开始浓硫酸表现出强氧化性,生成二氧化硫气体;当浓硫酸变为稀硫酸时,则表现出酸性,生成的气体为氢气探·知识奥秘(2)化学性质3. 强氧化性浓硫酸能够与大多数金属反应,为什么工业运输浓硫酸使用的是铁罐车?常温下,浓硫酸可使铁或铝的表面生成一层致密的氧化膜,阻止内部金属与浓硫酸进一步反应,这种现象叫做——钝化。钝化是化学变化探·知识奥秘(2)化学性质3. 强氧化性② 与非金属反应浓H2SO4与非金属(碳、硫、磷等)反应,只表现氧化性,产生SO2气体。③与还原性化合物反应H2SO4 (浓)+H2S=SO2↑+S↓+2H2OH2SO4 (浓)+2HI=SO2↑+I2+2H2O这就是浓硫酸不能用来干燥H2S、HI气体的原因析·典型范例A.浓硫酸具有吸水性,因而能使蔗糖炭化B.浓硫酸在常温下可迅速与铜片反应放出二氧化硫气体C.浓硫酸是一种干燥剂,能够干燥氨气、氢气等气体D.浓硫酸在常温下能够使铁、铝等金属钝化3.下列关于浓硫酸的叙述,正确的是( )DA.分别取10 mL溶液,质量大的是浓H2SO4,质量小的是稀H2SO4B.观察液体流动性,流动性好的是稀H2SO4,油状黏稠的是浓H2SO4C.把CuSO4·5H2O晶体投入溶液,逐渐变为白色粉末的是浓H2SO4,晶体溶解的是稀H2SO4D.将Al片分别投入溶液,反应快速放出气体的是浓H2SO4,放出气体慢的是稀H2SO44.下列方法用来鉴别浓H2SO4和稀H2SO4,不正确的是( )析·典型范例D第一单元含硫化合物的性质第1课时硫酸的工业制备浓硫酸的性质硫酸的制备装置硫酸的制备原理吸水性脱水性理·核心要点硫酸工业制备的方案选择强氧化性A.硫铁矿燃烧前需要粉碎,这样易于向沸腾炉中投料B.炉气进入接触室之前需要净化、干燥,因为炉气中的杂质易与SO2反应C.SO2氧化为SO3时需要使用催化剂,这样可以使SO2全部转化为SO3D.SO3的吸收一般用98.3%的浓H2SO4,而不用水,因为用水吸收易形成酸雾,不利于SO3的吸收1.在硫酸的工业制法中,下列措施以及采取这些措施的原因分析都正确的是( )练·技能实战D2.蔗糖与浓硫酸发生作用的过程如图所示。下列关于该过程的分析不正确的是( )练·技能实战CA.过程①白色固体变黑,主要体现了浓硫酸的脱水性B.过程②固体体积膨胀,与产生的大量气体有关C.过程中产生能使品红溶液褪色的气体,体现了浓硫酸的酸性 D.过程中蔗糖分子发生了化学键的断裂D.过程中蔗糖分子发生了化学键的断裂3.利用如图几个装置(内含物质)组装成实验装置,以验证木炭可被浓硫酸氧化成CO2。下列说法正确的是( )练·技能实战DA.丁中溶液褪色,乙中溶液变浑浊,说明甲中生成CO2B.丙中品红溶液褪色,乙中溶液变浑浊,说明甲中生成CO2C.丁和丙中溶液都褪色,乙中溶液变浑浊,说明甲中有CO2生成D.按气流从左向右流向,连接装置的正确顺序是A→F→E→C→D→B感谢您的聆听THANKS苏教版2019必修第一册
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 

.png)
.png)



