

【02-暑假预习】第15讲 影响盐类水解的主要因素及盐类水解的应用 (教师版)-2025年新高二化学暑假衔接讲练 (人教版)
展开 这是一份【02-暑假预习】第15讲 影响盐类水解的主要因素及盐类水解的应用 (教师版)-2025年新高二化学暑假衔接讲练 (人教版),共13页。试卷主要包含了反应物的性质,二元弱酸对应盐的水解常数,在空气中直接蒸发下列盐的溶液等内容,欢迎下载使用。
第一步:学
析教材 学知识:教材精讲精析、全方位预习
第二步:练
练习题 强方法:教材习题学解题、强化关键解题方法
练考点 会应用:核心考点精准练、快速掌握知识应用
第三步:记
串知识 识框架:思维导图助力掌握知识框架、学习目标复核内容掌握
第四步:测
过关测 稳提升:小试牛刀检测预习效果、查漏补缺快速提升
知识点1 影响盐类水解的主要因素
1.反应物的性质
盐类水解程度的大小主要由盐的性质决定,生成盐的弱酸酸性越弱(或弱碱碱性越弱),即越难电离(电离常数越小),该盐的水解程度越大,即越弱越水解。
2.实验探究反应条件对水解程度的影响
已知FeCl3发生水解反应的离子方程式:Fe3++3H2OFe(OH)3+3H+,根据实验操作填写下表:
【特别提醒】盐类的水解平衡移动,符合勒夏特列原理。
知识点二 盐类水解的应用
1.在化学实验中的应用
2.在生产生活中的应用
3. 盐溶液蒸干灼烧后所得产物的判断
大多数盐溶液蒸干灼烧后可以得到相应的盐,以下常见的三类盐溶液蒸干得不到相应的盐
(1)盐溶液水解生成易挥发性酸时,蒸干后一般得到对应的弱碱,如AlCl3、FeCl3溶液蒸干后一般得到Al(OH)3、Fe(OH)3,若灼烧则会生成Al2O3、Fe2O3。
(2)考虑盐受热时是否分解。因为Ca(HCO3)2、NaHCO3、NH4Cl固体受热易分解,因此蒸干灼烧后分别为Ca(HCO3)2→CaO;NaHCO3→Na2CO3;NH4Cl→NH3+HCl。
(3)还原性盐在蒸干时会被O2氧化,如Na2SO3溶液蒸干得到Na2SO4;FeSO4溶液蒸干得到Fe2(SO4)3。
知识点3 水解常数及其应用
1.盐的水解常数表达式
以CH3COONa为例
CH3COO-+H2OCH3COOH+OH-
Kh=eq \f(c(CH3COOH)·c(OH-),c(CH3COO-)),只与温度有关。
2.与对应弱酸电离常数的关系
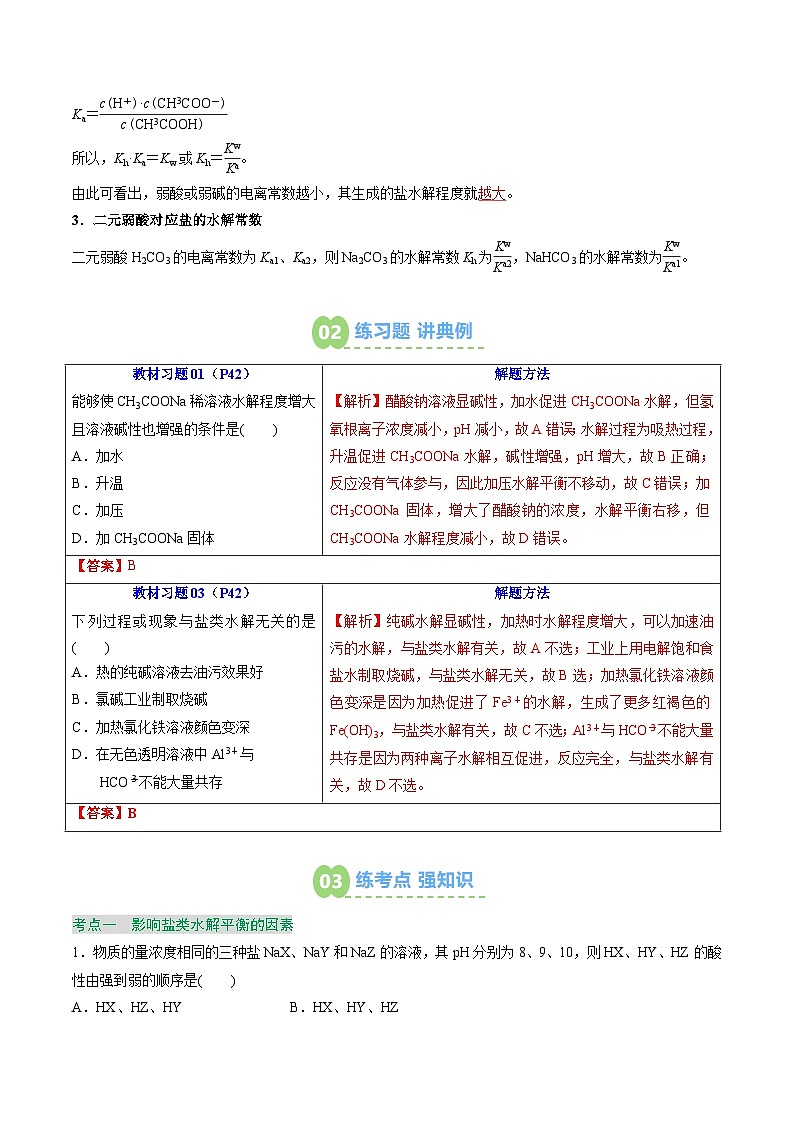
Ka=eq \f(c(H+)·c(CH3COO-),c(CH3COOH))
所以,Kh·Ka=Kw或Kh=eq \f(Kw,Ka)。
由此可看出,弱酸或弱碱的电离常数越小,其生成的盐水解程度就越大。
3.二元弱酸对应盐的水解常数
二元弱酸H2CO3的电离常数为Ka1、Ka2,则Na2CO3的水解常数Kh为eq \f(Kw,Ka2),NaHCO3的水解常数为eq \f(Kw,Ka1)。
考点一 影响盐类水解平衡的因素
1.物质的量浓度相同的三种盐NaX、NaY和NaZ的溶液,其pH分别为8、9、10,则HX、HY、HZ的酸性由强到弱的顺序是( )
A.HX、HZ、HY B.HX、HY、HZ
C.HZ、HY、HX D.HY、HZ、HX
【答案】B
【解析】利用盐类水解规律“越弱越水解,谁强显谁性”,结合同浓度三种酸对应的钠盐的溶液的pH可推知,碱性越强则对应的酸越弱。
2.为了使NH4Cl溶液中c(Cl-)与c(NHeq \\al(+,4))浓度比为1∶1,可在NH4Cl溶液中加入( )
①适量的HCl ②适量的NaCl ③适量的氨水 ④适量的NaOH ⑤适量的硫酸
A.①②⑤ B.③⑤ C.③④ D.④⑤
【答案】B
【解析】NH4Cl溶液中存在NHeq \\al(+,4)+H2ONH3·H2O+H+,为增大NHeq \\al(+,4)浓度,应加入酸或NH3·H2O,①加入HCl虽然增大了H+的浓度,但也增大了Cl-的浓度,不符合题目要求。
3.等物质的量浓度的下列溶液中c(NHeq \\al(+,4))由多到少的关系正确的是( )
①NH4Cl ②NH4HSO4 ③CH3COONH4 ④NH4Al(SO4)2 ⑤NH3·H2O ⑥(NH4)2SO4
A.①②③④⑤⑥ B.④⑥②①③⑤
C.②①③④⑤⑥ D.⑥②④①③⑤
【答案】D
【解析】①NH4Cl ===NHeq \\al(+ ,4)+Cl-;②NH4HSO4===NHeq \\al(+ ,4)+H++SOeq \\al(2-,4);③CH3COO-+H2OCH3COOH+OH-,促进NHeq \\al(+,4)的水解;④NH4Al(SO4)2===NHeq \\al(+,4)+Al3++2SOeq \\al(2-,4),Al3++3H2OAl(OH)3+3H+,抑制NHeq \\al(+,4)水解;⑤NH3·H2ONHeq \\al(+,4)+OH-,NH3·H2O只有少部分电离;⑥(NH4)2SO4===2NHeq \\al(+ ,4)+SOeq \\al(2-,4);故溶液中c(NHeq \\al(+,4))由多到少的顺序为⑥②④①③⑤。
6.在反应Al3++3H2OAl(OH)3+3H+的平衡体系中,要使平衡向水解方向移动,且使溶液的pH增大,应采取的措施是( )
A.加热 B.通入HCl气体
C.加入适量的NaOH溶液 D.加入固体AlCl3
【答案】C
【解析】盐类的水解存在一个平衡状态,当条件发生变化时,平衡可能发生移动,状态发生改变。A、C、D项都可促使水解平衡向水解方向移动,B项抑制水解反应的进行。采取措施后,使溶液的pH增大的是C项。
考点二 盐溶液蒸干(灼烧)产物的判断
5.在空气中直接蒸发下列盐的溶液:①Fe2(SO4)3;②Na2CO3;③KCl;④CuCl2;⑤NaHCO3。可以得到相应盐的晶体(可以含有结晶水)的是( )
A.①②③ B.①③⑤ C.②④ D.①③④⑤
【答案】A
【解析】①加热Fe2(SO4)3溶液时虽发生水解,但硫酸难挥发,蒸发Fe2(SO4)3溶液可得到Fe2(SO4)3晶体,故正确;②加热Na2CO3溶液水解生成NaOH,但NaOH和空气中的CO2反应又得到Na2CO3晶体,故正确;③KCl性质稳定,加热其溶液可得到KCl晶体,故正确;④加热CuCl2溶液水解生成氢氧化铜和HCl,HCl易挥发,得到氢氧化铜晶体,故错误;⑤NaHCO3不稳定,加热易分解生成Na2CO3,故错误。
6.为了得到比较纯净的物质,使用的方法恰当的是( )
A.向Na2CO3饱和溶液中通入过量的CO2后,在加压、加热的条件下,蒸发得到NaHCO3晶体
B.加热蒸发AlCl3饱和溶液可得到纯净的AlCl3晶体
C.向FeBr2溶液中加入过量的氯水,加热蒸发得到FeCl3晶体
D.向FeCl3溶液中加入足量的NaOH溶液,经过滤、洗涤沉淀,再充分灼烧沉淀得到Fe2O3
【答案】D
【解析】A项不恰当,因为NaHCO3加热易分解;B、C项也不恰当,因为AlCl3与FeCl3在加热蒸发的情况下,分别发生反应:Al3++3H2OAl(OH)3+3H+、Fe3++3H2OFe(OH)3+3H+,由于HCl挥发,水解趋于完全,最终得到的是Al(OH)3和Fe(OH)3。
7.下列物质的水溶液在空气中小心加热蒸干至质量不再减少,能得到较纯净的原溶质的是( )
①CuSO4 ②FeSO4 ③Ca(HCO3)2 ④NH4HCO3 ⑤KMnO4 ⑥FeCl3
A.全部 B.仅①②
C.仅①⑤ D.仅①
【答案】D
【解析】①CuSO4溶液水解生成氢氧化铜和硫酸,硫酸是难挥发性酸,故加热蒸干至质量不再减少时,能得到较纯净的原溶质;②FeSO4具有还原性,加热时Fe2+被氧化为Fe3+;③Ca(HCO3)2受热分解生成碳酸钙、二氧化碳和水,加热蒸干至质量不再减少时,能得到较纯净的碳酸钙;④NH4HCO3受热分解生成NH3、H2O和CO2,得不到原溶质;⑤KMnO4加热到质量不变时分解生成锰酸钾、二氧化锰和氧气,得不到原溶质;⑥FeCl3溶液水解生成氢氧化铁和氯化氢,加热时,氯化氢挥发促进FeCl3水解得到氢氧化铁,得不到原溶质。
考点三 盐类水解对离子共存的影响
8.下列离子因发生相互促进的水解反应而不能大量共存的是( )
A.K+、S2-、Al3+、AlOeq \\al(-,2) B.MnOeq \\al(-,4)、Na+、SOeq \\al(2-,4)、K+
C.SOeq \\al(2-,4)、Fe3+、S2-、K+ D.Fe2+、Cl-、H+、NOeq \\al(-,3)
【答案】A
【解析】A项,Al3+与S2-、AlOeq \\al(-,2)能发生相互促进的水解反应;C中的Fe3+与S2-和D中的Fe2+、H+、NOeq \\al(-,3)都因为发生氧化还原反应而不能大量共存。
9.在下列给定条件的溶液中,一定能大量共存的离子组是( )
A.无色溶液:Ca2+、H+、Cl-、HSOeq \\al(-,3)
B.能使pH试纸呈红色的溶液:Na+、NHeq \\al(+,4)、I-、NOeq \\al(-,3)
C.FeCl3溶液:K+、Na+、SOeq \\al(2-,4)、AlOeq \\al(-,2)
D.常温下,eq \f(Kw,c(H+))=0.1 ml·L-1的溶液:Na+、K+、SiOeq \\al(2-,3)、NOeq \\al(-,3)
【答案】D
【解析】A中H+与HSOeq \\al(-,3)不能共存;B中NOeq \\al(-,3)在酸性条件下具有强氧化性,可氧化I-,不能共存;C中Fe3+与AlOeq \\al(-,2)相互促进强烈水解生成Fe(OH)3、Al(OH)3,不能共存;D中溶液为碱性,离子可共存。
考点四 盐类水解的综合应用
10.下列关于盐类水解的应用中,说法正确的是( )
A.加热蒸干Na2CO3溶液,最后可以得到NaOH和Na2CO3的混合固体
B.除去MgCl2溶液中的Fe3+,可以加入NaOH固体
C.明矾净水的原理:Al3++3H2OAl(OH)3(胶体)+3H+
D.加热蒸干KCl溶液,最后得到KOH固体(不考虑与CO2的反应)
【答案】C
【解析】加热蒸干Na2CO3溶液,最后得到Na2CO3固体,A错误;镁离子、铁离子均能与OH-反应生成沉淀,所以不能用NaOH除去MgCl2溶液中的Fe3+,B错误;明矾在水中电离出铝离子,铝离子水解生成的氢氧化铝胶体具有吸附性,即Al3++3H2OAl(OH)3(胶体)+3H+,C正确;KCl不水解,加热蒸干KCl溶液,最后得到KCl固体,D错误。
11.下列说法中正确的是( )
A.AlCl3溶液和Al2(SO4)3溶液分别加热、蒸发、浓缩结晶、灼烧,所得固体的成分相同
B.实验室配制FeCl3溶液时,往往在FeCl3溶液中加入少量的硫酸
C.向CuCl2溶液中加入CuO,调节pH可除去溶液中混有的Fe3+
D.用Na2CO3和Al2(SO4)3两种溶液可作泡沫灭火剂
【答案】C
【解析】AlCl3溶液和Al2(SO4)2溶液分别加热、蒸发、浓缩结晶、灼烧,前者得到Al2O3,后者得到Al2(SO4)3,所得固体的成分不相同,故A错误;配制FeCl3溶液时,应将FeCl3固体溶解在盐酸中,再加水稀释到所需的浓度,若溶于硫酸,会引入杂质离子SOeq \\al(2-,4),故B错误;Fe3++3H2OFe(OH)3+3H+,向CuCl2溶液中加入CuO,消耗H+,使上述水解平衡正向移动生成氢氧化铁沉淀,达到通过调节pH除去溶液中混有的Fe3+的目的,故C正确;泡沫灭火器中常使用的原料是NaHCO3和Al2(SO4)3,故D错误。
12.下列过程或现象与盐类水解无关的是( )
A.热的纯碱溶液去油污效果好
B.氯碱工业制取烧碱
C.加热氯化铁溶液颜色变深
D.在无色透明溶液中Al3+与HCOeq \\al(-,3)不能大量共存
【答案】B
【解析】A.纯碱水解显碱性,加热时水解程度增大,可以加速油污的水解,与盐类水解有关,故A不选;B.工业上用电解饱和食盐水制取烧碱,与盐类水解无关,故B选;C.加热氯化铁溶液颜色变深是因为加热促进了Fe3+的水解,生成了更多红褐色的Fe(OH)3,与盐类水解有关,故C不选;D.Al3+与HCOeq \\al(-,3)不能大量共存是因为两种离子水解相互促进,反应完全,与盐类水解有关,故D不选。
知识导图记忆
知识目标复核
【学习目标】
1.了解影响盐类水解平衡的因素,分析外界条件对盐类水解平衡的影响。
2.了解盐类水解在生产生活中的应用。
3.盐的水解常数及其应用。
【学习重难点】
1.外界条件对盐类水解平衡的影响。
2.盐类水解的应用。
1.(24-25高二上·湖北黄冈·月考)化学与生产、生活密切相关,下列事实与盐类的水解无关的是
A.用热的纯碱溶液洗涤餐具上的油污B.用硫单质处理水银
C.草木灰与铵态氮肥不能混合使用D.用可溶性的铁盐作净水剂
【答案】B
【解析】盐的水解是一个吸热过程,升高温度水解程度增大,则热的纯碱溶液中c(OH-)比冷的纯碱溶液中大,去除油污的效果好,A不符合题意;汞易挥发,汞蒸汽会污染环境,用硫单质处理水银时,发生反应生成不挥发的HgS,与盐类的水解无关,B符合题意;草木灰的主要成分为K2CO3,水解使溶液显碱性,与铵态氮肥中的铵根离子反应生成氨气逸出,从而使肥分损失,所以草木灰等碱性肥料与铵态氮肥不能混合使用,C不符合题意;可溶性的铁盐在水溶液中发生水解,生成氢氧化铁胶体,具有吸附水中悬浮颗粒物的能力,可用作净水剂,D不符合题意;故选B。
2.(24-25高二上·广东广州·期中)K2Cr2O7在水溶液中存在平衡:Cr2O(橙)+H2O2CrO(黄)+2H+,下列说法正确的是
A.该反应是氧化还原反应
B.加入适量NaHSO4固体,平衡逆向移动
C.加入浓NaOH溶液,溶液呈橙色
D.向体系中加入适量水,平衡不移动
【答案】B
【解析】该反应中元素化合价没有发生变化,不是氧化还原反应,A项错误;向该溶液中加入NaHSO4固体,NaHSO4在溶液中电离出Na+、H+和SO。则溶液中H+浓度增大,平衡逆向移动,B项正确;向该溶液中加入浓NaOH溶液,OH-和H+中和,c(H+)降低,平衡向正反应方向移动,溶液呈黄色,C项错误;向该溶液中加入水,Cr2O、CrO、H+浓度均降低导致正逆反应速率均减慢,由于生成物系数之和大于反应物系数之和(水是纯液体,其系数不计算在内),所以Q7
B.NaOH、、的溶液均呈碱性,可以大量共存
C.在溶液中滴加2滴酚酞溶液显浅红色,微热,红色加深
D.“错把陈醋当成墨,写尽半生纸上酸”中陈醋里的醋酸是弱电解质
【答案】B
【解析】为强碱弱酸盐,水解使溶液显碱性,其pH>7,A正确;NaOH与不能共存:,B错误;为强碱弱酸盐,水解显碱性,盐类的水解是吸热过程,所以加热促进的水解,碱性增强,溶液红色加深,C正确;醋酸是弱酸,在水中能部分电离产生和,属于弱电解质,D正确;故选B。
4.(24-25高二上·河南·期中)在的平衡体系中,要使平衡向水解方向移动,且使溶液的pH增大,应采取的措施是
①加热 ②通入HCl ③加入适量 ④加入溶液
A.③④B.②③C.①②D.①④
【答案】A
【解析】①加热促进水解,氢离子浓度增大,但pH减小;②通入HCl,抑制水解,pH减小;③加入适量的KOH(s),H+与KOH反应,则向水解方向移动且使溶液的pH增大;④加入Na2SO4溶液,相当于加水,水解平衡正向移动,氢离子浓度减小,pH增大;故③④符合题意;故答案选A。
5.(24-25高二上·河南新乡·期中)常温下,关于0.1ml/L氯化铵溶液的下列说法中,错误的是
A.加入适量的水,减小,增大
B.该温度下,水的离子积常数
C.生活中,可用该溶液来除铁锈
D.该溶液中一定存在
【答案】A
【分析】NH4Cl溶液中存在:NH4Cl=+Cl-,H2OH++OH-,+H2ONH3·H2O+H+,且稀释电解质溶液对盐类水解起到促进作用,据此分析解题。
【解析】已知NH4Cl溶液中存在: +H2ONH3·H2O+H+,加入适量的水,水解平衡正向移动,根据勒夏特列原理可知,减小,减小,A错误;水的离子积是一个平衡常数,仅仅是温度的函数,故该温度下,水的离子积常数,B正确;由分析可知,NH4Cl溶液显酸性,故生活中,可用该溶液来除铁锈,C正确;根据电解质溶液中的电荷守恒可知,该溶液中一定存在:,D正确;故选A。
6.(24-25高二上·新疆·月考)在一定条件下,Na2S溶液存在水解平衡;S2-+H2OHS-+OH-。下列说法正确的是
A.加水稀释,平衡正移,HS-浓度增大B.升高温度,减少
C.稀释溶液,水解平衡常数不变D.加入NaOH固体,溶液pH减小
【答案】C
【解析】加水稀释,平衡正移,但是HS-浓度减小,故A错误;水解是吸热反应,升温,平衡正向移动,硫氢根离子浓度增大,硫离子浓度减小,所以增大,故B错误;水解平衡常数只受温度影响,温度不变,平衡常数不变,故C正确;加入氢氧化钠,溶液的碱性增强,溶液pH增大,故D错误;故选C。
7.(24-25高二上·广东江门·期末)溶液中,如果要使更接近于,可以采取的措施是
A.加入适量水 B.加入少量溶液
C.通入适量气体 D.加热
【答案】C
【解析】氯化铁是强酸弱碱盐,在溶液中水解生成氢氧化铁和盐酸,若要使0.1ml/L氯化铁溶液中铁离子浓度更接近于0.1ml/L,应向溶液中通入适量氯化氢气体,增大溶液中的盐酸浓度,使水解平衡向逆反应方向移动,故选C。
8.(24-25高二上·陕西铜川·月考)在一定条件下,溶液存在水解平衡:,下列说法正确的是
A.升高温度,增大B.加入固体,浓度增大
C.稀释溶液,水解平衡常数增大D.加入固体,溶液减小
【答案】A
【解析】硫离子在溶液中的水解反应为吸热反应,升高温度,平衡向正反应方向移动,溶液中硫离子浓度减小,氢硫酸根离子浓度增大,则溶液中增大,故A正确;向溶液中加入硫酸铜固体,铜离子与溶液中的硫离子反应生成硫化铜沉淀,溶液中的硫离子浓度减小,平衡向逆反应方向移动,溶液中氢硫酸根离子浓度减小,故B错误;水解平衡常数为温度函数,温度不变,水解平衡常数不变,则稀释溶液时,水解平衡常数不变,故C错误;向溶液中加入氢氧化钠固体,溶液中氢氧根离子浓度增大,溶液pH增大,故D错误;故选A。
9.(24-25高二上·新疆乌鲁木齐·月考)0.1的溶液中,由于的水解,使得。如果要使更接近于0.1,可以采取的措施是
A.加入少量盐酸B.加入适量的水C.加入适量的D.加热
【答案】C
【分析】水解的离子方程式为。
【解析】加入少量盐酸,和盐酸反应生成KHCO3,浓度减小,故不选A;加入适量的水稀释,浓度减小,故不选B;加入适量的,氢氧根离子浓度增大,平衡逆向移动,浓度增大,更接近于0.1,故选C;水解吸热,加热平衡正向移动,浓度减小,故不选D;故选C。
10.(24-25高二上·北京·期中)下列事实能从平衡移动的角度解释的是
A.、I2、平衡混和气加压后颜色变深
B.采用500℃的高温条件,有利于合成氨气
C.黄色的溶液,加热,溶液颜色加深
D.催化氧化为时,工业上采用常压而非高压
【答案】C
【解析】、I2发生反应,加压后各物质浓度增大,颜色加深,但平衡不移动,因此不能从平衡移动的角度解释,故A错误;合成氨的反应为放热,高温不利于平衡正向移动,采用高温是为了加快反应速率,故B错误;水解生成氢氧化铁,水解为吸热反应,升高温度有利于平衡正向移动,从而增大了氢氧化铁的浓度,使颜色加深,故C正确;,高压有利平衡正向移动,但常压条件下该反应转化率已经较高,未不增加成本,工业常采用常压,故D错误;故选C。
11.(24-25高二上·北京·期中)对于溶液的水解平衡与移动,下列说法正确的是
A.加入少量固体,比值增大
B.加入少量固体然后恢复至室温,水解程度增大
C.加入适量蒸馏水稀释溶液,溶液中所有离子浓度均减小
D.通入少量气体,水解程度增大,溶液增大
【答案】A
【解析】加入Na2CO3固体,会抑制CH3COO-的水解,使比值增大,A正确;加入NaOH固体,会抑制CH3COONa水解,水解程度减小,B错误;加水稀释,CH3COO-、H+浓度均减小,但温度不变,Kw不变,Kw=c(H+)·c(OH-),c(H+)减小,则c(OH-)就增大,C错误;通入HCl气体,会促进CH3COONa水解,水解程度增大,但溶液pH减小,D错误;故选A。
12.(24-25高二上·辽宁·月考)常温下,物质的量浓度相同的下列溶液:①溶液、②溶液、③溶液、④溶液、⑤溶液、⑥溶液,按由小到大排列的顺序正确的是
A.⑥
相关试卷
这是一份【02-暑假预习】第15讲 影响盐类水解的主要因素及盐类水解的应用 (教师版)-2025年新高二化学暑假衔接讲练 (人教版),共13页。试卷主要包含了反应物的性质,二元弱酸对应盐的水解常数,在空气中直接蒸发下列盐的溶液等内容,欢迎下载使用。
这是一份【02-暑假预习】第15讲 影响盐类水解的主要因素及盐类水解的应用 (学生版)-2025年新高二化学暑假衔接讲练 (人教版),共9页。试卷主要包含了反应物的性质,二元弱酸对应盐的水解常数,在空气中直接蒸发下列盐的溶液等内容,欢迎下载使用。
这是一份【暑假预习】第15讲 影响盐类水解的主要因素及盐类水解的应用 -2025年新高二化学暑假衔接讲练 (人教版)(含答案),文件包含暑假预习第15讲影响盐类水解的主要因素及盐类水解的应用教师版-2025年新高二化学暑假衔接讲练人教版docx、暑假预习第15讲影响盐类水解的主要因素及盐类水解的应用学生版-2025年新高二化学暑假衔接讲练人教版docx等2份试卷配套教学资源,其中试卷共22页, 欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)
.png)


