

广东省大湾区2025年初中学业水平质量监测卷一化学试题(解析版)
展开 这是一份广东省大湾区2025年初中学业水平质量监测卷一化学试题(解析版),共18页。试卷主要包含了考生必须保持答题卡的整洁,可能用到的相对原子质量, 氢化钛作为储氢材料备受关注等内容,欢迎下载使用。
注意事项:1.答题前,考生务必用黑色字迹的签字笔或钢笔将自己的姓名、座位号和考号填写在答题卡上。用2B铅笔在“考号填涂区”相应位置填涂自己的考号。将条形码粘贴在答题卡“条形码粘贴处”。
2.作答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目选项的答案信息点涂黑;如需改动,用橡皮擦干净后,再选涂其他答案,答案不能答在试卷上。
3.非选择题必须用黑色字迹的签字笔或钢笔作答,答案必须写在答题卡各题目指定区域内相应位置上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用铅笔和涂改液。不按以上要求作答的答案无效。
4.考生必须保持答题卡的整洁。考试结束后,将试卷和答题卡一并交回。
5.可能用到的相对原子质量:H-1 C-12 N-14 O-16 Al-27 S-32 Ti-48 Fe-56
一、选择题:本大题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题目要求的。
1. 广东文化底蕴深厚,越看“粤”精彩。下列物品主要由金属材料制成的是( )
A. 西周铜盉(信宜) B. 潮汕嵌瓷(潮州)
C. 木制龙舟(顺德) D. 粤剧戏服(广州)
【答案】A
【解析】A、铜盉是西周时期的一种青铜器,青铜是一种合金,主要由铜和锡组成。属于金属材料,选项正确;
B、潮汕嵌瓷是一种传统工艺,主要材料是陶瓷,属于无机非金属材料,选项错误;
C、木制龙舟,主要由木材制成,而不是金属。选项错误;
D. 粤剧戏服 粤剧戏服通常由布料制成,主要是天然纤维,选项错误;
故选A。
2. 广东省有着浓厚的岭南文化气息,具有众多非物质文化遗产。下列说法正确的是( )
A. 绘画的墨汁属天然有机色素B. 工夫茶的茶水,属于纯净物
C. 剪纸的运剪过程属物理变化D. 木雕的雕刻过程属化学变化
【答案】C
【解析】A、墨汁的主要显色成分是炭黑,炭黑主要成分是碳的单质,不属于有机物,选项错误;
B、茶水中含有多种物质,属于混合物,选项错误;
C、剪纸的运剪过程中没有新物质生成属于物理变化,选项正确;
D、木雕的雕刻过程中没有新物质生成属于物理变化,选项错误;
故选C。
3. 强调实验安全非常重要,下列图标与做“粗盐中难溶性杂质的去除”实验无关的是( )
A. 明火B. 护目镜
C. 洗手D. 锐器
【答案】D
【解析】A、粗盐提纯需要蒸发结晶,需要用到明火,故与实验有关;
B、在实验过程中,护目镜是用于保护眼睛的安全设备,尤其是在进行可能产生飞溅或有害气体的操作时,粗盐提纯需要蒸发结晶,故与实验有关;
C、实验结束要洗手,与实验有关;
D、粗盐提纯过程中不会用到锋利物品,与实验无关。
故选:D。
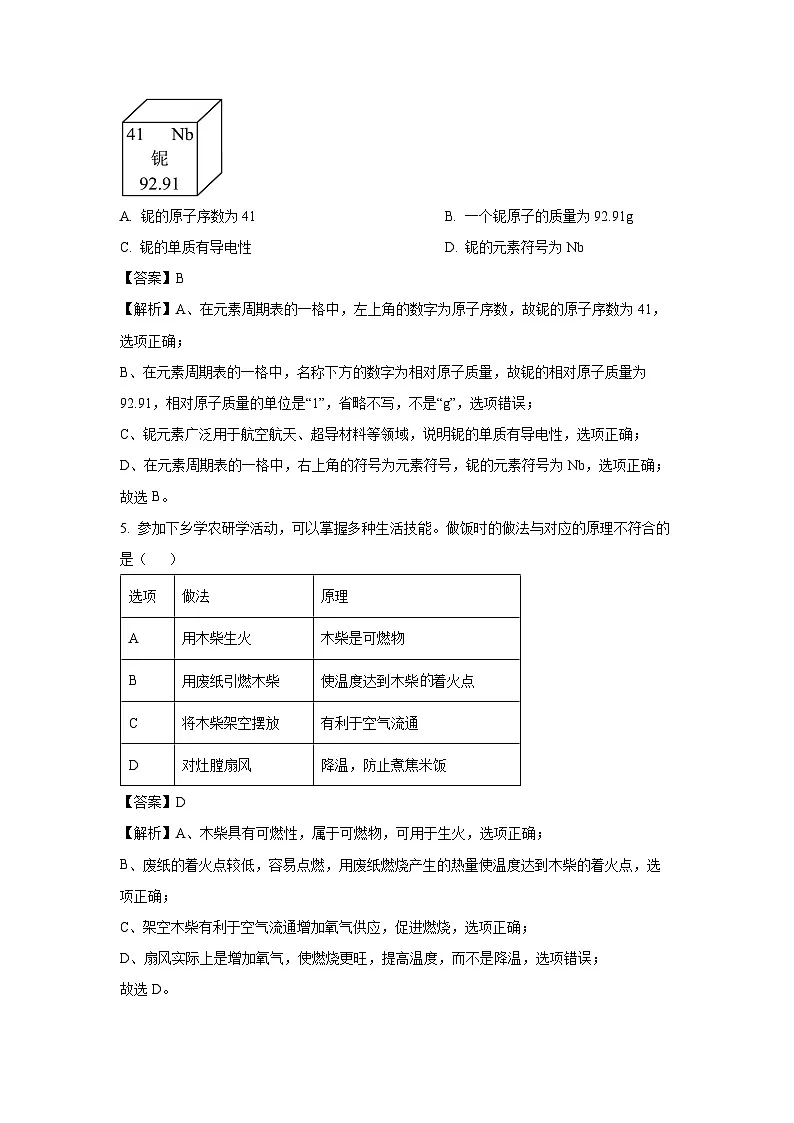
4. 铌元素广泛用于航空航天、超导材料等领域,它在元素周期表中的信息如图所示,下列说法错误的是( )
A. 铌的原子序数为41B. 一个铌原子的质量为92.91g
C. 铌的单质有导电性D. 铌的元素符号为Nb
【答案】B
【解析】A、在元素周期表的一格中,左上角的数字为原子序数,故铌的原子序数为41,选项正确;
B、在元素周期表的一格中,名称下方的数字为相对原子质量,故铌的相对原子质量为92.91,相对原子质量的单位是“1”,省略不写,不是“g”,选项错误;
C、铌元素广泛用于航空航天、超导材料等领域,说明铌的单质有导电性,选项正确;
D、在元素周期表的一格中,右上角的符号为元素符号,铌的元素符号为Nb,选项正确;
故选B。
5. 参加下乡学农研学活动,可以掌握多种生活技能。做饭时的做法与对应的原理不符合的是( )
【答案】D
【解析】A、木柴具有可燃性,属于可燃物,可用于生火,选项正确;
B、废纸的着火点较低,容易点燃,用废纸燃烧产生的热量使温度达到木柴的着火点,选项正确;
C、架空木柴有利于空气流通增加氧气供应,促进燃烧,选项正确;
D、扇风实际上是增加氧气,使燃烧更旺,提高温度,而不是降温,选项错误;
故选D。
6. 分类是一种科学方法,可使学习更高效。下列物质的分类合理的是( )
A. 酸:HCl、CH4B. 氧化物:Na2O、H2O
C. 碱:Cu2(OH)2CO3、Fe(OH)3D. 盐:Al2O3、AlCl3
【答案】B
【解析】A、HCl是离解出来的阳离子全部为氢离子,都属于酸;CH4是含碳化合物,属于有机物,不属于酸,选项错误;
B、Na2O、H2O都是由两种元素组成其中一种元素是氧元素的化合物,都属于氧化物,选项正确;
C、Fe(OH)3是解离出来的阴离子都是氢氧根离子的化合物,属于碱;Cu2(OH)2CO3能解离出金属离子和酸根离子,属于盐(或解离出的阴离子除氢氧根离子还有碳酸根离子,故不属于碱),选项错误;
D、Al2O3属于氧化物,AlCl3能解离出金属离子和酸根离子,属于盐,选项错误;
故选B。
7. 我国现代科学家为化学学科发展作出了不懈的努力,下列叙述错误的是( )
A. 张青莲院士为元素名称的中文命名作出了卓越贡献
B. 闵恩泽院士为我国炼油催化剂制造技术奠定了基础
C. 屠呦呦研究员为世界治疗疟疾作出了巨大贡献
D. 徐光宪院士为我国稀土工业发展作出了卓越贡献
【答案】A
【解析】A、张青莲主持测定了铟、铱、铕等原子的相对原子质量新值,为相对原子质量的测定做出了卓越贡献,徐寿为元素名称的中文命名作出了卓越贡献,选项错误;
B、闵恩泽研发了多种用于石油化工生产的催化剂,为我国炼油催化剂制造技术奠定了基础,选项正确;
C、屠呦呦发现了青蒿素,为世界治疗疟疾作出了巨大贡献,选项正确;
D、徐光宪是稀土分离专家,创立了“串级萃取理论”,为我国稀土工业发展作出了卓越贡献,选项正确;
故选A。
8. 化学用语是学习化学的重要工具,下列含氮物质中氮元素的化合价显+3价的是( )
A. NH3B. N2C. HNO2D. NO2
【答案】C
【解析】A、NH3中氢元素的化合价为+1,根据化合物中正负化合价代数为0,则氮元素的化合价为-3,故选项不符合题意;
B、N2为单质,则氮元素的化合价为0,故选项不符合题意;
C、HNO2中氢元素的化合价为+1,氧元素的化合价为-2价,设氮元素的化合价为x,根据则有(+1)+ x+(-2)×2=0,得x=+3价,故选项符合题意;
D、NO2中氧元素的化合价为-2价,根据化合物中正负化合价代数为0,则氮元素的化合价为+4,故选项不符合题意;
故选C。
9. 氢化钛(TiH2)作为储氢材料备受关注。其可用钛粉(Ti)和H2在一种纳米催化剂的作用下,控制一定的温度和压强反应得到,反应的微观示意图如图所示。下列说法正确的是( )
A. 该反应共生成两种物质
B. 反应的化学方程式为
C. 参加反应的物质的质量比为2:3
D. 反应前后纳米催化剂的化学性质不变
【答案】D
【解析】图中发生的反应为钛粉(Ti)和H2在催化剂和一定条件下生成氢化钛(TiH2),方程式为:反应的化。
A、反应只生成了一种物质氢化钛,反应后出现的(氢分子),是反应过程中剩余的,不是生成的,选项错误;
B、反应的化学方程式为,选项错误;
C、参加反应的物质的质量比为(48×2):(2×2)=24:1,选项错误;
D、根据:在化学反应中改变其他物质的反应速率,而本身的质量和化学性质在反应前后都没有发生变化的物质叫催化剂,反应前后纳米催化剂的化学性质不变,选项正确;
故选D。
10. 实验室用KMnO4制取O2时不会用到的仪器装置是( )
A. B.
C. D.
【答案】B
【解析】A、实验室用高锰酸钾制氧气时,需要加热,故需要用到铁架台和试管,故选项不符合题意;
B、实验室用高锰酸钾制氧气时,需用固固加热装置,不会用固液常温装置,故选项符合题意;
C、氧气密度比空气大,需要用向上排空气法收集,故需要用到向上排空气法收集装置,故选项不符合题意;
D、实验室用高锰酸钾制氧气时,需要加热,故需要用到酒精灯,故选项不符合题意。
故选:B。
侯德榜是我国化学工业的先驱,其发明的“侯氏制碱法”为我国基本化工原料工业奠定了基础。“侯氏制碱法”的简易流程如图甲所示。完成下面小题。
11. 根据如图乙所示的溶解度曲线,判断沉淀池中生成的沉淀为( )
A. NaClB. NH4Cl
C. NaHCO3D. NH4Cl和NaCl
12. 已知X某种气体,其化学式为( )
A. CO2B. HClC. COD. NH3
13. 纯碱(Na2CO3)在工业生产中常作为碱使用。下列关于Na2CO3的说法错误的是( )
A. 水溶液呈碱性
B. 属于碱
C. 与稀盐酸反应可产生CO2
D. 广泛用于玻璃、造纸、纺织等工业生产
【答案】11. C 12. A 13. B
【解析】11.沉淀池中的反应为氯化钠、氨气、二氧化碳与水反应生成碳酸氢钠和氯化铵,根据如图乙所示的溶解度曲线,碳酸氢钠的溶解度远远小于氯化铵和氯化钠,结合煅烧炉反应产生碳酸钠,可知沉淀为碳酸氢钠。
故选C;
12.反应沉淀出的碳酸氢钠加入分解生成碳酸钠、水和二氧化碳,故X为二氧化碳。
故选A;
13.A、碳酸钠溶液显碱性,所以俗称纯碱,选项正确;
B、碳酸钠是由金属离子和酸根离子构成的化合物,属于盐,选项错误;
C、碳酸钠与盐酸反应生成氯化钠、水和二氧化碳,选项正确;
D、碳酸钠广泛用于玻璃、造纸、纺织等工业生产,选项正确;
故选B。
14. 部分含碳物质的分类与碳元素的化合价关系如图所示。下列推断不合理的是( )
A. a是可燃冰的主要成分
B. b可能是天然存在的最硬的物质
C. 实验室中可用e制备d
D. c和d不可以相互转化
【答案】D
【解析】A、a点的物质类别是氢化物,其中碳元素的化合价为-4价,则a为甲烷,是可燃冰的主要成分,故选项说法合理;
B、b点的物质类别是单质,其中碳元素的化合价为0,金刚石是碳单质,所以b可能是金刚石,故选项说法合理;
C、e点的物质类别是盐,其中碳元素的化合价为+4价,则是e可以是碳酸钙;d点的物质类别是氧化物,其中碳元素的化合价为+4价,则d为二氧化碳,实验室常用碳酸钙与盐酸反应制取二氧化碳,故选项说法合理;
D、d为二氧化碳,c点的物质类别是氧化物,其中碳元素的化合价为+2价,则c为一氧化碳,一氧化碳在氧气中燃烧生成二氧化碳,二氧化碳与碳在高温条件下生成一氧化碳,两者可以相互转化,故选项说法不合理。
故选D。
15. 下列鉴别或除杂操作正确的是( )
【答案】D
【解析】A、氢氧化钠既能与HCl反应,也能与二氧化碳反应,会吸收掉二氧化碳,选项错误;
B、盐酸能与氧化铜反应,不与铜反应,除去了主要物质,选项错误;
C、碳酸钠既能与氯化钙反应碳酸钙沉淀,也能与氯化钡反应生成碳酸钡沉淀,除去了主要物质,选项错误;
D、NaOH溶于水放热,溶液温度显著升高。 NH4NO3溶于水吸热,溶液温度显著降低。 通过温度变化可以区分,选项正确;
故选D。
二、非选择题:本大题共6小题,第16小题7分,第17小题8分,第18~21小题各10分,共55分。
16. 《天工开物》蕴含着丰富的化学知识与方法。其中关于银的冶炼过程如图所示。
(1)铅、银属于___________(填“金属”或“非金属”)单质。
(2)“淘洗”时可用水除去矿砂中的一些杂质,其原理是利用了___________。
(3)补充完整“熔矿”时氧气与Ag2S反应的化学方程式:___________。
(4)“熔矿”“结银”操作如图乙所示,所需热量由木炭燃烧提供,木炭充分燃烧反应的化学方程式为___________。
(5)为使图乙中木炭燃烧更充分,可采取的措施是___________(写一条)。
【答案】(1)金属 (2)物质的溶解性不同(合理即可)
(3)2Ag2O (4)
(5)适当向炉膛鼓风(合理即可)
【解析】(1)铅和银都是带“金字旁”的汉字,可知铅和银属于金属单质。
(2)“淘洗” 时用水除去矿砂中的一些杂质,是利用杂质和矿砂在水中溶解性的差异,杂质可溶而矿砂不溶,从而实现分离。
(3)根据质量守恒定律,化学反应前后原子的种类和数目不变。反应前Ag原子个数为4,S原子个数为2,O原子个数为6;反应后已知物质中S原子个数为2,O原子个数为4,还缺少4个Ag原子、2个O原子,所以横线处应补充2Ag2O,这样才能保证反应前后原子种类和数目相等。
(4)木炭充分燃烧时与氧气反应生成二氧化碳,化学方程式为。
(5)将木炭架空能增大木炭与氧气的接触面积,适当向炉膛鼓风能提供更多的氧气,这些措施都能使木炭燃烧更充分。
【科普阅读】
17. 硫元素以硫化物、硫酸盐、有机硫和单质硫等形式广泛存在于自然界。硫在某些系外行星的大气层中以H2S和SO2的形式存在,这些物质经过光化学反应,产生了S8和H2SO4;硫在地壳中的含量为0.048%,是自然界中重要的非金属元素,其在自然界的循环过程如图所示。硫还存在于人体中,是甲硫氨酸(C5H11O2NS)和半胱氨酸(C3H7NO2S)等氨基酸的组成元素。硫是植物维持生命活动所需的元素,可以通过施加硫肥(硫黄或可溶性硫酸盐溶液)补充。我国古代“四大发明”之一的黑火药,主要由硫黄、硝酸钾和木炭按一定比例混合而成。
(1)短文中光化学反应生成的硫单质的化学式是___________。
(2)甲硫氨酸(C5H11O2NS)是一种有机化合物,其中硫元素的质量分数是___________(计算结果保留一位小数)。
(3)试写出一种能增强抗倒伏能力的硫肥:___________(填化学式)。
(4)黑火药燃爆会生成K2S、N2和CO2,写出黑火药燃爆的化学方程式:___________。
(5)由图可知,下列说法正确的是___________(多选,填字母)。
A. 过程Ⅰ中硫元素的化合价升高
B. 减少使用化石能源可以减少SO2排放
C. 含硫有机物和含硫无机物可相互转化
D. 过程Ⅱ是形成酸雨的原因之一
【答案】(1)S8 (2)21.5%
(3)K2SO4(答案合理即可)
(4) (5)ABCD
【解析】(1)由短文可知,光化学反应生成的硫单质的化学式是S8。故填:S8。
(2)甲硫氨酸(C5H11O2NS)中硫元素的质量分数是:
。故填:21.5%。
(3)钾元素可增强作物抗倒伏能力,故填:K2SO4(答案合理即可)。
(4)硫黄、硝酸钾和木炭在点燃条件下反应生成,该反应的化学方程式为:。故填:。
(5)A.过程Ⅰ中,SO2中硫元素化合价为+4,中硫元素化合价为+6,硫元素的化合价升高,故A正确;
B.减少使用化石能源可以减少SO2排放,故B正确;
C.由图可知,含硫有机物和含硫无机物可相互转化,故C正确;
D.过程Ⅱ产生二氧化硫,二氧化硫是形成酸雨的原因之一,故D正确。
故选:ABCD。
【基础实验和跨学科实践】
18. 在化学实验操作中,小明和小红分别抽取了Ⅰ、Ⅱ组试题进行实验。
Ⅰ组:O2和CO2的制取与性质探究
(1)实验室中装置A、B都可以用来制取氧气和二氧化碳,其中仪器a的名称是___________,实验室制取二氧化碳的反应的化学方程式为___________,装置C中凹陷的软质塑料瓶的优点与装置___________(填“A”或“B”)相似。
(2)小明提出用装置C可以验证可燃物燃烧的条件,进行如下实验:
i.捏住乙处瓶身(如图所示)一段时间后,点燃丁处酒精灯,观察到丙处硫不燃烧。
ii.继续实验:放开乙处瓶身,捏住甲处瓶身一段时间,观察到丙处的现象是___________。
通过对比实验i、ii,可以得出结论:物质燃烧需要___________。并且能够得出CO2的化学性质之一是___________。
(3)戊中氢氧化钠溶液的作用是___________。
Ⅱ组:制作简易供氧器
小红制作了如图所示的简易供氧器,她选用的试剂是过碳酸钠和二氧化锰。过碳酸钠易溶于水,在水中分解产生Na2CO3和H2O2.
(4)检验生成的气体是氧气的方法:___________。
(5)右瓶中水的作用是___________。(写一点)
【答案】(1)①. 长颈漏斗 ②. ③. A
(2)①. 发出明亮的蓝紫色火焰 ②. 与氧气接触 ③. 不燃烧、不支持燃烧
(3)吸收SO2,防止污染空气
(4)将带火星的木条放在导管口,木条复燃,说明是氧气
(5)湿润氧气,且可通过产生气泡的速率观测生成氧气的速率
【解析】(1)由图可知,仪器a的名称是:长颈漏斗;
实验室通常用石灰石(或大理石)与稀盐酸反应制取二氧化碳,石灰石的主要成分碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,该反应的化学方程式为:;
装置C中凹陷的软质塑料瓶可通过捏、放塑料瓶下部,控制固液的接触和分离,从而控制反应的发生和停止,A装置中可将固体置于带孔塑料板上,关闭弹簧夹,通过长颈漏斗添加液体,固液接触,生成气体,装置内压强增大,将液体压入长颈漏斗中,固液分离,反应停止,打开弹簧夹,气体导出,固液接触,反应开始,故优点是:可以控制反应的发生和停止,B装置可通过分液漏斗控制液体的滴加速率,从而控制反应速率,故装置C中凹陷的软质塑料瓶的优点与装置A相似;
(2)ii.继续实验:放开乙处瓶身,捏住甲处瓶身一段时间,过氧化氢在二氧化锰的催化下分解生成水和氧气,故丙处硫在氧气中燃烧,观察到的现象是:发出明亮的蓝紫色火焰;
实验i中捏住乙处瓶身(如图所示)一段时间后,石灰石的主要成分碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,点燃丁处酒精灯,丙中硫温度达到了着火点,但是隔绝氧气,不燃烧,实验ii中,放开乙处瓶身,捏住甲处瓶身一段时间,过氧化氢在二氧化锰的催化下分解生成水和氧气,丙处硫与氧气接触,温度达到了着火点,燃烧,故对比实验i、ii,说明燃烧需要与氧气接触;
实验i中捏住乙处瓶身(如图所示)一段时间后,石灰石的主要成分碳酸钙和稀盐酸反应生成氯化钙、二氧化碳和水,点燃丁处酒精灯,丙中硫温度达到了着火点,与二氧化碳接触,丙处硫不燃烧,说明二氧化碳不燃烧、不支持燃烧;
(3)二氧化硫有毒,散逸到空气中,会污染空气,二氧化硫能与氢氧化钠反应,故戊中氢氧化钠溶液的作用是:吸收二氧化硫,防止污染空气;
(4)氧气具有助燃性,故检验生成的气体是氧气的方法是:将带火星的木条放在导管口,木条复燃,说明已经集满;
(5)右瓶中水的作用是:湿润氧气,且可通过产生气泡的速率观测生成氧气的速率。
【科学探究】
19. 老师要求同学们设计实验鉴别稀盐酸、碳酸钠溶液和澄清石灰水三种无色溶液。两组同学分别设计实验如下:
(1)第1组:用紫色石蕊溶液鉴别三种溶液,其设计的理由是___________。老师认为这个方案不严谨,原因是___________。
(2)第2组:分别用三支试管将三种溶液(编号分别为a、b、c)两两进行混合,观察到的现象如下表所示。
由实验现象可推断溶液b是___________。溶液a与溶液c反应的化学方程式是___________。
【实验拓展】将第2组实验剩余的稀盐酸和澄清石灰水进行混合,等充分反应后对所得溶液中溶质的成分进行探究。
【作出猜想】猜想一:只有CaCl2;猜想二:有CaCl2和HCl;猜想三:有CaCl2和Ca(OH)2;猜想四:有CaCl2、HCl和Ca(OH)2。
老师认为猜想四不合理,理由是___________。
【实验探究】为证明其余猜想是否正确,同学们进行了如下实验:
【交流评价】同学们反思后发现实验Ⅱ所得结论不严谨,其理由是___________。
【反思拓展】在分析化学反应后所得物质的成分时,除考虑生成物外,还需考虑___________。
【答案】(1)① 酸性、碱性溶液能使紫色石蕊溶液变色 ②. 碳酸钠溶液与澄清石灰水均能使紫色石蕊溶液变蓝色
(2)①. 澄清石灰水 ②. ③. Ca(OH)2与HCl不能共存 ④. 三 ⑤. 白色沉淀 ⑥. 氯化钙、盐酸均能与硝酸银反应生成氯化银白色沉淀,故加入硝酸银溶液,产生白色沉淀,不能说明猜想一成立 ⑦. 反应物否过量
【解析】(1)紫色石蕊溶液鉴别三种溶液,其设计的理由是酸性、碱性溶液能使紫色石蕊溶液变色;
由于稀盐酸显酸性,能使紫色石蕊溶液变红,碳酸钠溶液显碱性,能使紫色石蕊溶液变蓝,澄清的石灰水即氢氧化钙溶液显碱性,能使紫色石蕊溶液变蓝,因此这个方案不合理;
(2)由于澄清石灰水即氢氧化钙溶液与碳酸钠反应生成碳酸钙白色沉淀和氢氧化钠,所以b中产生白色沉淀,证明b中溶液是澄清石灰水;
由于稀盐酸与碳酸钠反应生成氯化钠、水和二氧化碳气体,所以c中有气泡产生,反应的化学方程式为:;
由于HCl和Ca(OH)2反应生成氯化钙和水,所以HCl和Ca(OH)2不能共存,即猜想四不合理;
Ⅰ取少量反应后的溶液于试管中,加入CuCl2溶液,无明显现象。说明没有氢氧化铜生成,即反应后所得溶液中没有氢氧化钙,所以猜想三不成立;
Ⅱ由于猜想二成立,说明反应后的溶液中含氯化钙,取少量反应后的溶液于试管中,加入硝酸银溶液,氯化钙与硝酸银反应生成氯化银白色沉淀,观察到有白色沉淀产生;
氯化钙与硝酸银反应生成氯化银白色沉淀,盐酸与硝酸银反应也生成氯化银白色沉淀,所以取少量反应后的溶液于试管中,加入硝酸银溶液,有白色沉淀生成,猜想一不一定成立;
由于发生化学反应时反应物不一定正好完全反应,即某种反应物可能有剩余,所以在分析化学反应后所得物质的成分时,除考虑生成物外还需考虑反应物是否有剩余。
20. 用废铁屑(含Fe和Fe2O3)制取FeCO3进而制备铁红(Fe2O3)的主要流程如图1所示。
(1)用粉碎机将废铁屑研成粉末的目的是___________,使反应更充分。
(2)“操作1”的名称为___________。
(3)“溶解池”中得到的溶液的溶质是H2SO4、Fe2(SO4)3以及___________。
(4)从“操作1”中获得的FeCO3固体需要进行洗涤,检验FeCO3固体已洗净的方法是:取最后一次的洗涤液于洁净的试管中,先滴加过量稀盐酸,再滴加___________(填化学式)溶液,无明显现象。
(5)“煅烧窑”中发生反应的化学方程式为___________。
(6)研究团队模拟炼铁的过程,对一定质量的:Fe2O3进行加热,通过精密仪器测定反应过程中固体质量随温度变化的曲线,结果如图所示。
【查阅资料】用CO还原Fe2O3炼铁的过程大致分为以下三个阶段。
阶段1:
阶段2:
阶段3:
i.温度控制在300~500℃时,固体质量没有发生变化,原因是__________。
ii.图中H点对应的固体成分是___________。
iii.图中M点对应a的值为___________。
【答案】(1)增大反应物之间接触面积,使反应更快更充分
(2)过滤 (3)硫酸亚铁/FeSO4
(4)BaCl2(合理即可)
(5)
(6)①. 没有达到反应温度 ②. 四氧化三铁/Fe3O4 ③. 18.0/18
【解析】(1)用粉碎机将废铁屑研成粉末的目的是:增大反应物之间的接触面积,使反应更快更充分;
(2)“操作1”实现了固液分离,名称是:过滤;
(3)废铁屑中含铁和氧化铁,加入稀硫酸,氧化铁和稀硫酸反应生成硫酸铁和水,铁和稀硫酸反应生成硫酸亚铁和氢气,硫酸应过量,故“溶解池”中得到的溶液的溶质是H2SO4、Fe2(SO4)3以及FeSO4;
(4)碳酸钠和硫酸亚铁反应生成硫酸钠和碳酸亚铁,故碳酸亚铁表面可能附着硫酸钠,硫酸钠能与氯化钡反应生成硫酸钡和氯化钠,故检验碳酸亚铁固体已经洗净的方法是:取最后一次的洗涤液于洁净的试管中,先滴加过量稀盐酸,再滴加BaCl2溶液,无明显现象,说明洗涤液中不含硫酸钠,则已经洗涤干净;
(5)由图可知,“煅烧窑”中发生的反应应是碳酸亚铁和空气中的氧气在高温下反应生成氧化铁,根据质量守恒定律,化学反应前后元素的种类不变,反应物中含Fe、C、O,生成物中含Fe、O,故生成物中还应含C,故还应生成了二氧化碳,该反应的化学方程式为:;
(6)i.由化学方程式可知,温度达到500℃才开始反应,故温度控制在300~500℃时,固体质量没有发生变化,原因是:没有达到反应温度;
ii.温度在500-600℃时,一氧化碳和氧化铁反应生成四氧化三铁和二氧化碳,H点时氧化铁已经完全反应,此时固体为四氧化三铁;
iii.温度在600-700℃时,一氧化碳和四氧化三铁反应生成FeO和二氧化碳,故M点固体为FeO,根据质量守恒定律,化学反应前后元素的种类和质量不变,故最后得到铁的质量与FeO中铁元素的质量相等,由图可知,最后生成铁的质量为14.0g,则FeO的质量为:,故对应a的值为18.0。
21. 我国有着储量丰富的低品铝土矿资源,科研人员通过采用焙烧—碱浸预脱硅工艺,获得高铝硅比铝精矿,实现“贫矿变富矿”,并有效地提高了氧化铝的溶出率。其工艺流程如图所示。
(1)流程中的“碱浸脱硅”是使用烧碱溶液浸泡“铝土矿焙砂”,以除去矿砂中的SiO2,其反应同CO2与烧碱反应相似。请写出“碱浸脱硅”反应的化学方程式:___________。
(2)现有一种铝土矿样品,氧化铝的含量为40%,其中有95%的氧化铝能转化成高纯度氧化铝,然后通过电解制得金属铝,理论上100t该铝土矿可制得金属铝___________t(写出计算过程,计算结果保留一位小数,工业制铝反应的化学方程式:)。
(3)某种铝土矿采用上述工艺可获得铝精矿。其预脱硅效果受焙烧温度等因素影响。其中焙烧温度对脱硅率的影响如图所示,根据曲线图判断,最佳焙烧温度是___________。
【答案】(1)
(2)解:设可制得金属铝的质量为x。
x=20.1t
答:可制得20.1t的金属铝
(3)1050℃
【解析】(1)“碱浸脱硅”中二氧化硅和氢氧化钠反应生成硅酸钠和水,反应的化学方程式为:;
(2)见答案;
(3)根据曲线图可知,焙烧温度是1050℃时,脱硅率最高,因此最佳焙烧温度是1050℃。
选项
做法
原理
A
用木柴生火
木柴是可燃物
B
用废纸引燃木柴
使温度达到木柴着火点
C
将木柴架空摆放
有利于空气流通
D
对灶膛扇风
降温,防止煮焦米饭
选项
实验目的
操作
A
除去CO2中混有的HCl
通过足量NaOH溶液
B
除去CuO中的Cu
加入过量稀盐酸,过滤
C
鉴别BaCl2溶液与CaCl2溶液
加入适量Na2CO3溶液
D
鉴别NaOH固体与NH4NO3固体
分别加水溶解,用温度计测量温度变化
溶液
a
b
c
a
—
有沉淀产生
有气体产生
b
有沉淀产生
—
无明显现象
c
有气体产生
无明显现象
—
实验序号
操作
现象
结论
Ⅰ
取少量反应后的溶液于试管中,加入CuCl2溶液
无明显现象
猜想___________不成立
Ⅱ
取少量反应后的溶液于另一支试管中,加入硝酸银溶液
有___________产生
猜想一成立
相关试卷
这是一份广东省大湾区2025年初中学业水平质量监测卷一化学试题(解析版),共18页。试卷主要包含了考生必须保持答题卡的整洁,可能用到的相对原子质量, 氢化钛作为储氢材料备受关注等内容,欢迎下载使用。
这是一份广东省大湾区2026年初中学业水平质量监测卷化学试卷附答案,共24页。试卷主要包含了选择题,非选择题,【科普阅读】,【基础实验和跨学科实践】,【科学探究】等内容,欢迎下载使用。
这是一份2025年广东省大湾区教育研究院初中学业水平模拟测试化学试题(解析版)-A4,共18页。试卷主要包含了选择题,非选择题等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 




.png)




