






高中化学人教版 (新课标)选修4 化学反应原理第二章 化学反应速率和化学平衡第二节 影响化学反应速率的因素教案配套ppt课件
展开 这是一份高中化学人教版 (新课标)选修4 化学反应原理第二章 化学反应速率和化学平衡第二节 影响化学反应速率的因素教案配套ppt课件,共21页。PPT课件主要包含了保鲜的冷冻蔬菜,没合适的取向,没足够的能量,体积减小,压强增大,浓度增大,体积增大,浓度减小,压强减小,体积变化等内容,欢迎下载使用。
生活小常识 食物变质之谜
内因 参加反应物质的性质 (主要因素)
外因 浓度、压强、温度、催化剂
其他因素:光、颗粒大小、溶剂等
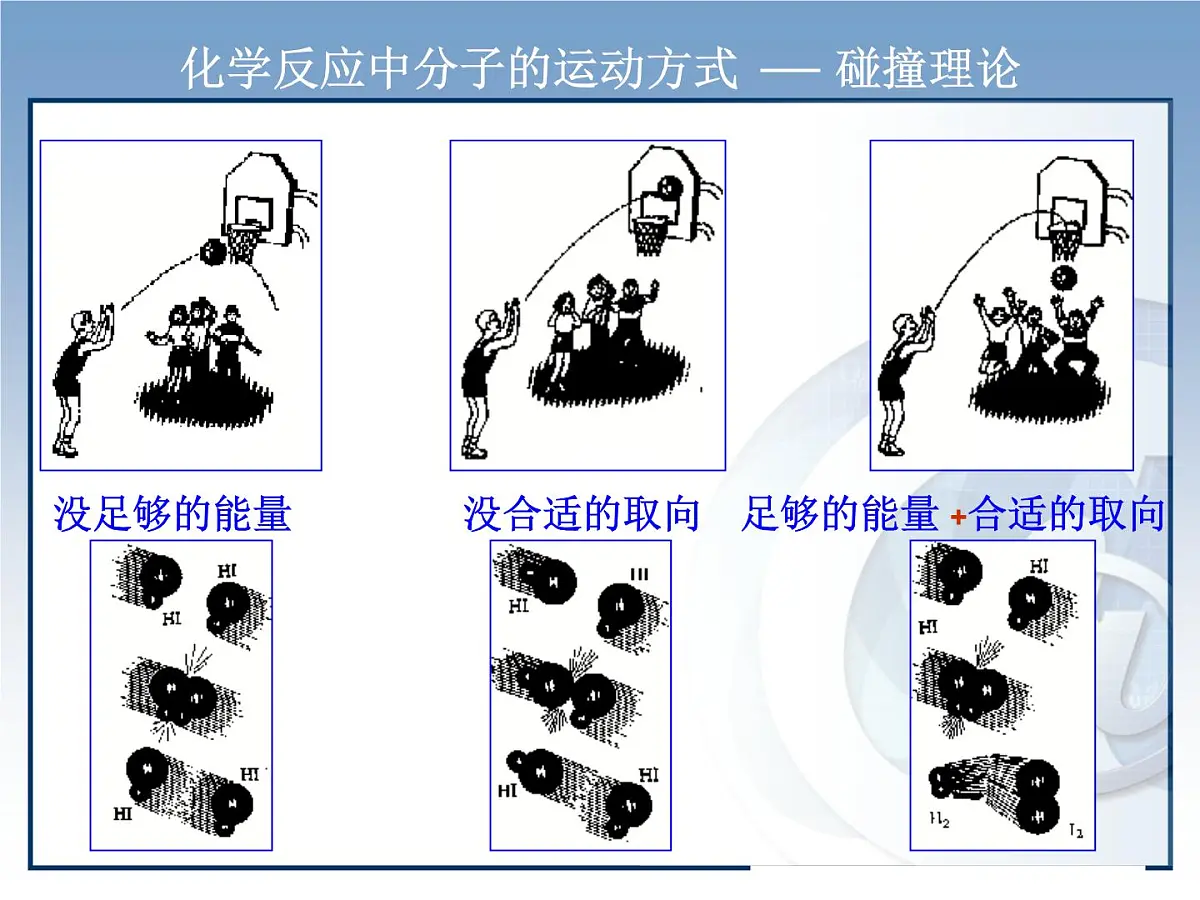
化学反应中分子的运动方式 碰撞理论
足够的能量 +合适的取向
有效碰撞: 能够发生化学反应的碰撞。
活化分子:能够发生有效碰撞的分子。
化学反应速率主要取决于有效碰撞的几率。
实验原理
实验目的 根据稀硫酸和不同浓度的硫代硫酸钠反应出现黄色浑浊物的时间来判断浓度对反应速率的影响
Na2S2O3 + H2SO4 == Na2SO4 + SO2 + S +H2O
实验结论 浓度高的硫代硫酸钠中首先出现黄色浑浊物
当反应物的浓度增大时,单位体积内的分子数增多,活化分子数也相应的增多,有效碰撞率提高,反应速率也必然增大。
其他条件不变时,增大反应物的浓度,可以增大反应速率;减小反应物的浓度,可以减小化学反应的速率。
a、此规律只适用于气体或溶液的反应,对于纯固体或液体的反应物,一般情况下其浓度是常数,因此改变它们的量一般不会改变化学反应速率。
b、随着化学反应的进行,反应物的浓度会逐渐减小,因此一般反应速率也会逐渐减小。
在反应中保持体系容积不变,充入He,反应的速率怎么变?
在反应中保持体系压强不变,充入He,反应的速率怎么变?
压强的改变对反应速率的影响,需看是否造成浓度的改变,当然不讲改变压强的原因时默认为体积的变化
应用1:一定条件下,在CaCO3(块状)+2HCl=CaCl2+H2O+CO2反应中,为了加快反应的速率,下列那些方法可行:A、增加HCl的浓度 B、加水 C、增加同浓度盐酸的量 D、改加CaCO3粉末
应用2:如反应:3KSCN+FeCl3 Fe(SCN)3+3KCl若在上述反应体系中加入KCl固体,会不会影响化学反应速率?
实验2-3结论:温度高的溶液先出现浑浊
Na2S2O3+H2SO4=Na2SO4+SO2+S↓+H2O
【结论】其他条件不变,温度升高,反应速率加快
→普通分子变为活化分子
2、一般说来,温度每升高10℃,速率增加2-4倍。
(1)温度对反应速率影响的规律,对吸热反应,放热反应都适用。(2)反应若是可逆反应,升高温度,正、逆反应速率都加快,降低温度,正、逆反应速率都减小。
催化剂对反应速率的影响
实验2-4结论:加入催化剂可以加快反应的速率
使用催化剂,能够降低反应所需的能量,这样会使更多的反应物的分子成为活化分子,大大增加单位体积内反应物分子中活化分子所占的百分数。因而使反应速率加快。
【结论】能改变化学反应速率而自身的化学组成和质量在反应前后保持不变
1)同一催化剂能同等程度的改变化学反应的速率。2)催化剂只能改变反应速率,不能将不反应变成反应3)催化剂有一定的选择性和活化温度:4)催化剂中毒:催化剂的活性往往因接触少量杂质而明显下降,甚至遭到破坏,这种现象叫催化剂中毒。催化剂中毒会严重影响反应的顺利进行。工业上为了防止催化剂中毒,要把原料进行净化除去毒物。
下列条件的变化,是因为降低反应所需的能量而增加单位体积内的反应物活化分子百分数致使反应速率加快的是( ) A、增大浓度 B、增大压强 C、升高温度 D、使用催化剂
对于反应N2+O2=2NO在密闭容器中进行,下列条件哪些不能加快该反应的化学反应速率( ) A、缩小体积使压强增大 B、体积不变充入 N2 使压强增大C、体积不变充入 O2使压强增大 D、使体积增大到原来的2倍E、体积不变充入氦气使压强增大
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 

.png)




