

所属成套资源:全套人教版高中化学必修第一册复习提升练+专题强化练+综合拔高练含答案
人教版高中化学必修第一册第二章海水中的重要元素——钠和氯实验整合练钠、氯及其化合物的实验探究含答案
展开
这是一份人教版高中化学必修第一册第二章海水中的重要元素——钠和氯实验整合练钠、氯及其化合物的实验探究含答案,共16页。
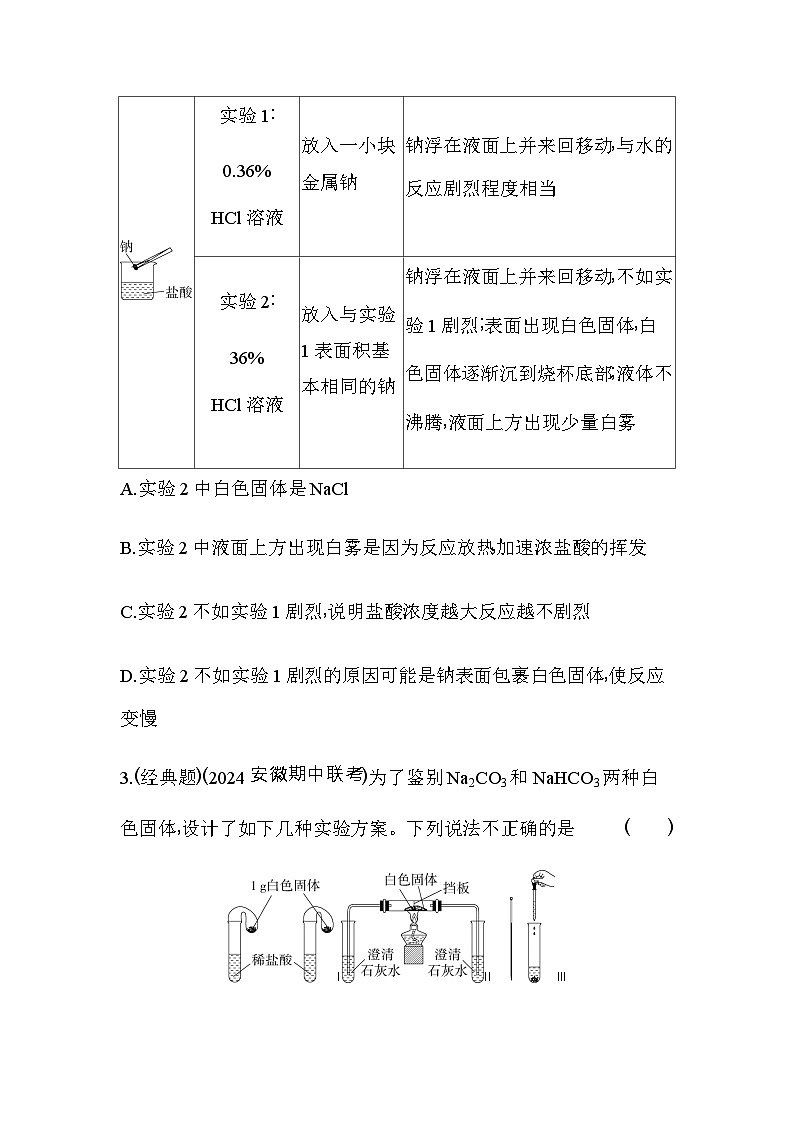
实验整合练 钠、氯及其化合物的实验探究实验1 钠及其化合物的实验探究1.(2024山东青岛期中)NaH是有机合成中用途很广泛的物质。已知:NaH遇水蒸气剧烈反应。某小组设计如图实验装置制备NaH,下列说法错误的是 ( )安全漏斗的作用是“液封” B.装置A中的试剂是稀硫酸和粗锌C.装置B中的试剂是浓硫酸D.实验开始后先点燃C处酒精灯,再启动A中反应2.(2024北京十一中期中)某小组同学探究金属Na与不同浓度的盐酸反应,进行下列实验。下列说法不正确的是 ( )A.实验2中白色固体是NaClB.实验2中液面上方出现白雾是因为反应放热,加速浓盐酸的挥发C.实验2不如实验1剧烈,说明盐酸浓度越大反应越不剧烈D.实验2不如实验1剧烈的原因可能是钠表面包裹白色固体,使反应变慢3.(经典题)(2024安徽期中联考)为了鉴别Na2CO3和NaHCO3两种白色固体,设计了如下几种实验方案。下列说法不正确的是 ( )ⅠⅡ ⅢA.装置Ⅰ中的Na2CO3和NaHCO3均能与盐酸反应,产生气体速率快的是NaHCO3B.当稀盐酸足量时,装置Ⅰ中气球鼓起体积较小的是NaHCO3C.加热装置Ⅱ,澄清石灰水变浑浊一侧的白色固体是NaHCO3D.使用装置Ⅲ,在相同条件下分别配制Na2CO3和NaHCO3溶液并立刻测量溶液温度,也能鉴别这两种白色固体4.(2024山东泰安新泰一中质量检测)化学物质丰富多彩,化学反应千变万化,而常见物质之间的反应往往“隐藏着某些反应机理”。学校化学兴趣小组对过氧化钠参与的某些反应进行了初步探究。该小组设计如图实验装置,验证“二氧化碳与水接触时才能和过氧化钠反应”。步骤1:打开活塞K2,关闭K1,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。步骤2:打开活塞K1,关闭K2,打开分液漏斗活塞加入盐酸,将带火星的木条放在a处。请回答下列问题:(1)装置①中反应的化学方程式是 。 (2)装置②中盛放的试剂是 ,该试剂的作用是 ;③中的试剂是 。 (3)本实验预期现象是 。 (4)有同学提出质疑,认为上述实验即使观察到木条复燃,也不能证明有水存在时,是过氧化钠与二氧化碳发生了化学反应,其理由是 。 (5)本小组还进一步探究了Na2O2与H2O的反应,实验如下:下列有关说法不正确的是 (填字母)。 A.实验ⅰ中发生反应的化学方程式为2Na2O2+2H2O 4NaOH+O2↑B.实验ⅲ中MnO2是H2O2分解反应的催化剂C.本实验可以说明Na2O2与H2O反应过程中有H2O2生成D.本实验可以说明使酚酞试液褪色的是O2实验2 氯及其化合物的实验探究5.(2024福建宁德一中月考)84消毒液的主要成分是NaCl和NaClO。已知:酸性条件下,84消毒液中的NaCl和NaClO会反应生成氯气。实验小组同学围绕“84消毒液能否与医用酒精发生反应”这一问题进行了如下实验。下列推理不合理的是 ( )A.由①②可知,①中产生的大量气泡与酒精挥发无关B.由①③可知,①中刺激性气味的产生可能与酒精无关C.由①②③可推断,84消毒液与医用酒精混合后,溶液中发生了化学反应D.由①④可推断,酸性条件有利于84消毒液与医用酒精发生反应6.(2024江苏南菁高级中学月考)利用NaClO氧化尿素[CO(NH2)2]制备N2H4·H2O(水合肼)的实验流程如图所示:已知:①Cl2与烧碱溶液的反应是放热反应;②N2H4·H2O有强还原性,能与NaClO剧烈反应生成N2。下列说法不正确的是 ( )A.步骤Ⅰ中为避免温度过高,可采用冰水浴B.步骤Ⅰ制备NaClO溶液时,测得产物中NaClO与NaClO3的物质的量之比为5∶1,则参与反应的氧化剂与还原剂的物质的量之比为5∶3C.步骤Ⅱ中可将尿素水溶液逐滴滴入NaClO碱性溶液中D.生成水合肼反应的离子方程式为ClO-+CO(NH2)2+2OH- Cl-+N2H4·H2O+CO32−7.(经典题)(2024福建泉州七中期中)化学是一门以实验为基础的学科,物质的检验鉴别、生产制备都可通过合适的实验方案实现。(1)纯净干燥的氯气与熔融金属锡反应可制备SnCl4,实验装置如图所示。已知:ⅰ.金属锡熔点为231 ℃,化学活泼性与铁相似;ⅱ.SnCl4的沸点为114 ℃,且易与水反应。回答下列问题:①装置Ⅰ中反应的离子方程式为 ,装置Ⅳ中发生反应的化学方程式为 。 ②装置Ⅱ中的试剂是 ;装置Ⅴ的作用是 。 ③装置Ⅵ最好选用下列装置中的 (填标号)。 A BC④为了顺利完成实验,点燃酒精灯的正确操作是 (填字母)。 A.先点燃Ⅰ处酒精灯,后点燃Ⅳ处酒精灯B.先点燃Ⅳ处酒精灯,后点燃Ⅰ处酒精灯C.同时点燃Ⅰ、Ⅳ两处酒精灯(2)某同学探究不同条件下Cl2与正二价锰化合物的反应,实验装置如图所示:查阅资料显示:a.Mn2+在一定条件下能被Cl2或ClO-氧化成MnO2(棕黑色)、MnO42−(绿色)、MnO4−(紫色)。b.浓碱条件下,MnO4−可被OH−还原为MnO42−。c.Cl2的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。①通入Cl2前,Ⅱ、Ⅲ中白色沉淀Mn(OH)2变为棕黑色沉淀MnO2。②对比实验Ⅰ、Ⅱ通入Cl2后的实验现象,对于Mn2+还原性与溶液酸碱性的认识是 。 ③据资料b,Ⅲ中应得到绿色溶液,而实验中得到紫色溶液,分析现象与资料不符的原因:原因一:可能是通入Cl2导致溶液的碱性减弱。原因二:可能是氧化剂过量,氧化剂将MnO42−氧化为MnO4−。ⅰ.用化学方程式表示可能导致溶液碱性减弱的原因: 。 ⅱ.取Ⅲ中放置后的1 mL悬浊液,加入4 mL 40% NaOH溶液,观察到溶液紫色迅速变为绿色,且有无色无味气体产生,该气体的化学式为 ;同时还可观察到溶液的绿色缓慢加深,即可证明Ⅲ的悬浊液中氧化剂过量。 答案与分层梯度式解析1.D 装置分析:加入液体后,部分液体存于安全漏斗上部弯管中起液封作用,避免氢气从漏斗中逸出,A正确;装置A中稀硫酸与粗锌反应生成氢气,用于后续与Na的反应,B正确;B是干燥氢气的装置,装置B中试剂为浓硫酸,C正确;先启动A中反应,利用生成的氢气将装置中的空气排出,防止钠与氧气反应,然后点燃C处酒精灯(易错点),D错误。2.C 钠和HCl反应生成氯化钠和氢气,氯化钠在浓度较大的盐酸中溶解度降低,所以实验2中钠表面出现NaCl白色固体,A正确;钠和盐酸反应放热,实验2中液面上方出现白雾是因为反应放热,加速浓盐酸的挥发,B正确;实验2不如实验1剧烈的原因是钠表面包裹白色固体,使钠与盐酸接触面积减小,反应变慢,C不正确,D正确。3.B Na2CO3和NaHCO3均能与盐酸反应生成CO2,盛放NaHCO3的气球鼓起更快,说明NaHCO3与盐酸反应速率更快,A正确;盐酸足量、固体质量相等时,n(Na2CO3)





