






人教版 (2019)必修 第一册第一节 物质的分类及转化备课ppt课件
展开通过对化学物质按组成和性质进行分类法的学习,进一步掌握酸、碱、盐、氧化物的概念及主要性质,会预测在一定条件下某种物质能发生的化学变化。
请你描述!下列的美丽景象是发生了什么变化?
美丽的溶洞、美丽的凤仙花,自然界中物质的转化
美丽的化学实验中物质的转化
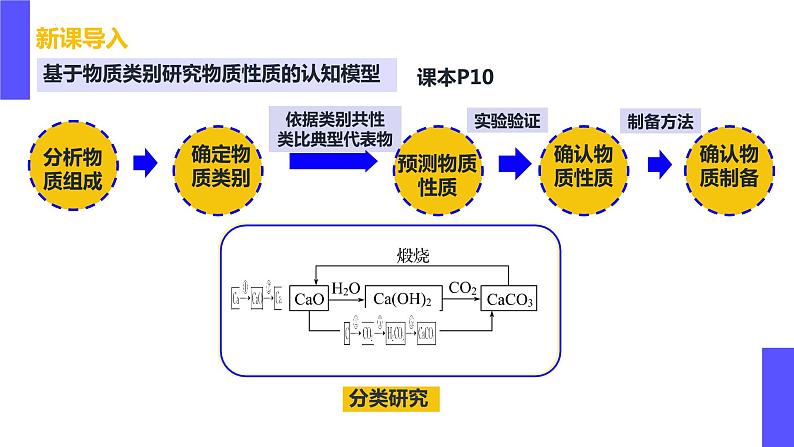
物质制备模型和转化关系图
你知道吗?下列诗句中涉及了哪些化学物质和类别?
依据类别共性类比典型代表物
基于物质类别研究物质性质的认知模型
请你思考! 请思考如何制备Na2SO3?
资料:亚硫酸钠(Na2SO3)常用作织物的漂白剂,在食品工业上也是常见的疏松剂和抗氧化剂。但Na2SO3在空气中容易氧化,因此自然界中几乎没有稳定存在的Na2SO3,只能通过制备来获得。
这些物质都可以制备Na2SO3吗?
NaClNa2CO3 K2SO3 K2SO4
基于物质类别研究物质性质
1.基于物质类别研究单质的性质
金属+氧气→金属氧化物
金属 + 酸 → 盐 + 氢气
金属 + 盐 → 新盐 + 新金属
非金属+氧气→非金属氧化物
类推S和O2反应的方程式
如何类推SO2和Na2O的性质?
2.基于物质类别研究氧化物的性质
酸性氧化物 + 水 → 酸
酸性氧化物 + 碱 → 盐 + 水
碱性氧化物 + 水 → 碱
碱性氧化物 + 酸 → 盐 + 水
酸性氧化物+碱性氧化物→盐
CO2 + 2NaOH Na2CO3 + H2O
SO2 + 2NaOH Na2SO3 + H2O
CaO + 2HCl CaCl2 + H2O
Fe2O3 + 6HCl 2FeCl3 + 3H2O
Na2O + 2HCl 2NaCl + H2O
凡能与酸反应生成盐和水的氧化物
凡能与碱反应生成盐和水的氧化物
类推SO2和Na2O的部分性质
【例1】预测陌生物质的性质——如何吸收烟气中的SO2?
请你思考! 如何认识H2SO3的性质?请同学们完成P10思考与讨论。
3.基于物质类别研究酸的性质
2HCl +Fe = FeCl2 +H2↑
使紫色石蕊试液变红色,无色酚酞试液不变色
CaO+2HCl===CaCl2+H2O
HCl +NaOH = NaCl +H2O
Na2CO3+2HCl===2NaCl+CO2↑+H2O
酸+碱性氧化物→盐+水
酸溶液能使指示剂变色
4.基于物质类别研究碱的性质
使紫色石蕊试液变蓝色,无色酚酞试液变红色
Ca(OH)2+ H2SO4=CaSO4↓+2H2O
CO2+2NaOH =Na2CO3+H2O
2NaOH+CuSO4 =Cu(OH)2 ↓+Na2SO4
碱+酸性氧化物→盐+水
5.基于物质类别研究盐的性质
Fe +CuSO4 =Cu+FeSO4
CaCO3+2HCl=CaCl2+H2O+CO2↑
2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
NaCl+AgNO3=AgCl↓+NaNO3
盐 + 金属→ 新盐 + 新金属
盐 + 酸→ 新盐 + 新酸
盐 + 碱→ 新盐 + 新碱
盐 + 盐→ 新盐 + 新盐
(1)请推断它们的化学式分别为:①_______;②______;③_____;④_____;⑤_________。(2)写出下列序号之间的化学方程式:①和②:_______________________________________;②和④:_______________________________________;②和⑤:________________________________________;③和④:_________________________________________。
【例2】在稀硫酸、二氧化碳、铜片、食盐、生石灰、一氧化碳、纯碱、铁片和木炭粉9种物质间存在下面的相互关系,选择①~⑤中适当的物质,使有连线的两物质能发生反应。
Fe+H2SO4===FeSO4+H2↑
CaO+H2SO4===CaSO4+H2O
Na2CO3+H2SO4===Na2SO4+CO2↑+H2O
CO2+CaO===CaCO3
请你思考! 根据物质的性质和分类,结合教材P11页“思考与讨论”请设计出将金属和非金属单质转化为盐的基本流程。
1.完成下列物质的转化,写出化学方程式:①_________________。②_____________________。③__________________________________。
2Ca+O2===2CaO
CaO+H2O===Ca(OH)2
Ca(OH)2+H2SO4===CaSO4↓+2H2O
④_______________。⑤___________________。⑥__________________________________。
CO2+H2O===H2CO3
Ca(OH)2+H2CO3===CaCO3↓+2H2O
2.物质转化的应用:物质制备方法的确定依据:物质的___________、物质之间的_________。
三、物质制备模型和转化关系图
1.不同类别物质之间的反应和转化关系图
2.设计以Na为原料制备Na2SO3的转化路径
请你思考!请你设计一个以Na为原料制备Na2SO3的转化路径。
请你思考!以硫、钠单质为例,归纳单质、氧化物、酸、碱、盐之间的转化关系。
⑦Na2O+H2SO4=Na2SO4+H2O
1.单质→盐的转化关系:
①4Na+O2=2Na2O
②Na2O+H2O=2NaOH
③2NaOH+CO2=Na2CO3+H2O
⑥SO3+H2O=H2SO4
箭头表示转化关系,连线表示相互反应。
2.八个相互反应的关系:
⑧2Na+S=Na2S
⑨Na2O+SO3=Na2SO4
⑩Na2O+H2SO4=Na2SO4+H2O
⑪2NaOH+SO3=Na2SO4+H2O
⑫2NaOH+H2SO4=Na2SO4+H2O
⑬2NaOH+CuSO4=Cu(OH)2↓+Na2SO4
⑭Na2CO3+H2SO4=Na2SO4+CO2↑+H2O
⑮Na2CO3+CuSO4=CuCO3↓+Na2SO4
【例3】单质、氧化物、酸、碱和盐的相互关系,可以用下图简单表示,限选择铁、碳、氧气、盐酸、氧化钙、二氧化碳、水、氢氧化钙8种物质作为反应物,将图中指定序号的转变用化学方程式表示(所写化学方程式不得重复)。
②___________________________________;③___________________________________;④___________________________________;⑤___________________________________;⑥___________________________________;⑦___________________________________。
CO2+Ca(OH)2===CaCO3↓+H2O
Fe+2HCl===FeCl2+H2↑
CaO+2HCl===CaCl2+H2O
Ca(OH)2+2HCl===CaCl2+2H2O
物理变化和化学变化的判断方法
指示剂、金属、金属氧化物、碱、盐
指示剂、酸性氧化物、酸、盐
金属单质、氧化物的性质
1.下列有关氧化物的判断正确的是( ) A.凡是含氧的化合物均可称为氧化物 B.依据性质不同氧化物只能分为酸性氧化物和碱性氧化物 C.酸性氧化物都能与碱反应生成盐和水 D.金属氧化物一定是碱性氧化物
2.下列物质中,与酸、碱、盐均能反应的物质是( )A.CuO B.CaCO3C.Na2CO3D.CO2
3.A、B、C、D、E中都含有同一种元素,它们之间的相互转化关系如图所示,其中所含的相同元素是 ( ) A.铜B.碳 C.铁 D.钙
高中化学人教版 (2019)必修 第一册第一节 物质的分类及转化备课ppt课件: 这是一份高中化学人教版 (2019)必修 第一册<a href="/hx/tb_c161971_t3/?tag_id=26" target="_blank">第一节 物质的分类及转化备课ppt课件</a>,共37页。PPT课件主要包含了素养目标,教学目标,新课导入,胶体的性质,分散系,分散系及其分类,胶体及其性质,胶体的制备和提纯,课堂思考,课堂探究等内容,欢迎下载使用。
高中人教版 (2019)第一章 物质及其变化第一节 物质的分类及转化教学课件ppt: 这是一份高中人教版 (2019)<a href="/hx/tb_c161971_t3/?tag_id=26" target="_blank">第一章 物质及其变化第一节 物质的分类及转化教学课件ppt</a>,共48页。PPT课件主要包含了素养目标,教学目标,新课导入,简单分类法及其应用,化学中常用的分类方法,同素异形体,课堂思考,分类的标准,课堂探究,分类方法等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第二节 离子反应公开课ppt课件: 这是一份高中化学人教版 (2019)必修 第一册<a href="/hx/tb_c161973_t3/?tag_id=26" target="_blank">第二节 离子反应公开课ppt课件</a>,共40页。PPT课件主要包含了素养目标,教学目标,新课导入,离子共存,离子的检验鉴别,离子反应的其他应用,课堂思考,课堂探究,CO32-,Ca2+等内容,欢迎下载使用。













