





还剩13页未读,
继续阅读
所属成套资源:全套鲁科版高中化学必修第一册课时课件
成套系列资料,整套一键下载
鲁科版高中化学必修第一册专题6制备及探究实验课件
展开
这是一份鲁科版高中化学必修第一册专题6制备及探究实验课件,共21页。
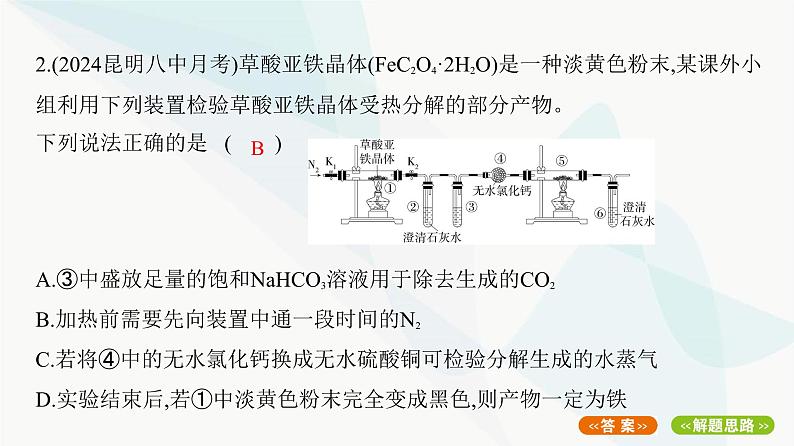
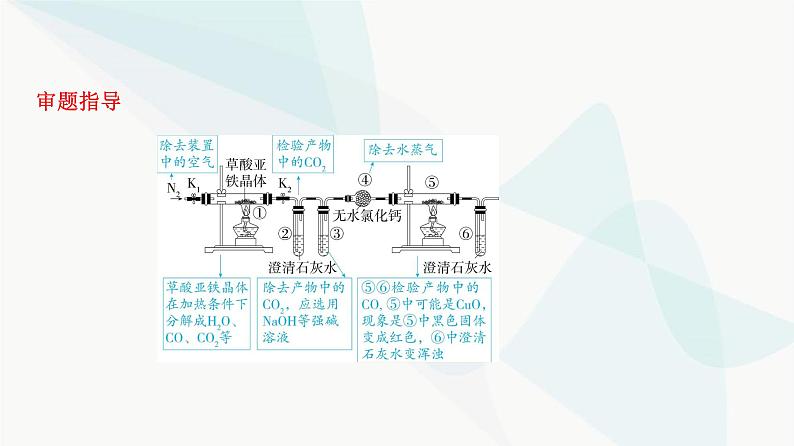
C审题指导 该实验的目的是探究SO2与BaCl2溶液反应生成沉淀的条件,根据 “强酸制弱酸”原理,若SO2与BaCl2溶液直接混合,不能得到BaSO3沉淀,若溶液 呈碱性,SO2转化为S ,可得到BaSO3沉淀,若通入氧化性气体,将SO2氧化为S ,可得到BaSO4沉淀。解题思路 根据审题指导可知,e、f两管中的试剂可以分别是KMnO4固体和浓 盐酸,反应产生氯气,Cl2将SO2氧化为S ,产生BaSO4沉淀,故A正确;e、f两管中的试剂可以分别是NaOH固体和浓氨水,产生氨气,可以得到BaSO3沉淀,故B正 确;若e、f两管物质混合产生NH3,氨气极易溶于水,d导管直接插入BaCl2溶液中 易引起倒吸,故C错误;玻璃管的作用是连通大气,平衡压强,以便左右两边产生的 气体顺利导入,也可连接尾气处理装置,故D正确。A.③中盛放足量的饱和NaHCO3溶液用于除去生成的CO2B.加热前需要先向装置中通一段时间的N2C.若将④中的无水氯化钙换成无水硫酸铜可检验分解生成的水蒸气D.实验结束后,若①中淡黄色粉末完全变成黑色,则产物一定为铁2.(2024昆明八中月考)草酸亚铁晶体(FeC2O4·2H2O)是一种淡黄色粉末,某课外小 组利用下列装置检验草酸亚铁晶体受热分解的部分产物。下列说法正确的是 ( )B解题思路 碳酸氢钠不和二氧化碳反应,A错误;实验开始前必须先通入一段时 间的N2,除去装置中的空气,防止干扰实验,B正确;从②、③溶液中导出的气体会 带出水蒸气,④中放置无水硫酸铜无法检验分解生成的水蒸气,C错误;①中淡黄 色粉末完全变为黑色,产物可能是Fe、FeO或Fe3O4,D错误。AA.KClO3发生氧化反应 B.反应过程中需持续通入N2C.乙装置应置于冰水浴中 D.丙装置用于吸收ClO2尾气解题思路 甲装置用来制备ClO2,根据反应原理,KClO3作为氧化剂,发生还原反 应,A错误;ClO2体积分数大于10%时可能发生爆炸,所以需要持续通入氮气稀释 ClO2,B正确;乙装置用水吸收ClO2得到其水溶液,ClO2水溶液在温度过高时可能 发生爆炸,乙装置应置于冰水浴中,C正确;丙装置用于吸收ClO2尾气,防止污染空 气,D正确。4.(2024福州期末)硫酰氯(SO2Cl2)常用于制造医药品、染料等,某实验小组拟用 干燥的氯气和二氧化硫在活性炭催化下制取硫酰氯,装置如图所示: 已知:SO2Cl2的沸点为69 ℃,遇水能发生剧烈反应并产生白雾。下列说法错误的是 ( )A.装置①中,为了提高浓盐酸的利用率,可控制分液漏斗缓慢逐滴滴加B.装置②中试剂是饱和食盐水,装置③中试剂是浓硫酸C.装置④需要热水浴,控制温度超过69 ℃,装置⑤需要冰水浴D.“尾气处理”时需在装置⑤后接装有氢氧化钠溶液的洗气瓶D审题指导 利用纯净干燥的氯气和二氧化硫反应制取硫酰氯,由实验装置可知,装置①中制备氯气,装置②中除去氯气中的氯化氢,装置③中干燥氯气,装置④中制备SO2Cl2,装置⑤中收集SO2Cl2,最后尾气处理。解题思路 装置①中,可控制分液漏斗缓慢逐滴滴加浓盐酸,以便控制反应速 率,提高原料利用率,A正确;生成的氯气中含有氯化氢和水蒸气,装置②中试剂 是饱和食盐水,装置③中试剂是浓硫酸,B正确;SO2Cl2的沸点为69 ℃,装置④需要 热水浴,控制温度超过69 ℃,使生成的硫酰氯进入装置⑤中,其中装置⑤需要冰 水浴,收集产品,C正确;为吸收尾气氯气和二氧化硫,同时防止水蒸气进入装置⑤ 中,“尾气处理”时需在装置⑤后接装有碱石灰的干燥管,D错误。B解题思路 KMnO4与浓盐酸反应的化学方程式为2KMnO4+16HCl(浓) 2KCl+5Cl2↑+2MnCl2+8H2O,A正确;氯气能与碱石灰反应,c中无水氯化钙不能用 碱石灰代替,B错误;干燥的Cl2不能使品红试纸褪色,加水,Cl2和水反应产生的次 氯酸能使品红试纸褪色,C正确;注射器在实验中除了向f中加水外,还可以向上 拉活塞,储存尾气,防止污染,D正确。6.(15分)(2024广东肇庆期末)研究铁及其化合物的性质与转化关系是中学化学 重要的学习内容。回答下列问题:(1)人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血。市场出售的某种麦片 中含有微量、颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是HCl)作用 下转化成亚铁盐。写出该反应的离子方程式: 。(2)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业上常 用向NaClO和NaOH混合溶液中滴加Fe(NO3)3溶液的方法制备Na2FeO4,反应中氧 化剂与还原剂的物质的量之比为 ,制备1 mol Na2FeO4转移的电子数目为 。(3)某兴趣小组通过下列实验探究Fe2+、Fe3+的性质。已知:Fe2+可与K3[Fe(CN)6]溶液反应生成蓝色沉淀。①甲组同学得出结论“Cl2可将Fe2+氧化”,其反应的离子方程式为 ;同学们认为甲组实验不够严谨,改进了实验:用煮沸冷却后的水配 制溶液,向2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入几滴氯水 和1滴KSCN溶液,溶液变红,证明了结论正确,煮沸的作用是 。②其他组同学认为乙组的实验同样不够严谨,可能是 使 溶液紫色褪去。请设计补充实验:取a溶液少许,滴加 ,若出现 ,则结论正确。答案 (除标注外,每空2分)(1)Fe+2H+ Fe2++H2↑(1分)(2)3∶2 3×6.02×1023(或1.806×1024)(3)①Cl2+2Fe2+ 2Fe3++2Cl- 除去水中的溶解氧②维生素C过量,与高锰酸钾反应 K3[Fe(CN)6]溶液(或氢氧化钠溶液) 蓝色沉 淀(或白色沉淀变为灰绿色,最终变为红褐色,合理即可,与前一空对应)K3[Fe(CN)6]溶液(或氢氧化钠溶液),出现蓝色沉淀(或白色沉淀变为灰绿色,最终 变为红褐色),证明结论正确。
C审题指导 该实验的目的是探究SO2与BaCl2溶液反应生成沉淀的条件,根据 “强酸制弱酸”原理,若SO2与BaCl2溶液直接混合,不能得到BaSO3沉淀,若溶液 呈碱性,SO2转化为S ,可得到BaSO3沉淀,若通入氧化性气体,将SO2氧化为S ,可得到BaSO4沉淀。解题思路 根据审题指导可知,e、f两管中的试剂可以分别是KMnO4固体和浓 盐酸,反应产生氯气,Cl2将SO2氧化为S ,产生BaSO4沉淀,故A正确;e、f两管中的试剂可以分别是NaOH固体和浓氨水,产生氨气,可以得到BaSO3沉淀,故B正 确;若e、f两管物质混合产生NH3,氨气极易溶于水,d导管直接插入BaCl2溶液中 易引起倒吸,故C错误;玻璃管的作用是连通大气,平衡压强,以便左右两边产生的 气体顺利导入,也可连接尾气处理装置,故D正确。A.③中盛放足量的饱和NaHCO3溶液用于除去生成的CO2B.加热前需要先向装置中通一段时间的N2C.若将④中的无水氯化钙换成无水硫酸铜可检验分解生成的水蒸气D.实验结束后,若①中淡黄色粉末完全变成黑色,则产物一定为铁2.(2024昆明八中月考)草酸亚铁晶体(FeC2O4·2H2O)是一种淡黄色粉末,某课外小 组利用下列装置检验草酸亚铁晶体受热分解的部分产物。下列说法正确的是 ( )B解题思路 碳酸氢钠不和二氧化碳反应,A错误;实验开始前必须先通入一段时 间的N2,除去装置中的空气,防止干扰实验,B正确;从②、③溶液中导出的气体会 带出水蒸气,④中放置无水硫酸铜无法检验分解生成的水蒸气,C错误;①中淡黄 色粉末完全变为黑色,产物可能是Fe、FeO或Fe3O4,D错误。AA.KClO3发生氧化反应 B.反应过程中需持续通入N2C.乙装置应置于冰水浴中 D.丙装置用于吸收ClO2尾气解题思路 甲装置用来制备ClO2,根据反应原理,KClO3作为氧化剂,发生还原反 应,A错误;ClO2体积分数大于10%时可能发生爆炸,所以需要持续通入氮气稀释 ClO2,B正确;乙装置用水吸收ClO2得到其水溶液,ClO2水溶液在温度过高时可能 发生爆炸,乙装置应置于冰水浴中,C正确;丙装置用于吸收ClO2尾气,防止污染空 气,D正确。4.(2024福州期末)硫酰氯(SO2Cl2)常用于制造医药品、染料等,某实验小组拟用 干燥的氯气和二氧化硫在活性炭催化下制取硫酰氯,装置如图所示: 已知:SO2Cl2的沸点为69 ℃,遇水能发生剧烈反应并产生白雾。下列说法错误的是 ( )A.装置①中,为了提高浓盐酸的利用率,可控制分液漏斗缓慢逐滴滴加B.装置②中试剂是饱和食盐水,装置③中试剂是浓硫酸C.装置④需要热水浴,控制温度超过69 ℃,装置⑤需要冰水浴D.“尾气处理”时需在装置⑤后接装有氢氧化钠溶液的洗气瓶D审题指导 利用纯净干燥的氯气和二氧化硫反应制取硫酰氯,由实验装置可知,装置①中制备氯气,装置②中除去氯气中的氯化氢,装置③中干燥氯气,装置④中制备SO2Cl2,装置⑤中收集SO2Cl2,最后尾气处理。解题思路 装置①中,可控制分液漏斗缓慢逐滴滴加浓盐酸,以便控制反应速 率,提高原料利用率,A正确;生成的氯气中含有氯化氢和水蒸气,装置②中试剂 是饱和食盐水,装置③中试剂是浓硫酸,B正确;SO2Cl2的沸点为69 ℃,装置④需要 热水浴,控制温度超过69 ℃,使生成的硫酰氯进入装置⑤中,其中装置⑤需要冰 水浴,收集产品,C正确;为吸收尾气氯气和二氧化硫,同时防止水蒸气进入装置⑤ 中,“尾气处理”时需在装置⑤后接装有碱石灰的干燥管,D错误。B解题思路 KMnO4与浓盐酸反应的化学方程式为2KMnO4+16HCl(浓) 2KCl+5Cl2↑+2MnCl2+8H2O,A正确;氯气能与碱石灰反应,c中无水氯化钙不能用 碱石灰代替,B错误;干燥的Cl2不能使品红试纸褪色,加水,Cl2和水反应产生的次 氯酸能使品红试纸褪色,C正确;注射器在实验中除了向f中加水外,还可以向上 拉活塞,储存尾气,防止污染,D正确。6.(15分)(2024广东肇庆期末)研究铁及其化合物的性质与转化关系是中学化学 重要的学习内容。回答下列问题:(1)人体血液中如果缺乏亚铁离子,就会造成缺铁性贫血。市场出售的某种麦片 中含有微量、颗粒细小的还原铁粉,这些铁粉在人体胃酸(主要成分是HCl)作用 下转化成亚铁盐。写出该反应的离子方程式: 。(2)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂,主要用于饮用水处理,工业上常 用向NaClO和NaOH混合溶液中滴加Fe(NO3)3溶液的方法制备Na2FeO4,反应中氧 化剂与还原剂的物质的量之比为 ,制备1 mol Na2FeO4转移的电子数目为 。(3)某兴趣小组通过下列实验探究Fe2+、Fe3+的性质。已知:Fe2+可与K3[Fe(CN)6]溶液反应生成蓝色沉淀。①甲组同学得出结论“Cl2可将Fe2+氧化”,其反应的离子方程式为 ;同学们认为甲组实验不够严谨,改进了实验:用煮沸冷却后的水配 制溶液,向2 mL FeCl2溶液中先加入0.5 mL煤油,再于液面下依次加入几滴氯水 和1滴KSCN溶液,溶液变红,证明了结论正确,煮沸的作用是 。②其他组同学认为乙组的实验同样不够严谨,可能是 使 溶液紫色褪去。请设计补充实验:取a溶液少许,滴加 ,若出现 ,则结论正确。答案 (除标注外,每空2分)(1)Fe+2H+ Fe2++H2↑(1分)(2)3∶2 3×6.02×1023(或1.806×1024)(3)①Cl2+2Fe2+ 2Fe3++2Cl- 除去水中的溶解氧②维生素C过量,与高锰酸钾反应 K3[Fe(CN)6]溶液(或氢氧化钠溶液) 蓝色沉 淀(或白色沉淀变为灰绿色,最终变为红褐色,合理即可,与前一空对应)K3[Fe(CN)6]溶液(或氢氧化钠溶液),出现蓝色沉淀(或白色沉淀变为灰绿色,最终 变为红褐色),证明结论正确。
相关资料
更多









