









中职化学高教版(2021)医药卫生类第三节 烃的衍生物一等奖课件ppt
展开主题五 简单有机化合物及其应用 5.3 烃的衍生物
1. 了解烃的衍生物的结构特点和官能团。知道有机物的官能团与其性质有关,且基团间能够相互影响,进一步巩固结构决定性质的观念。2. 学会分析烃的衍生物发生反应的活性部位及原因,知道消去反应、酯化反应等有机反应的反应机理,进一步了解氧化、加成、取代等有机反应类型,知道有机化合物之间在一定条件下可以相互转化。3. 了解溴乙烷、乙醇、苯酚、乙醛、乙酸等烃的衍生物的主要性质及其在生产、生活中的重要应用。认识酒后驾车的危害并知道检测酒驾的原理及方法。
1842年,北爱尔兰爱丁堡大学的妇科专家辛普森(1811—1870)首次尝试使用仿作为麻醉药为患者进行手术并取得了功,但氯仿毒副作用较大,不适用于临。受到氯仿具有麻醉作用的启发,人类发了更多麻醉效果好、毒副作用小的卤代烃全身吸入性麻醉药,如氟烷(1,1,1-三氟-2-氯-2-溴乙烷)(图5-3-1)。你能写氯仿、氟烷的结构简式吗?这些化合物中除碳、氢两种元素外,还含有哪些元素?
烃分子中的氢原子被其他原子或原子团所取代,衍生出的一系列新的化合物称为烃的衍生物。烃的衍生物的性质取决于其所含的官能团。
烃分子中的氢原子被卤素原子取代所生成的化合物称为烃的卤素衍生物,简称为卤代烃,最简单的卤代烃是一卤代烷烃,其通式为CnH2n+1X(X=F、Cl、Br、I),溴乙烷是卤代烷烃的典型代表。
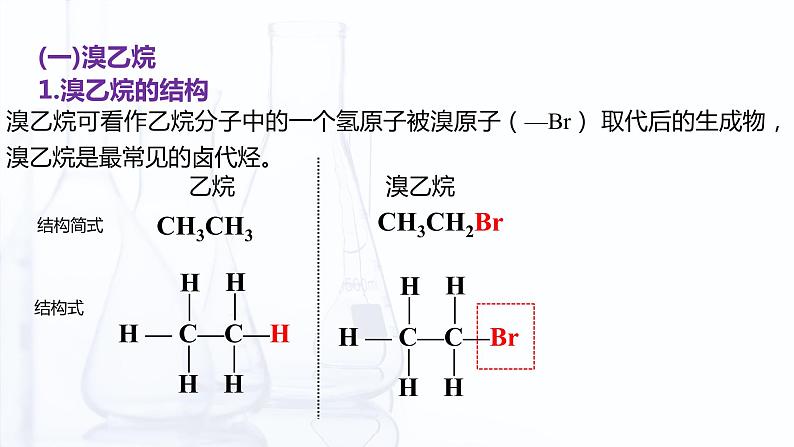
乙烷 溴乙烷
溴乙烷可看作乙烷分子中的一个氢原子被溴原子(—Br) 取代后的生成物,溴乙烷是最常见的卤代烃。
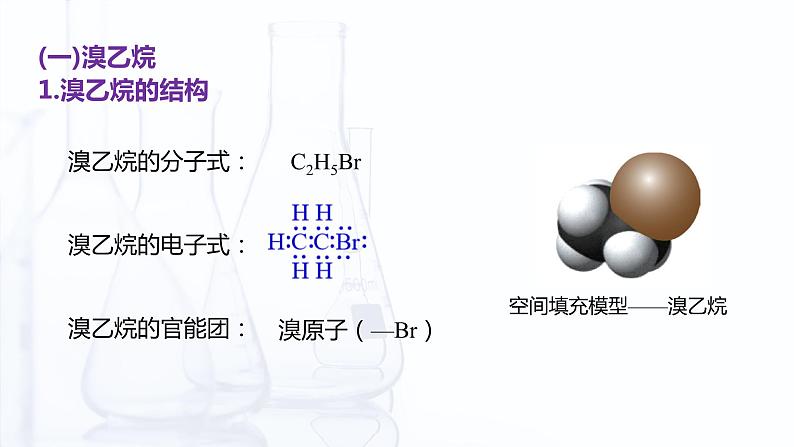
溴乙烷的分子式:溴乙烷的电子式:溴乙烷的官能团:
溴乙烷为无色、易挥发、有类似乙醚气味的油状液体,露置在空气中或见光后会逐渐变为黄色,沸点38.4℃,比水重,不溶于水,可与乙醇、乙醚、氯仿等有机溶剂混溶。
操作1:取两支试管(试管①、试管②)分别加入10~15滴溴乙烷,在试管①中加入 5 滴硝酸银溶液,振荡, 加热。在试管②中,加入1 mL 5%的氢氧化钠溶液,充分振荡,加热,静置。
实验探究1:溴乙烷的水解反应
操作2:待试管②中液体分层后,用滴管移取10滴上层水溶液,滴入另一洁净试管(试管③)中,加入1 mL稀硝酸再滴加数滴硝酸银溶液,观察比较现象。
思考:加稀HNO3酸化的目的是什么?加入NaOH溶液有何作用?
溴乙烷和氢氧化钠水溶液在加热条件下反应,有Br-产生,Br-+Ag+ AgBr↓(浅黄色)
溶液不再分层,有浅黄色沉淀生成
加HNO3酸化的目的是:中和过量的NaOH,防止生成Ag2O暗褐色沉淀,干扰淡黄色沉淀的现象,又影响AgBr的生成量;同时验证沉淀不溶于稀硝酸。NaOH溶液的作用是:中和水解后生成的HBr,降低生成物的浓度,使水解平衡向右移动。
溴乙烷与强碱的水溶液共热时会发生取代反应(又称为水解反应),溴乙烷转变为乙醇。
实验探究2:溴乙烷的消去反应
操作3:按照下图所示安装仪器。向大试管(试管④)中注入 5 mL溴乙烷和15 mL饱和氢氧化钾的乙醇溶液,加热,观察是否有气体放出? 若有,尝试采用排水法收集。操作4:取少量大试管中的反应剩余物放入另一试管(试管⑤)中,再向该试管中加入稀硝酸至溶液呈酸性,滴加硝酸银溶液,观察现象。
溴乙烷和氢氧化钾的乙醇溶液在加热条件下反应,有乙烯、Br-生成。
在一定条件下从一个有机化合物分子中脱去一个或几个小分子(如水、卤化氢)生成不饱和化合物(含双键或三键)的反应称为消去反应。卤代烃与强碱的乙醇溶液共热发生消去反应。规律:有水取代,有醇消去;水解制醇,消去制烯。
获得卤代烃的途径:取代反应、加成反应
1.定义:烃分子中的氢原子被卤素原子取代后所生成的化合物。
(X= F、Cl、Br、I)
【注意】只含C、X、H(不一定),不含其它原子。
(1)按卤素原子的种类分类
(2)按卤素原子的数目分类
与烷烃相似,即最长、最近、最简、最多、最小的命名原则。但不同点是主链必须含有官能团。 命名步骤:1.选主链,含官能团(卤素原子)2.定编号,近官能团(卤素原子)3.写名称,标官能团(卤素原子) 其它要求与烷烃相同!!!
以烃为母体,卤原子为取代基
从距简单官能团(卤素原子)近的一端编号
选择含官能团最长碳链作为主链
CH2Br—CH2Br
(三)卤代烃的物理性质
1.常温下,卤代烃中除个别为气体外,大多为液体或固体。2.卤代烃不溶于水,可溶于有机溶剂,某些卤代烃本身是很好的有机溶剂。3.卤代烃的密度和沸点都高于相应的烃。密度一般随着碳原子数目的增加而减小,沸点随碳原子数目的增加而升高。
4.一氟(R-F)和一氯(R-Cl)代(脂肪)烃:密度小于水 溴或碘代烃及多卤代烃: 密度大于水
(四)卤代烃在医药领域的应用
1.三氯甲烷三氯甲烷又称氯仿,是无色、稍带有甜味的易挥发液体,点为61.7 ℃,密度为1.483 kg/L,微溶于水,和很多有机溶剂互溶,氯仿是优良的有机溶剂。在医学上,氯仿有麻醉作用,但毒性较大,对人体心、肝、肾有损害而弃用。
2.四氯化碳四氢化碳是无色液体,沸点为76.8 ℃,密度为1.59 kg/L,能溶解脂肪、油漆、树脂、橡胶等物质,曾广泛用作溶剂、灭火剂、香料的浸出剂、纤维的脱脂剂、粮食的蒸煮剂、药物的萃取剂、织物的干洗剂等,但是由于其毒性及对臭氧层的破坏,现甚少使用并被限制生产。
3.氟烷氟烷的化学名称是1.1,1-三氟-2-氯-2-溴乙烷,又称三氟氯溴乙烷,是一种无色、易流动的重质液体,密度为1.87 kg/L,沸点为50.2 ℃。氟烷有类似氯仿的气味,味甜,不燃、不爆、微溶于水。氟烷有麻醉作用、诱导期短,苏醒快,是目前医学上常用的吸入性全身麻醉药之一。
1.乙醇的组成和结构 观察与认知
乙醇,俗称酒精,是酒的主要成分。杜甫《饮中八仙歌》曰:“李白斗酒诗百篇”。曹操《短歌行》有“何以解忧?唯有杜康。”那么,乙醇具有怎样的组成、结构和性质呢?
乙烷 乙醇
乙醇可以看作乙烷分子中的1个氢原子被羟基(—OH)取代后的生成物。
乙醇的分子式:乙醇的电子式:乙醇的官能团:乙醇的结构特点:
乙醇分子中的O—H键和C—O键都属于极性键,比较活泼。
乙醇是无色透明、易挥发、有特殊香味的液体。沸点为78.5℃,密度为0.789 g/cm3。易溶于水,能与水任意比例互溶,本身是重要的有机溶剂,能够溶解多种无机物和有机物。
实验探究1:乙醇、水与金属钠的反应
操作1:取2支干燥的试管,向一支试管(试管①)中加入3 mL无水乙醇,向另一支试管(试管②)中加入3 mL水。操作2:向试管①、②中分别放入一小块金属钠,收集生成的气体,验纯并点燃,在火焰上方罩一只干燥的烧杯,待烧杯内壁有液滴出现,倒转烧杯,向烧杯中加入少量澄清石灰水。
实验探究1:乙醇与金属钠、水与金属钠的反应
反应较平缓,速度较慢;钠沉在试管底部
反应剧烈,速度快;钠浮在水面上
金属钠与乙醇反应比较平稳,与水反应很剧烈。
2.乙醇的性质(1)乙醇与金属钠的反应
乙醇与金属钠反应时,乙醇分子中羟基上的氢原子被金属钠取代,生成乙醇钠(CH3CH2ONa),并放出氢气。此反应与水和钠的反应同属置换反应,但乙醇与钠的反应要缓慢得多。说明乙醇分子中羟基中的氢原子比水分子中的氢原子更难解离。
2.乙醇的性质(2)乙醇的氧化反应
乙醇在空气中燃烧火焰呈淡蓝色,并放出大量的热。是一种常用的清洁燃料。
在热的催化剂(Cu或Ag)存在下,乙醇蒸气能被空气氧化生成乙醛CH3CHO
实验探究2:乙醇的氧化反应
操作2:取1支干燥的试管,向试管中加入5滴0.1 ml/L K2Cr2O7溶液和2 ~ 3mL稀H2SO4溶液,摇匀;向试管中加入10滴乙醇,振摇,观察现象。
硫酸的作用:使重铬酸钾在酸性条件下生成绿色的硫酸铬;作为可逆反应平衡体系中的生成物阻止重铬酸钾转变为黄色的铬酸钾(K2CrO4),以防止对前一个反应颜色变化的干扰。
依据乙醇易被氧化剂氧化的原理设计的酒精检测仪被广泛用于交警检查司机是否酒后驾车。
2.乙醇的性质(3)乙醇的消去反应
操作1:如图所示安装仪器,圆底烧瓶中放入乙醇、浓硫酸、沸石,加热至170℃ 左右,观察现象。
实验探究3:乙醇的消去反应
乙醇在浓硫酸的作用下,加热到170 ℃时有无色气体逸出,该气体可使溴水和酸性高锰酸钾溶液褪色。同时,烧瓶中混合液颜色变黑。即生成了乙烯,且部分乙醇炭化。
浓硫酸的作用:催化剂、脱水剂。温度计水银球位置和作用:液面以下,指示反应温度。 碎瓷片或沸石的作用:防止暴沸。 溶液变黑的原因:乙醇被浓硫酸炭化。乙烯中可能混有的杂质:CO2和SO2
羟基与苯环直接相连的化合物叫做酚。酚分子中的羟基“—OH”称为酚羟基,酚羟基是酚的官能团。与同样含有羟基的醇类物质比较,具有怎样的联系和区别呢?
——羟基和苯环直接相连。
——羟基和脂肪烃基相连,或者和苯环的侧链相连。
1.苯酚的组成与结构 观察与认知
苯 苯酚
苯酚可以看作是苯分子里的1个氢原子被羟基取代后的生成物,是最简单的酚。
苯酚的分子式:苯酚的官能团:苯酚的结构特点:
苯环与羟基之间的相互作用使酚羟基在性质上与醇羟基有显著差异。
纯净的苯酚为无色、具有特殊气味的晶体,熔点43℃,沸点182℃。露置在空气中时易发生氧化而显不同程度的黄色至红色。常温下,苯酚微溶于水,当温度高于70 ℃时,能与水任意比例混溶。苯酚易溶于乙醇、乙醚等有机溶剂。苯酚有毒,能凝固蛋白质,具有杀菌作用。
2.苯酚的性质(1)苯酚的酸性
苯环使酚羟基上的氢更活泼,更容易解离出H+。苯酚的酸性比碳酸弱。
2.苯酚的性质(2)苯酚的取代反应
操作4:向1支盛有少量苯酚溶液的试管中,滴入适量浓溴水,振荡,观察实验现象。
一开始局部产生沉淀。振荡后沉淀消失,继续滴加浓溴水,最后能产生稳定的沉淀。
2.苯酚的性质(3)苯酚的氧化反应
苯酚在空气中或遇到氧化剂时,很容易被氧化,生成黄色的醌类化合物
2.苯酚的性质(4)苯酚与三氯化铁的显色反应
苯酚能与三氯化铁溶液作用产生紫色的有色化合物。这一反应非常灵敏,可用于检验苯酚的存在。
纯净的苯酚可制成洗涤剂和软膏,有杀菌和止痛作用。药皂中通常也掺入少量的苯酚。苯酚也是一种重要的有机合成原料,多用于制造酚醛塑料(俗称电木)、合成纤维(如锦纶)、炸药(如2,4,6-三硝基苯酚)、染料、农药(如植物生长调节剂2,4-D)、药品(如阿司匹林)等。
有些人喝酒时会出现脸红现象,这是因为酒精在人体内代谢的过程中会产生乙醛,乙醛是一种血管扩张剂。那么乙醛有哪些性质和应用呢?
乙醛的分子式:乙醛的结构简式:乙醛的结构式:
乙醛是无色、易挥发、有强烈刺激性气体的液体,易燃,沸点 20.8 ℃,密度 0.78 g/cm3 ;能与水、乙醇、乙醚等互溶。
2.乙醛的性质(1)乙醛的还原反应
醛的催化加氢反应,是还原反应
实验探究1:乙醛的银镜反应
操作1:取1支试管,加入 2 mL 2% (质量分数)的AgNO3溶液,然后边振荡试管,边逐滴加入 2%(质量分数)稀氨水,直到最初生成的沉淀恰好溶解为止,制得银氨溶液。操作2:向该溶液中滴加3滴乙醛,振荡后把试管放入热水浴里加热,等待片刻,观察试管内壁上有什么变化并填写表格。
试管内壁有光亮的银镜生成
2.乙醛的性质(2)乙醛的氧化反应
实验后,银镜用HNO3浸泡,再用水洗。
实验探究2:乙醛的费林反应
操作3:向洁净的试管中加入1 mL费林试剂A和1 mL费林试剂B溶液,振荡混匀;然后加入0.5 mL的乙醛,加热至沸。观察记录现象。
试管中有砖红色沉淀生成。
费林试剂由氢氧化钠、硫酸铜、酒石酸钾钠组成。乙醛与费林试剂反应,生成砖红色的氧化亚铜沉淀。费林反应也可用来检验醛基。可用新制氢氧化铜代替费林试剂。
醛基(-CHO)与烃基(或氢原子)相连构成的一类化合物,简写RCHO
CnH2n+1CHO(n≥0) 或 CnH2nO(n ≥1)
羰基碳原子连接一个氢原子构成
醛基 -CHO 或 OHC-不能写成-COH\HOC-
醛基碳的杂化类型sp2
在醛类中,甲醛是最简单的醛。甲醛又叫蚁醛,是一种无色、有强烈刺激性气味的气体,易溶于水。甲醛的用途非常广泛,它是一种重要的化工原料,能合成多种有机化合物;它的水溶液(又称福尔马林)具有杀菌、防腐性能,可用于消毒和制作生物标本。苯甲醛是最简单的芳香醛,俗称苦杏仁油,是一种有苦杏仁气味的无色液体。苯甲醛是制造染料、香料及药物的重要原料。
HCHO + [Ag(NH3)2]OH
自然界的许多植物中含有醛,其中有些具有特殊的香味,可作为植物香料使用。
乙酸是一种常见的、重要的羧酸,也是最早由自然界中得到的有机化合物之一,你知道乙酸俗称醋酸的原因吗?
乙酸的分子式:乙酸的结构简式:乙酸的结构式:乙酸的结构特点:
乙酸分子中的羧基由羰基和羟基直接相连而成。
纯净的乙酸是无色液体、有强烈刺激性酸味,沸点117.9 ℃,熔点16.6 ℃,当温度低于16.6 ℃时,就凝结成冰状的晶体,无水乙酸又称为冰醋酸。
操作1:取3支试管,分别加入1 mL0.1 ml/L盐酸、1 mL0.1 ml/L乙酸、1 mL稀苯酚溶液,用pH试纸分别检测溶液的pH。操作2:取3支试管,分别加入2 mL0.1 ml/L盐酸、2 mL0.1 ml/L乙酸、2 mL稀苯酚溶液,各放入一小粒锌粒,观察现象。操作3:取3支试管,分别加入2 mL0.1 ml/L盐酸、2 mL0.1 ml/L乙酸、2 mL稀苯酚溶液,各加入少许NaHCO3粉末,观察现象。
2.乙酸的性质(1)乙酸的酸性
pH:盐酸<乙酸<苯酚
有气泡生成速率:盐酸>乙酸>苯酚
盐酸、乙酸有气泡生成速率:盐酸>乙酸;苯酚无现象
2.乙酸的性质(2)乙酸与乙醇反应
羧酸与醇在浓硫酸存在下共热生成酯和水的反应,称为酯化反应。酯化反应是可逆反应。
操作1:在1支试管里加入3 mL乙醇,边摇动边慢慢滴加2 mL浓硫酸和2 mL乙酸,然后按图所示连接好装置。操作2:用酒精灯均匀地加热试管。操作3:数分钟后,将产生的蒸气经导管通至加有酚酞试液的饱和碳酸钠溶液液面上,观察实验现象。
实验探究2:乙酸的酯化反应
浅红色饱和碳酸钠溶液的液面上有一层无色透明的油状液体
浓硫酸的作用:催化剂兼脱水剂饱和碳酸钠溶液的作用:吸收乙醇、中和乙酸、降低乙酸乙酯的溶解度,便于分层。
1.对下列物质所属类别的判断中,不正确的是A.CH3COOH、醛B.CH3COOC2H5、酯C.CH3CH2OH、醇D.CH2ClCH3、卤代烃【答案】A
2.化学与生活密切相关,下列叙述中正确的是A.甘油属于油脂,常用于化妆品中B.甲醛是一种无色有刺激性气味的液体,可以配制福尔马林溶液C.医院用75%的酒精杀菌、消毒,75%是指质量分数D.苯酚又名石炭酸,有腐蚀性,可用于消毒【答案】D
3.乙醇和乙酸是两种常见的有机化合物,下列说法正确的是A.乙醇和乙酸均能与金属钠反应B.乙醇能发生氧化反应,而乙酸不能发生氧化反应C.乙醇和乙酸均能使紫色石蕊试液变红D.乙醇和乙酸的分子结构中均含有碳氧双键【答案】A
4.下列说法正确的是( )A.乙醛的分子式为CH3CHOB.乙醛的结构简式为CH3CHOC.乙醛是一种有刺激性气味的气体D.乙醛不溶于有机溶剂,也不溶于水【答案】B
5.实验室制备乙酸甲酯的装置如图所示。下列说法正确的是 A.b中导气管口应插入液面下B.将乙酸和甲醇的混合液加入浓硫酸中搅拌混合C.饱和碳酸钠溶液的作用为吸收甲醇、乙酸D.若用18O标记甲醇,则产物乙酸甲酯中不含18O【答案】C
业精一分汗禾滴,爱心一颗花万朵。
P137,1.2.3
化学农林牧渔类第三节 纤维素优质ppt课件: 这是一份化学农林牧渔类第三节 纤维素优质ppt课件,共19页。PPT课件主要包含了学习目标与核心素养,主要内容,纤维素,常见的磷脂,磷脂的应用,存在方式,组成与结构,常见的蜡脂,组成及结构,纤维素与淀粉的异同等内容,欢迎下载使用。
高教版(2021)农林牧渔类第一节 油脂精品ppt课件: 这是一份高教版(2021)农林牧渔类第一节 油脂精品ppt课件,共19页。PPT课件主要包含了学习目标与核心素养,主要内容,油脂的组成及结构,油脂的性质,油脂在生物体内的作用,物理性质,化学性质,二化学性质,课堂小结等内容,欢迎下载使用。
化学高教版(2021)第三节 烃的衍生物优质课件ppt: 这是一份化学高教版(2021)第三节 烃的衍生物优质课件ppt,共42页。PPT课件主要包含了学习目标与核心素养,主要内容,C6H6O,C2H4O,CH3CHO,CHO醛基,CH3COONa,结构式,官能团,-COOH等内容,欢迎下载使用。












