





人教版九年级下册课题2 溶解度第2课时巩固练习
展开二、合作探究,质疑解难
一、情景引入,导入新知
三、要点回放,夯实基础
四、课堂小结,点拨提升
五、目标检测,检查效果
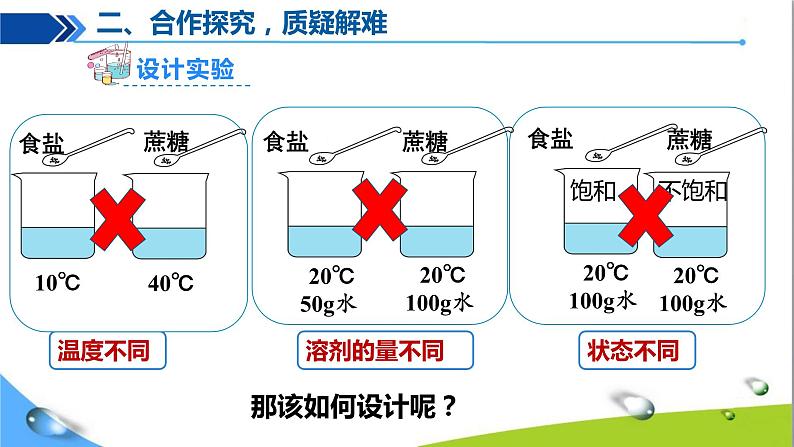
如何定量地比较食盐与蔗糖哪个的溶解能力更强呢?
能利用物质的溶解性设计物质分离的方案。
知道影响溶解度的因素,能利用气体溶解度解释生活中的有关现象。
在一定______下,某固态物质在_____溶剂里达到_____状态时所溶解的_____。用 表示。
阅读课本第35、36页,了解固体的溶解度及其含义。
在20℃时,氯化钠的溶解度是36g的意义?
在20℃时,100g水里最多能溶解氯化钠的质量是36g。
在20℃时,100g水里溶解36g的氯化钠就达到饱和状态。
下列说法对吗?如果不对,说明错在哪里。1.把31.6gKNO3 溶解在100g水里,恰好形成饱和溶液,所以KNO3的溶解度为31.6g。___________________________________________。2. 20℃时,把20gKNO3溶解在水里配制成饱和溶液,所以20℃时,KNO3的溶解度为20g。______________________________。
错误,未指明溶剂是100 g
3. 20℃时,20gKNO3能溶解在100g水里,所以20℃时,KNO3的溶解度为20g。_________________________________。4. 20℃时,把31.6gKNO3溶解在100g水里,恰好形成饱和溶液,所以20℃时,KNO3的溶解度为31.6。______________________________。
错误,未指明是饱和溶液
2.固体溶解度的四要素
在 100g 溶剂里(一般指水)
3.影响因素 (1)内部因素: 。 (2)外部因素:________。
1.例1 已知20℃时,KNO3的溶解度为31.6g。下列相关理解正确的是( ) A.100g水中溶解31.6 gKNO3固体达到饱和状态B.20℃时,100gKNO3溶液中溶解了31.6 gKNO3固体C.20℃时,100g水中最多能溶解31.6 gKNO3固体D.20℃时,31.6gKNO3固体溶于水形成饱和溶液
2.已知60℃时,硝酸钠的溶解度为124g。60℃时,向70g硝酸钠固体中加入50g水,充分搅拌后,所得溶液的质量是( ) A.100g B.112g C.124g D.120g
1.50℃时,氯化铵的溶解度约为50g,则50℃时氯化铵饱和溶液中溶质、溶剂、溶液的质量比约为 ( ) A.1∶2∶3 B.2∶3∶1 C.1∶1∶2 D.1∶3∶2
4. 溶解性与固体溶解度的关系
1.固体溶解度的表示方法:列表法和溶解度曲线。
用纵坐标表示溶解度,横坐标表示温度,根据下表中数据,在坐标图中绘制KNO3和NaCl的溶解度曲线并回答问题。
从你绘制的溶解度曲线中查出:NaCl在25 ℃和85 ℃时的溶解度分别约为________、________。
2.固体溶解度曲线纵坐标表示_________,用横坐标表示_______。意义:来表示固体物质的溶解度受_____变化影响。
该温度下两种物质的溶解度相同
2.结晶法提纯物质(适用于溶解度随温度变化趋势有差异的物质):
(1)点P表示_________________________。(2)t2℃时,A、B、C的溶解度由大到小为_______。(3)要使接近饱和的C的溶液变为饱和,需要_____温度。(4)t2℃时,向50g水中加入20gA,能否达到A的饱和溶液?加入30g?(5)t2℃时,A物质的饱和溶液150g降温到t1℃析出A____g。(6)t2℃时,将等质量A、B、C三种物质的饱和溶液降温到t1℃时,析出晶体的质量由大到小的顺序是________。(7)当A中含有少量B时,提纯A,可采用 方法。 当B中含有少量A时,提纯B,可采用 方法。
1.如图是固体A、B、C的溶解度曲线,回答问题:
t1℃时,A、C的溶解度相同
总结:提纯谁,就让谁结晶,陡用降温,平用蒸发。
气体的溶解度:某气体的______为101kPa和___________时,在________里达到___________时所溶解的气体体积。
打开可乐盖时有气体冒出
打开瓶塞,压强减小,CO2溶解性减弱,所以从水中逸出
温度升高CO2溶解性减弱,从体内逸出
温度升高O2溶解性减弱,鱼浮出水面呼吸
①压强:压强增大,气体溶解度变____。
②温度:温度升高,气体溶解度变____。
定义:在_________下,某固态物质在__________里达到__________时所溶解的_______,叫做这种物质在这种溶剂里的溶解度“S”表示。影响因素:内部:______和______的性质外部:_____。固体物质溶解度曲线: 陡升_________,缓升_________,下降__________。结晶方法: (陡升型)、 (缓升型)。
压强增大,气体溶解度变_____。
温度升高,气体溶解度变_____。
2.影响气体溶解度的因素:
增加溶质蒸发溶剂降低温度
溶解度数据表溶解度曲线
概念影响因素:溶质和溶剂本身的性质、 温度、压强
影响因素:溶质和溶剂本身的性质、 温度
1. 下列对“20 ℃时,硝酸钾溶解度为31.6 g”的理解,正确的是( )A.20 ℃时,31.6 g硝酸钾溶解在100 g水里B.20 ℃时,100 g溶液中含31.6 g硝酸钾C.31.6 g硝酸钾溶解在100 g水中达到饱和状态D.20 ℃时,31.6 g硝酸钾溶解在100 g水中恰好达到饱和状态
2. 20℃时,将5g固体R溶于50g水中,充分搅拌后,有0.5g固体未溶解,则20℃时固体R的溶解度为 ,属于 (选填“微溶““可溶”或“易溶”)物质。此温度下若要将1.8gR配制成饱和溶液,需要加水的质量是 。
3.(2023·连云港)NHCI和NaCl的溶解度曲线如图所示。下列说法中正确的是( )A.NH4Cl的溶解度比NaCl的大B.NH4CI的溶解度受温度的影响比NaCl的大C.20℃时 NH4CI的饱和溶液,升温到40℃时 仍是饱和溶液D.60℃时,在100g水中加入40gNaCl,形成不饱和溶液
4.如图是甲、乙两种物质的溶解度曲线,下列叙述正确的是( )A.20℃时,甲的溶解度大于乙的溶解度B.40℃时,甲、乙两种物质的溶解度相等C.采用降温的方法可以将乙的不饱和溶液转化为饱和溶液D.60℃时,在100g水中加入100g甲,充分溶解后溶液质量为200g
5. 据新闻报道,夏天经常有啤酒瓶自爆伤人的事件发生,其主要原因是( )A. 温度升高,气体的溶解度减小 B. 压强增大,气体的溶解度增大C. 温度升高,气体的溶解度增大 D. 压强增大,气体的溶解度减小
初中化学人教版九年级下册课题2 溶解度精品第1课时当堂检测题: 这是一份初中化学人教版九年级下册<a href="/hx/tb_c9866_t7/?tag_id=28" target="_blank">课题2 溶解度精品第1课时当堂检测题</a>,文件包含溶解度第1课时pptx、氯化钠在水中的溶解mp4、硝酸钾在水中的溶解mp4等3份试卷配套教学资源,其中试卷共0页, 欢迎下载使用。
人教版九年级下册课题2 溶解度精品课堂检测: 这是一份人教版九年级下册<a href="/hx/tb_c9866_t7/?tag_id=28" target="_blank">课题2 溶解度精品课堂检测</a>,文件包含第九单元课题2溶解度一原卷版docx、第九单元课题2溶解度一解析版docx等2份试卷配套教学资源,其中试卷共34页, 欢迎下载使用。
九年级下册课题2 溶解度随堂练习题: 这是一份九年级下册课题2 溶解度随堂练习题,共7页。试卷主要包含了饱和溶液与不饱和溶液,结晶,下列关于饱和溶液的说法正确的是等内容,欢迎下载使用。













