





高教版(2021)农林牧渔类第三节 化学键优质课课件ppt
展开1.能从原子的结构和组成出发,初步
【学习目标】 1. 通过观看视频或搭建模型,了解构成分子的微粒间的相互作用,建立化学键的概念。 2. 通过观看视频或动画,认识离子键和共价键的形成过程及条件,知道离子化合物和共价化合物的组成。
【核心素养】 能用变化的观念与平衡思想理解化学键的断裂和形成是化学反应中物质变化的实质,培养学生求真务实的科学态度。
原子可以结合成分子,如氯化氢分子。原子也可以失去电子或得到电子形成带电荷的阴、阳离子,阴、阳离子再结合成分子,如氯化钠分子。那么你知道钠离子和氯离子是怎样形成的吗?它们又是怎样结合成分子的呢?
使离子相结合或原子相结合的作用力通称为化学键。
通过阴、阳离子之间强烈的静电作用形成的化学键称为离子键。
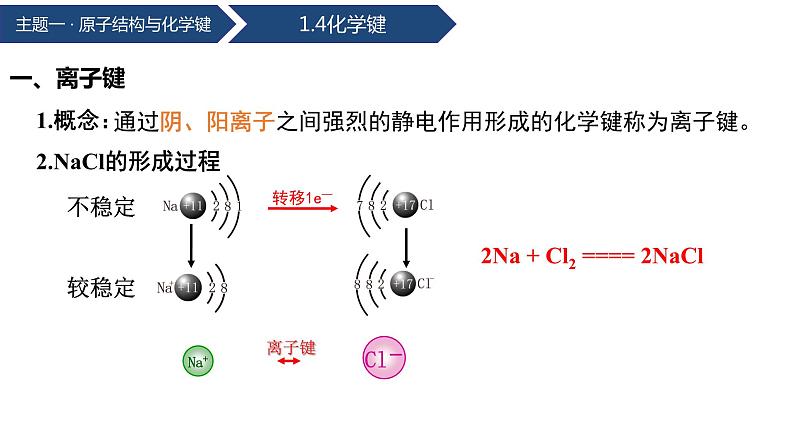
2.NaCl的形成过程
主题一 · 原子结构与化学键
2Na + Cl2 ==== 2NaCl
通常活泼金属(如钾、钠、钙等)与活泼非金属(如氯、溴、氧等)都能形成离子键。由离子键结合而成的化合物就称为离子化合物。
如 NaCl、KCl、MgO、CaO、ZnSO4、NaOH等,还有绝大多数盐类、碱类、部分金属氧化物都是离子化合物。
离子化合物的熔点、沸点较高,质硬而脆。
观察下列物质,你能辨识出下列哪些是离子化合物吗? NaCl CuSO4 KNO3 Cu NH4Cl H2O
氢元素和氯元素都是非金属原子,它们可以发生反应生成氯化氢分子。观看氯化氢分子形成的图例,相比氯化钠分子的形成过程你发现了什么区别?在成键过程中非金属原子核外电子是怎样作用的?
H2 + Cl2 = 2HCl
在化学上,常用一根短线表示一对共用电子对,因此,氢分子又可表示为H-H,氯分子表示为Cl-Cl。 HCl中的氢原子的一个电子,和Cl原子最外层的7个电子中的一个电子共用一对电子,彼此都能成为稳定结构,从而结合成为HCl分子,可表示为H—Cl。
原子间通过共用电子对所形成的相互作用,称为共价键。
如HCl、NH3、H2O、酒精、甘油等。
共价化合物一般硬度小,熔点、沸点较低。
只由共价键结合而成的化合物称为共价化合物
查阅资料,了解刚玉、水晶等宝石的主要成分,并讨论其组成的元素分别是金属元素还是非金属元素?属于哪种化合物?
红刚玉主要成分:Al2O3
水晶主要成分:SiO2
在化学反应中,反应物中的原子重新组合的过程包含着反应物分子内化学键的断裂和生成物分子中化学键的形成。 因此化学键的断裂和形成是化学反应中物质变化的实质
配位键,又称为配位共价键,是一种特殊的共价键。配位键成键的两原子间共享的一对电子不是由两原子各提供一个,而是来自一个原子(即提供孤对电子),另一个原子只提供空轨道,用→指向接受孤电子对的原子。 通常把金属离子(或原子)与某些分子或离子(称为配体)以配位键结合形成的化合物称为配位化合物,简称配合物。
1.元素周期表上的0族元素,以前被称为“惰性气体”,后因在空气中含量稀少改称“稀有气体”。稀有气体的分子全部是由单个原子组成的,都是单原子分子,为什么不能形成双原子分子呢? 2.下列物质由离子键结合的是 ,由共价键结合的是 既含有离子键又含有共价键的是 。(1)甲醇(CH3OH); (2)MgCl2; (3) NaOH 。
答: (2) (1) (3)
答:因为稀有气体元素的原子最外层电子排布都是稳定结构,不容易得失电子,也不容易与其他原子通过共用电子对结合,所以很难形成双原子分子。
高教版(2021)农林牧渔类基础模块主题六 常见生物分子及合成高分子化合物第一节 糖类完整版课件ppt: 这是一份高教版(2021)农林牧渔类基础模块主题六 常见生物分子及合成高分子化合物第一节 糖类完整版课件ppt,共34页。PPT课件主要包含了学习目标与核心素养,蛋白质等,主要内容,糖类的组成和分类,葡萄糖,蔗糖麦芽糖,存在形式,按照所含官能团的不同,分子结构,⑥使高锰酸钾褪色等内容,欢迎下载使用。
中职化学第三节 化学平衡完美版ppt课件: 这是一份中职化学第三节 化学平衡完美版ppt课件,共22页。PPT课件主要包含了学习目标与核心素养,主要内容,吸热反应和放热反应,可逆反应与不可逆反应,化学平衡,影响化学平衡的因素,放热反应,吸热反应,不可逆反应,可逆反应等内容,欢迎下载使用。
农林牧渔类第五节 盐的水解获奖课件ppt: 这是一份农林牧渔类第五节 盐的水解获奖课件ppt,共19页。PPT课件主要包含了学习目标与核心素养,主要内容,CuSO4,课堂小结等内容,欢迎下载使用。












