






高教版(2021)农林牧渔类第一节 原子结构精品ppt课件
展开人类生活在一个着得见、摸得着的宏观物质世界,而构成这一切的却是一些肉眼无法直接观察的微观物质。也许你已经知道了分子、原子等微观粒子的名字,它们的性质、结合成宏观物质的方式,是构成宏观物质世界的基础。学习微观粒子的内部结构及其相互作用方式,可以帮助我们了解和探索浩瀚物质世界的奥秘。
1.能从原子的结构和组成出发,初步
【学习目标】 1.通过观看原子结构的探究史的视频、原子结构模型和图片,认识原子的结构,了解原子的组成,认识构成原子的各种粒子间的关系,了解质量数(A)和质子数(Z)的含义,培养宏观辨识和微观探析等学科核心素养。 2.通过观察碳原子、氯原子、钠原子等原子的核外电子运动的动画,了解原子核外电子的排布规律,认识核外电子排布的一般规律。 3.根据核外电子排布的一般规律,能画出1~20号元素的原子结构示意图,培养学生求真务实的科学态度。
【核心素养】 以"证据推理和模型认知""宏观辨识与微观探析"两个化学核心素养目标为指向,体验原子结构模型的认识过程,强化结构决定性质观念。
水在人们的日常生活和工农业生产中必不可少;空气中除了含量最多的氧气和氮气,还有一类很重要的稀有气体,它们在生产和科学研究中有着广泛的用途;重要的调味品食盐的主要成分是氯化钠(图1-1-1),它在人体正常生理活动中起着重要作用。这些物质都是由各种微观粒子构成的,那么,你知道构成水、稀有气体、氯化钠等物质的微粒分别是什么吗?
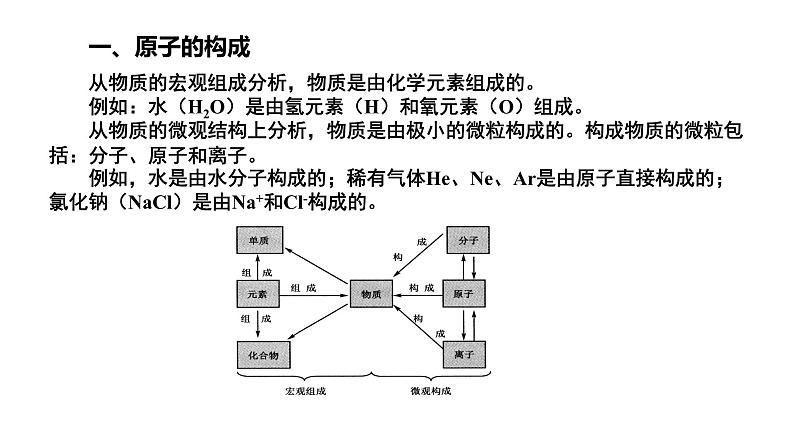
从物质的宏观组成分析,物质是由化学元素组成的。 例如:水(H2O)是由氢元素(H)和氧元素(O)组成。 从物质的微观结构上分析,物质是由极小的微粒构成的。构成物质的微粒包括:分子、原子和离子。 例如,水是由水分子构成的;稀有气体He、Ne、Ar是由原子直接构成的;氯化钠(NaCl)是由Na+和Cl-构成的。
古希腊哲学家认为原子是世间万物中最小的粒子。希腊语中“atm(原子)”的愿意就是指“不可分割的粒子”。
现代科学证明,原子是由比它更小的微粒构成的,物质是无限可分割的。
【观察与认知】 下图是在扫描隧道显微镜下移动排列的原子图,左图是用101个铁原子拼出的迄今为止最小的汉字。右图是中国科学院科学家以超真空扫描隧道显微镜为手段,通过移动单个硅原子构成“中国”二字。观察下图,你能看出原子是真实存在的吗?你能否进一步判断出原子是带电的还是电中性的?
101个铁原子(Fe)拼出的汉字 通过移动单个硅原子构成“中国”二字
原子是由居于原子中心的原子核和核外电子构成的,原子的尺寸比1nm更微小,它的直径约为1×10-10m。 原子核是由质子和中子组成的。原子核的直径为1×10-15~1×10-14m,约为原子直径的十万分之一。在原子内部的空间里,电子绕核高速运动,其速度大小接近光速。
(二)粒子的电性和电量
原子核中的每个质子带1个单位的正电荷,中子不带电,每个核外电子带1个单位的负电荷。经测定,原子核所带的电量与核外电子所带的电量相等,电性相反,所以原子是呈电中性的。原子核所带电荷数称为核电荷数。由于中子不带电,所以核电荷数等于核内质子数。核电荷数、核内质子数、核外电子数存在如下关系:
核电荷数=核内质子数=核外电子数
(三)粒子的质量和质量数
通常用一个12C原子质量的1/12作为标准,其他粒子的质量和它相比得出数值,称为粒子的相对质量。
【交流与讨论】 锂是世界上最轻的金属,约等于常见轻金属铝密度的五分之一,手机、蓝牙耳机等常见的电子产品中应用的锂离子电池中就含有丰富的锂元素。打开元素周期表,观察元素周期表中锂和铝的位置,你能从原子的角度说出锂比铝轻的原因吗?
表1-1-1 构成原子的粒子及其性质
【结论】原子核外电子质量微乎其微,原子的质量几乎全部集中在原子核上。
如果电子的质量忽略不计,原子相对质量的整数部分就等于质子相对质量(取整数)和中子相对质量(取整数)之和,这个数叫做质量数,用符号A表示。
(每个质子带1个单位正电荷 )
(每个电子带1个单位负电荷)
质量数(A)=质子数(Z)+中子数(N)
【小试牛刀】有A、B两种元素,已知元素A的核电荷数为a,且A3-与Bn+的电子排布完全相同,则元素B的质子数为( ) A.a-n-3 B.a+n+3 C.a+n-3 D.a-n+3
【观察与认知】 观察碳原子、氯原子、钠原子等原子的核外电子运动的动画,它们的原子核外电子排布是否有其规律?你能画出它们的原子结构示意图吗?
在含有多个电子的原子中,电子的能量并不相同。能量低的电子,在离核近的区域运动;能量高的电子,在离核远的区域运动。通常用电子层来表示运动着的电子距离原子核的远近。
表1-1-2 电子层与电子离核距离和电子能量高低的关系
表1-1-3核电荷数为1~18的元素原子核外电子的排布
表1-1-4稀有气体元素原子的电子层排布
核外电子排布的一般规律: 1.核外电子总是尽先排布在能量最低的电子层里,然后依次排布在能量逐步升高的电子层里。 2.各电子层最多容纳的电子数为2n2个(n为电子层数)。即K层最多容纳的电子数为2×12=2个, L层最多容纳的电子数为2×22=8个, M层最多容纳的电子数为2×32=18个,以此类推。 3.最外层电子数不超过8个(K层为最外层时不超过2个)。次外层的电子数不超过18个,倒数第三层的电子数不超过32个。 以上规律是相互联系的,不能孤立地理解。例如,19号元素钾的核外电子排布为2、8、8、1。而不能排布为2、8、9,否则违背最外层电子数不超过8个的规律。一般地说,最外层8个电子是相对稳定的结构。
【交流与讨论】 钠原子最外层只有1个电子,若达到8个电子的稳定结构,在化学反应中是得7个电子容易还是失去1个电子容易?氯原子最外层有7个电子,若达到8个电子的稳定结构,其趋势如何?
【实践活动】 质子数相同而中子数不同的同一元素的不同原子互称为同位素。它们在元素周期表中占据相同的位置。氢有三种同位素:氕、氘、氚。查阅资料,对比它们原子核的组成,了解氢元素的同位素在不同领域的应用,撰写一篇报告,在课堂上交流。
53 78 53
一种元素可以有几种不同的原子。
2个氢气分子、3个氢原子、4个氢离子、质量数为3的氢原子。
【小试牛刀】已知A、B、C三种元素的原子中,质子数为A<B<C,且都小于18,A元素的原子最外层电子数是次外层电子数的2倍;B元素的原子核外M层电子数是L层电子数的一半;C元素的原子次外层电子数比最外层电子数多1个。试推断: (1)三种元素的元素符号: A________;B________;C________。 (2)画出三种元素的原子结构示意图: A________;B________;C_________。
1.下列有关原子核外电子的说法错误的是( ) A.每个电子层作为最外层时,最多可容纳8个电子 B.电子在核外是分层排布的 C.电子不停地做高速运动 D.离原子核近的电子能量低,离原子核远的电子能量高
2.近日,中国科学院获得了全球第一条季节性河水钡同位素56138Ba变化曲线,填补了同位素陆表系统循环研究的空白。下列说法正确的是( ) A.56138Ba读作钡56B.56138Ba的中子数为82 C.56138Ba2+的电子数为136D.钡元素的质量数为138
3.根据电子排布情况,推断前20号元素中,符合要求的所有元素(1)最外层电子数为1:_________________;(2)最外层电子数是次外层电子数的3倍:______。(3)最外层电子数为内层电子数的2倍:____。(4)最外层电子数是电子层数的2倍:___________。(5)M电子层有3个电子:____。(6)L层电子数是K层和M层电子数之和的2倍:_____。(7)其简单阴离子带三个单位负电荷,且电子结构与氖相同:____。
高教版(2021)农林牧渔类第一节 油脂精品ppt课件: 这是一份高教版(2021)农林牧渔类第一节 油脂精品ppt课件,共19页。PPT课件主要包含了学习目标与核心素养,主要内容,油脂的组成及结构,油脂的性质,油脂在生物体内的作用,物理性质,化学性质,二化学性质,课堂小结等内容,欢迎下载使用。
高教版(2021)农林牧渔类基础模块主题六 常见生物分子及合成高分子化合物第一节 糖类完整版课件ppt: 这是一份高教版(2021)农林牧渔类基础模块主题六 常见生物分子及合成高分子化合物第一节 糖类完整版课件ppt,共34页。PPT课件主要包含了学习目标与核心素养,蛋白质等,主要内容,糖类的组成和分类,葡萄糖,蔗糖麦芽糖,存在形式,按照所含官能团的不同,分子结构,⑥使高锰酸钾褪色等内容,欢迎下载使用。
中职化学高教版(2021)农林牧渔类第一节 氧化还原反应优秀课件ppt: 这是一份中职化学高教版(2021)农林牧渔类第一节 氧化还原反应优秀课件ppt,共18页。PPT课件主要包含了学习目标与核心素养,主要内容,氧化还原反应的概念,氧化剂和还原剂,化学反应的分类,①按照反应形式分类,C+O2CO2,氧化剂与还原剂,常见氧化剂,常见还原剂等内容,欢迎下载使用。












