






初中人教版课题1 生活中常见的盐教学课件ppt
展开1.食盐主要成分_______2.粗盐提纯的步骤_________________________
溶解、过滤、蒸发、结晶
碳酸钠(Na2CO3)
水溶液呈碱性,纯碱不是碱,是盐
用途:常用于玻璃、造纸、纺织和洗涤剂的生产等。
碳酸氢钠(NaHCO3)
2NaHCO3 Na2CO3 + H2O + CO2↑
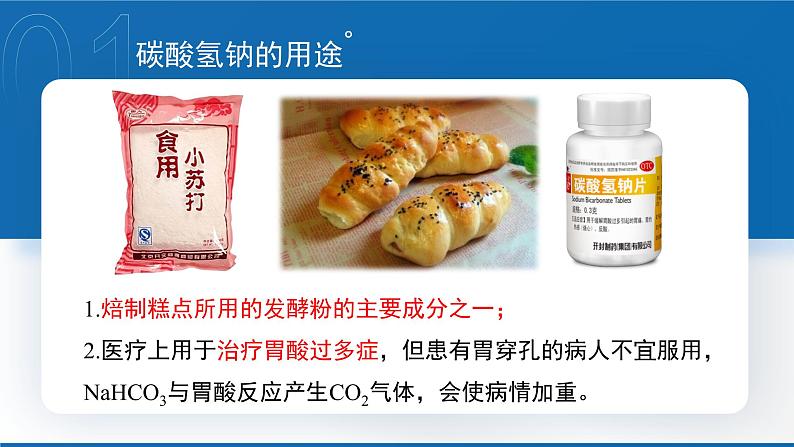
1.焙制糕点所用的发酵粉的主要成分之一;2.医疗上用于治疗胃酸过多症,但患有胃穿孔的病人不宜服用,NaHCO3与胃酸反应产生CO2气体,会使病情加重。
主要成分是碳酸钙的物质
碳酸钙用于实验室制取二氧化碳
CaCO3 + 2HCl == CaCl2 + H2CO3
H2CO3 == H2O + CO2↑
CaCO3 + 2HCl == CaCl2 + H2O + CO2↑
交流讨论:根据上述反应,推断一下Na2CO3和NaHCO3能否与稀盐酸反应?如果能反应,它们又会生成什么物质?
碳酸钠(或碳酸氢钠)与稀盐酸的反应
2 =2NaCl+CO2↑+H2O
=NaCl+CO2↑+H2O
盐的化学性质(1):盐 + 酸 = 新盐+新酸
Na2CO3+ HCl
CaCO3+2HCl= CaCl2+ CO2 ↑ +H2O
CO32-(或HCO3- )的检验
该样品是碳酸盐(溶液中存在CO32- 、HCO3-)
逻辑推理:活泼金属与酸反应有气体产生,则与酸反应产生气体的一定是活泼金属( )
碳酸钠溶液与澄清石灰水反应
碳酸钠与氢氧化钙反应生成碳酸钙,碳酸钙难溶于水,故溶液中出现浑浊(产生白色沉淀)
溶液中出现浑浊(产生白色沉淀)
Na2CO3+Ca(OH)2=CaCO3↓ +2NaOH
盐的化学性质(2):盐+ 碱= 新盐 + 新碱
交流讨论:观察下列这些反应,它们有什么共同点吗?
Na2CO3 + 2HCl == 2NaCl + H2O+CO2↑NaHCO3 + HCl == NaCl + H2O+CO2↑Na2CO3 + Ca(OH)2 == CaCO3↓ + 2NaOH
复分解反应:在溶液中,两种化合物互相交换成分,生成另外两种化合物的反应。
AB + CD → AD + CB
特点:“互交换,价不变”。
四大基本反应类型的比较
我国制碱工业的先驱--侯德榜
20世纪20年代,突破氨碱法制碱技术的奥秘,主持建成亚洲第一座纯碱厂;30年代,领导建成了中国第一座兼产合成氨、硝酸、硫酸和硫酸铵的联合企业;40~50年代,又发明了连续生产纯碱与氯化铵的联合制碱新工艺,以及碳化法合成氨流程制碳酸氢铵化肥新工艺;并使之在60年代实现了工业化和大面积推广。
拓展:石笋和钟乳石的形成
石灰岩的主要成分是碳酸钙,当遇到溶有二氧化碳的水时,会反应生成溶解性较大的碳酸氢钙: CaCO3 + H2O + CO2 == Ca(HCO3) 2。石灰岩地区若长期被含有二氧化碳的水侵蚀,就形成了溶洞。溶有碳酸氢钙的水遇热或当压强突然变小时,溶解在水里的碳酸氢钙就会分解,重新生成碳酸钙沉积下来,同时释放出二氧化碳:Ca(HCO3)2 == CaCO3↓+ H2O + CO2↑。石灰岩溶洞里奇特的钟乳石、石笋、石柱等就是这样形成的。
碳酸钠、碳酸氢钠和碳酸钙用途
碳酸钠、碳酸氢钠和碳酸钙和稀盐酸反应
碳酸根离子、碳酸氢根离子的检验
碳酸钠和澄清石灰水反应
1.下列属于复分解反应的是( )A.2NaOH+CO2=Na2CO3+H2O B.Zn+H2SO4=ZnSO4+H2↑ C.Na2CO3+2HCl=2NaCl+CO2↑+H2O D.CaCO3 CaO+CO2↑
2.下列物质的名称、俗称与化学式完全对应的是( )A.氯化钠 食盐 NaCl B.碳酸钠 纯碱 NaCO3C.氢氧化钙 生石灰 Ca(OH)2 D.碳酸氢钠 苏打 NaHCO3
3.下列有关盐的用途叙述错误的是 ( )A. 碳酸氢钠用于烘焙糕点 B. 碳酸钠用于造纸、纺织C. 碳酸钙用于配制农药波尔多液 D. 氯化钠用于消除道路积雪
初中课题1 生活中常见的盐一等奖教学课件ppt: 这是一份初中<a href="/hx/tb_c9873_t3/?tag_id=26" target="_blank">课题1 生活中常见的盐一等奖教学课件ppt</a>,共19页。PPT课件主要包含了白色固体难溶于水,小苏打,碳酸盐的化学性质,与酸反应生成二氧化碳,实验11-1,碳酸根离子的检验,练习一,样品中一定含有,练习二,该溶液中一定含有等内容,欢迎下载使用。
人教版九年级下册第十一单元 盐 化肥课题1 生活中常见的盐教学课件ppt: 这是一份人教版九年级下册第十一单元 盐 化肥课题1 生活中常见的盐教学课件ppt,共21页。PPT课件主要包含了产生蓝色沉淀,产生白色沉淀,Cl-,反应前,反应后,CO2↑,SO42-,NO3-,有水生成,有气体生成等内容,欢迎下载使用。
人教版九年级下册第十一单元 盐 化肥课题1 生活中常见的盐教学课件ppt: 这是一份人教版九年级下册第十一单元 盐 化肥课题1 生活中常见的盐教学课件ppt,共21页。PPT课件主要包含了亚硝酸钠NaNO2,盐的概念,HCl,CaOH2,NaCl,H2SO4,NaOH,Na2CO3,NaHCO3,CaCO3等内容,欢迎下载使用。














