


苏教版 (2019)必修 第一册第三单元 物质的分散系精品一课一练
展开1.3物质的分散系 同步练习 2022-2023学年高一上学期化学苏教版(2020)必修第一册
一、单选题
1.下列物质能通过化合反应直接制得的是
①FeCl2 ②FeCl3 ③Fe(OH)3 ④HCl
A.只有①②③ B.只有②③ C.只有①③④ D.全部
2.下列叙述不正确的是
A.实验测定冰醋酸、固体KNO3均不能导电,所以CH3COOH、KNO3均是非电解质
B.铜丝有较好的导电性,不是电解质
C.AgCl、BaSO4都难溶于水,但它们都是电解质
D.蔗糖在水溶液和熔融状态下均不能导电,所以蔗糖属于非电解质
3.下列操作能观察到丁达尔效应的是
A.光束通过盐酸溶液 B.光束通过NaCl
C.光束通过CuSO4溶液 D.光束透过树叶间的缝隙射入密林中
4.下列对物质的分类正确的是
A.纯碱属于碱 B.CuSO4·5H2O属于盐 C.H2CO3属于有机物 D.蔗糖属于电解质
5.当光束通过下列分散系时,能观察到丁达尔效应的是
A.硫酸铜溶液 B.氢氧化铁胶体 C.饱和食盐水 D.稀盐酸
6.电解质溶液导电能力的强弱。主要取决于
A.电解质的性质 B.溶液中电解质的物质的量浓度
C.电解质的溶解度 D.溶液中自由移动离子的物质的量浓度
7.下表中物质的分类组合,完全正确的是( )
编号 | A | B | C | D |
强电解质 | KNO3 | H2SO4 | BaSO4 | NaCl |
弱电解质 | NH3·H2O | CaCO3 | HClO | C2H5OH |
非电解质 | CO2 | Al | H2O | CH3COOH |
A.A B.B C.C D.D
8.下列物质属于非电解质的是
A.Cu B.HCl C.NH3 D.NaCl
9.关于胶体的叙述不正确的是
A.胶体的分散质粒子直径在![]() 之间
之间
B.胶体区别于其它分散系的本质特征是胶体的分散质能透过滤纸
C.向沸水中滴加饱和![]() 溶液,通过
溶液,通过![]() 与水反应可制得胶体
与水反应可制得胶体
D.实验室利用“丁达尔效应”,可以鉴别氯化钠溶液和淀粉溶液
10.下列关于强、弱电解质的叙述,有错误的是
A.强电解质在溶液中完全电离,不存在电离平衡
B.纯净的强电解质在液态时,有的导电,有的不导电
C.同一弱电解质的溶液,当温度、浓度等不同时,其导电能力也不同
D.在溶液中,导电能力强的电解质是强电解质,导电能力弱的电解质是弱电解质
11.分类是化学学习与研究的常用方法,下列分类正确的是
A.SO2、SO3、CO2均属于酸性氧化物
B.Na2O、Al2O3都是金属氧化物,属于碱性氧化物
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.根据溶液导电能力强弱,将电解质分为强电解质、弱电解质
12.下列物质中,属于电解质的是
A.铜丝 B.乙醇 C.NaCl溶液 D.MgCl2固体
13.下列物质在水溶液中的电离方程式书写正确的是( )
A.CH3COOH=H++CH3COO- B.NaHSO4=Na++H++![]()
C.H3PO4![]() 3H++
3H++![]() D.NaHCO3
D.NaHCO3![]() Na++H++
Na++H++![]()
14.下列物质的电离方程式书写正确的是
A.H2SO4=![]() +
+![]() B.NaOH=Na++O2-+H+
B.NaOH=Na++O2-+H+
C.NH4NO3=![]() +
+![]() D.CH3COOH=CH3COO-+H+
D.CH3COOH=CH3COO-+H+
二、填空题
15.(1)有以下物质:①CO2气体②FeCl3溶液③淀粉溶液④NH4Cl晶体⑤蔗糖溶液⑥钠⑦BaSO4固体⑧CCl4⑨NaOH溶液⑩CH3COOH
属于强电解质的是___,属于非电解质是___,能导电的是___。
(2)写出⑩的电离方程式___。
16.现有下列物质:①NaCl晶体;②冰醋酸(纯醋酸晶体);③CO2;④铜;⑤蔗糖;⑥熔融的KNO3;⑦稀盐酸溶液;⑧酒精;⑨液氯;⑩BaSO4固体
(1)能导电的是___。(填标号,下同)
(2)属于电解质的是___。
(3)属于非电解质的是___。
(4)既不是电解质也不是非电解质的是___。
三、计算题
17.“题18图”为两物质的溶解度曲线。请回答:
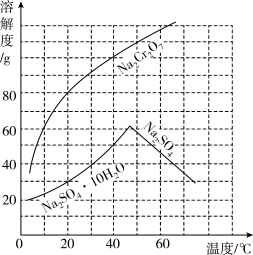
(1)50℃时,Na2Cr2O7的溶解度为________g;60℃时溶解度:Na2Cr2O7__________Na2SO4(填“<”、“=”、“>”)。
(2)在50℃时,把210gNa2Cr2O7饱和溶液降温到10℃时,析出Na2Cr2O7______________g (假设不含结晶水)。
18.回答下列问题。
(1)现有下列物质:①CO2 ②液态氯化氢 ③CH4 ④熔融NaOH ⑤NH4Cl固体 ⑥氨水
请用序号回答下列问题:能导电的是___。属于电解质的是___。属于非电解质的是___。
(2)K2SO4和Fe2(SO4)3的混合溶液,已知其中Fe3+的浓度为0.5mol/L,SO42-浓度为0.9mol/L,则K+的物质的量浓度为___mol/L。
(3)1.204×1024个H2SO4分子的物质的量为___mol,共含___个氢原子。将上述H2SO4溶于水配成600mL溶液,再加水稀释到1000mL,稀释后溶液的物质的量浓度为___mol/L。
(4)15.6gNa2R2中含0.4mol的Na+,则R的相对原子质量是___。
四、实验题
19.现有甲、乙、丙三名同学分别进行硅酸胶体的制备实验。
分组 | 实验操作 | 实验现象 |
甲 | 将1%硅酸钠溶液滴入沸水中,冷却后用激光笔进行照射 | 无明显现象,未出现“光亮的通路” |
乙 | 向1%硅酸钠溶液中加入几滴酚酞溶液,缓慢滴入稀盐酸,溶液红色褪去后停止滴加,用激光笔进行照射 | 出现“光亮的通路” |
丙 | 向1%硅酸钠溶液中加入等体积的稀盐酸,用激光笔进行照射 | 未出现“光亮的通路”,溶液中出现浑浊 |
已知:I.硅酸钠(Na2SiO3)溶液呈碱性;II.常温下硅酸(H2SiO3)的溶解度为5×10-5 g/100 g水
试回答下列问题:
(1)成功制备硅酸胶体的是_______同学,出现“光亮的通路”这种现象的名称是_______。
(2)形成硅酸胶体的离子方程式为_______。
(3)根据三位同学的实验操作可得,成功制备硅酸胶体的关键在于_____A.硅酸钠溶液的质量分数 B.稀盐酸的加入量
C.激光笔进行照射 D.酚酞溶液加入
(4)丙同学制备实验中溶液出现浑浊的原因是_______。
(5)制备的胶体中含有的主要杂质是_______,除去此杂质可采取的操作方法为_______。
参考答案:
1.D
【详解】①氯化亚铁可以由氯化铁和铁化合得到;②氯化铁可以由铁和氯气化合得到;③氢氧化铁可以由氢氧化亚铁和氧气和水化合得到;④氯化氢可以由氢气和氯气化合得到。所以选D。
【点睛】这里所说的化合反应没有要求必须是单质之间的化合,所以也可以是化合物之间的化合。有些化合物元素比较多,可以由化合物之间的化合得到。例如氧化钠和水化合反应生成氢氧化钠,氧化钠和二氧化碳化合得到碳酸钠,碳酸钠和水和二氧化碳化合得到碳酸氢钠等。
2.A
【详解】A.实验测定冰醋酸、固体KNO3均不能导电,他们没有自由移动的离子,但溶于水后有自由移动的离子,能导电,所以CH3COOH、KNO3均是电解质,故A错误;
B.铜丝有较好的导电性,铜丝是单质,既不是电解质,也不是非电解质,故B正确;
C.AgCl、BaSO4都难溶于水,在熔融状态下能导电,因此它们都是电解质,故C正确;
D.蔗糖在水溶液和熔融状态下均不能导电,蔗糖属于有机物,所以蔗糖属于非电解质,故D正确。
综上所述,答案为A。
3.D
【分析】胶体具有丁达尔效应。
【详解】A.盐酸溶液不是胶体,光束通过盐酸溶液,不能观察到丁达尔效应,A错误;
B.NaCl不是胶体,光束通过NaCl溶液,不能观察到丁达尔效应,B错误;
C.CuSO4溶液不是胶体,光束通过CuSO4溶液,不能观察到丁达尔效应,C错误;
D.小液滴或固体小颗粒分散在空气中形成胶体,光束透过树叶间的缝隙射入密林中,能观察到丁达尔效应,D正确;
故选D。
4.B
【详解】A.纯碱是碳酸钠属于盐类,故A错误;
B.CuSO4·5H2O,由金属阳离子和酸根离子结合而成,属于盐类,故B正确;
C.H2CO3属于无机酸,不是有机物,故C错误;
D.蔗糖溶于水不能发生电离,属于非电解质,故D错误;
故选:B。
5.B
【详解】A.硫酸铜溶液不属于胶体,不能表现胶体的性质,不能发生丁达尔效应,故A错误;
B.氢氧化铁胶体属于胶体,能表现胶体的性质,能发生丁达尔效应,故B正确;
C.饱和食盐水不属于胶体,不能表现胶体的性质,不能发生丁达尔效应,故C错误;
D.稀盐酸不属于胶体,不能表现胶体的性质,不能发生丁达尔效应,故D错误;
故选B。
6.D
【详解】电解质溶液的导电性主要与离子浓度及离子所带电荷数有关,故导电能力的强弱主要取决于溶液中自由移动离子的物质的量浓度,故选D。
7.A
【详解】A.KNO3在水溶液或熔融状态下完全电离,属于强电解质;NH3·H2O为弱碱,属于弱电解质,CO2的水溶液虽导电,但不是自身导电,属于非电解质,故A正确;
B.CaCO3在熔融状态下能完全电离,属于强电解质,Al属于单质,不是非电解质,故B错误;
C.H2O属于弱电解质,故C错误;
D.C2H5OH属于非电解质,CH3COOH属于弱电解质,故D错误;
答案选A。
8.C
【详解】A.Cu是金属单质,既不是电解质又不是非电解质,故不选A;
B.HCl的水溶液能导电,HCl是电解质,故不选B;
C.NH3自身不能电离,NH3是非电解质,故选C;
D.NaCl溶液能导电,NaCl是电解质,故不选D;
选C。
9.B
【详解】A.胶体的分散质粒子直径在![]() 之间,A正确;
之间,A正确;
B.胶体区别于其它分散系的本质特征是分散质粒子直径大小不同,B错误;
C.向沸水中滴加饱和![]() 溶液,继续加热可以通过
溶液,继续加热可以通过![]() 的水解反应可制得胶体,C正确;
的水解反应可制得胶体,C正确;
D.胶体有丁达尔效应,所以可以用丁达尔效应鉴别溶液和胶体,D正确;
故选B。
10.D
【详解】A.强电解质在溶液中完全电离,不存在电离平衡,故A正确;
B.离子化合物类强电解质,液态时能导电,如NaCl,K2SO4等,共价化合物类强电解质,液态时不导电,如AlCl3,HCl等,故B正确;
C.弱电解质存在电离平衡,电离过程是吸热过程,温度改变,电离平衡移动,离子浓度不同,导电能力不同,故C正确;
D.溶液的导电能力与溶液中离子浓度成正比,与电解质的强弱无关,强电解质溶液的导电能力不一定比弱电解质溶液强,故D错误;
故选D。
11.A
【详解】A.CO2、SO2、SO3均只和碱反应生成盐和水,属于酸性氧化物,故A正确;
B.Al2O3可与酸也能与碱反应,属于两性氧化物,而Na2O为碱性氧化物,故B错误;
C.根据分散系中分散质粒子直径大小将分散系分为溶液、胶体和浊液,故C错误;
D.依据溶液中是否完全电离,电解质分为强电解质和弱电解质,强电解质导电能力不一定比弱电解质,故D错误;
故选:A。
12.D
【详解】在熔融状态或水溶液中可以导电的化合物为电解质;
A.铜丝虽然导电但为单质,不是电解质,故A不符合题意;
B.乙醇无论水溶液还是熔融状态,都不能导电,为非电解质,故B不符合题意;
C.氯化钠溶液为混合物,不是电解质,故C不符合题意;
D.氯化镁固体为化合物,其水溶液和熔融状态都可以导电,为电解质,故D符合题意;
综上所述答案为D。
13.B
【详解】A.醋酸为弱酸,是弱电解质,电离时应当用可逆符号, ![]() ,A错误;
,A错误;
B.硫酸为强酸,NaHSO4其电离成Na+、H+、SO42-,B正确;
C.磷酸不是强酸,应分步电离,以第一步为主,![]() ,C错误;
,C错误;
D.碳酸氢钠应完全电离,所以电离方程式应使用等号,碳酸为弱酸,碳酸氢根离子不能拆写,![]() ,D错误。
,D错误。
答案选B。
14.C
【详解】A.H2SO4是强酸,在溶液中完全电离出氢离子和硫酸根离子,其电离方程式为H2SO4═2H++![]() ,故A错误;
,故A错误;
B.NaOH是强电解质,在水溶液中完全电离生成钠离子和氢氧根离子,电离方程式为NaOH═Na++OH-,故B错误;
C.硝酸铵在溶液中完全电离为铵根离子和硝酸根离子,故电离方程式为NH4NO3=![]() +
+![]() ,故C正确;
,故C正确;
D.乙酸为弱酸,部分电离出乙酸根离子和氢离子,电离方程式为:CH3COOH⇌CH3COO-+H+,故D错误。
答案选C。
15. ④⑦ ①⑧ ②⑥⑨ CH3COOH⇌CH3COO-+H+
【分析】(1)在水溶液中或熔化状态下能导电的化合物属于电解质;在水溶液中和熔化状态下都不能导电的化合物属于非电解质;在溶液中或熔融状态下完全电离的为强电解质;
(2)醋酸是弱酸,不能完全电离。
【详解】(1)①CO2气体溶于水生成H2CO3,其水溶液能导电,但其本身不导电,为非电解质;
②FeCl3溶液能导电,但是混合物,不是电解质,也不是非电解质;
③淀粉溶液不能导电,是混合物,不是电解质,也不是非电解质;
④NH4Cl晶体的水溶液导电,是强电解质,但晶体本身不导电;
⑤蔗糖溶液不能导电,是混合物,不是电解质,也不是非电解质;
⑥钠能导电,是单质,不是电解质,也不是非电解质;
⑦BaSO4固体不导电,但熔融状态下能导电,是强电解质;
⑧CCl4不能导电,是非电解质;
⑨NaOH溶液能导电,但是混合物,不是电解质,也不是非电解质;
⑩CH3COOH是弱电解质,且本身不导电;
故属于强电解质的是④⑦,属于非电解质是①⑧,能导电的是②⑥⑨;
(2)CH3COOH为弱电解质,其电离方程式为:CH3COOH⇌CH3COO-+H+。
【点睛】电解质是指在水溶液中或熔融状态下能导电的化合物,例如酸、碱、盐、活泼金属氧化物等,凡在上述情况下不能导电的化合物叫非电解质,例如非金属氧化物、一些氢化物和一些有机物如蔗糖和酒精等;特别注意能导电的不一定是电解质,且非电解质的水溶液也可能导电,如CO2的水溶液导电,是因为生成碳酸的缘故;另外电解质和非电解质都是化合物,既要排除单质又要排除混合物。
16. ④⑥⑦ ①②⑥⑩ ③⑤⑧ ④⑦⑨
【分析】①NaCl晶体中没有自由移动的电子和离子,不能导电,其水溶液可电离出钠离子和氯离子可导电,属于电解质;
②冰醋酸(纯醋酸晶体)中没有自由移动的电子和离子,不能导电,其水溶液可电离出氢离子和醋酸根离子可导电,属于电解质;
③CO2没有自由移动的电子和离子,不能导电,其与水反应后所得的溶液可电离出离子可导电,但不是自身电离,属于非电解质;
④铜有自由移动的电子,能导电,但属于单质不是化合物,既不是电解质也不是非电解质;
⑤蔗糖没有自由移动的电子和离子,不能导电,其水溶液或熔融状态下都不能导电,属于非电解质;
⑥熔融的KNO3有自由移动的离子,可导电,其水溶液可电离出钾离子和硝酸根离子可导电,属于电解质;
⑦稀盐酸溶液中含有自由移动的离子能导电,但属于混合物,既不是电解质也不是非电解质;
⑧酒精没有自由移动的电子和离子,不能导电,其水溶液或熔融状态下都不能导电,属于非电解质;;
⑨液氯没有自由移动的离子或电子,不导电,液氯属于单质,不是化合物,既不是电解质也不是非电解质;
⑩BaSO4固体中没有自由移动的离子,不导电,但在熔融状态下可电离出钡离子和硫酸根离子,可导电,属于电解质;
【详解】(1)根据分析,能导电的是④⑥⑦,
答案为:④⑥⑦;
(2)根据分析,属于电解质的是①②⑥⑩,
答案为:①②⑥⑩;
(3)根据分析,属于非电解质的是③⑤⑧,
答案为:③⑤⑧;
(4)根据分析,既不是电解质也不是非电解质的是④⑦⑨,
答案为:④⑦⑨。
【点睛】不论电解质还是非电解质都必须是化合物,能导电的物质不一定是电解质,能否导电主要看是否存在自由移动的电子和自由移动的离子;区分电解质和非电解质的方法是看在水溶液或熔融状态下自身能否导电。
17. 110 > 50
【分析】根据图像可知,Na2Cr2O7的溶解度随温度升高而增大,Na2SO4的溶解度随温度升高而减小。
【详解】(1)由曲线可知,50℃时,Na2Cr2O7的溶解度为110g;60℃时Na2Cr2O7的溶解度>Na2SO4的溶解度。
(2)由曲线可知,50℃时,Na2Cr2O7的溶解度为110g,10℃时Na2Cr2O7的溶解度为60g,50℃时,把210gNa2Cr2O7饱和溶液降温到10℃时,析出Na2Cr2O7的质量为110g-60g=50g。
18. ④⑥ ②④⑤ ①③ 0.3mol/L 2 2.408×1024(4NA) 2 16
【详解】(1)①CO2液态时不导电,化合物,为非电解质;
②液态氯化氢溶于水后导电,化合物,为电解质;
③CH4溶于水和液态时均不导电,化合物,为非电解质;
④熔融NaOH能导电,化合物,为电解质;
⑤NH4Cl固体不导电,溶于水能导电,化合物,为电解质;
⑥氨水为混合物,既不是电解质,也不是非电解质;
则能导电的是④⑥;属于电解质的为②④⑤;属于非电解质的为①③;
(2)根据溶液呈电中性, c(Fe3+)![]() 3+ c(K+)
3+ c(K+)![]() 1= c(SO42-)
1= c(SO42-)![]() 2,则c(K+)=0.3mol/L;
2,则c(K+)=0.3mol/L;
(3)n(H2SO4)=N/NA=1.204×1024/6.02×1023=2mol;含有4mol氢原子,即氢原子个数为2.408×1024(4NA);c(H2SO4)=n/V=2mol/1L=2mol/L;
(4)一个Na2R2中含2个Na+,含0.4mol Na+的Na2R2的物质的量为0.2mol,则M(Na2R2)=m/n=15.6g/0.2mol=78g/mol,则R的摩尔质量为(78 g/mol -23 g/mol×2)/2=16g/mol。
19.(1) 乙 丁达尔效应
(2)SiO![]() +2H+=H2SiO3(胶体)
+2H+=H2SiO3(胶体)
(3)B
(4)过量的盐酸导致胶体发生聚沉
(5) NaCl 渗析法
【分析】(1)
乙同学用激光灯照射,出现“光亮的通路”,所以成功制备硅酸胶体的是乙同学,出现“光亮的通路”这种现象的名称是丁达尔效应。
(2)
向1%硅酸钠溶液中缓慢滴入稀盐酸,可以形成胶体,形成硅酸胶体的离子方程式为SiO![]() +2H+=H2SiO3(胶体);
+2H+=H2SiO3(胶体);
(3)
根据三位同学的实验操作可得,成功制备硅酸胶体的关键在于稀盐酸的加入量,故选B;
(4)
丙同学制备实验中,加入过量盐酸,过量的盐酸导致胶体发生聚沉,所以溶液出现浑浊;
(5)
硅酸钠和盐酸反应生成硅酸胶体和氯化钠,所以制备的胶体中含有的主要杂质是NaCl,胶体粒子不能通过半透膜、氯化钠溶液能透过半透膜,除去NaCl杂质可采取的操作方法为渗析法。
高中化学苏教版 (2019)必修 第一册第三单元 物质的分散系复习练习题: 这是一份高中化学苏教版 (2019)必修 第一册第三单元 物质的分散系复习练习题,共18页。试卷主要包含了单选题,填空题,实验探究题等内容,欢迎下载使用。
高中化学第三单元 物质的分散系课后作业题: 这是一份高中化学第三单元 物质的分散系课后作业题,共16页。试卷主要包含了单选题,填空题,实验题等内容,欢迎下载使用。
高中化学苏教版 (2019)必修 第一册第三单元 物质的分散系练习题: 这是一份高中化学苏教版 (2019)必修 第一册第三单元 物质的分散系练习题,共11页。试卷主要包含了单选题,填空题,实验题等内容,欢迎下载使用。













