

2022-2023学年天津市八校联考高一上学期期中考试化学试题含解析
展开天津市八校联考2022-2023学年高一上学期期中考试化学试题
学校:___________姓名:___________班级:___________考号:___________
一、单选题
1.下列物质不属于酸性氧化物的是
A.Na2O B.SO3 C.SiO2 D.P2O5
【答案】A
【分析】能与碱反应生成盐和水的氧化物是酸性氧化物,据此判断。
【详解】A.Na2O和酸反应生成盐和水,是碱性氧化物,A符合;
B.SO3能与碱反应生成盐和水,是酸性氧化物,B不符合;
C.SiO2能与碱反应生成盐和水,是酸性氧化物,C不符合;
D.P2O5能与碱反应生成盐和水,是酸性氧化物,D不符合;
答案选A。
2.人们利用焰色试验制造了绚丽多彩的烟花,下列物质的焰色为紫色(透过蓝色钴玻璃)的是
A.Na2CO3 B.KCl C.CaCl2 D.CuSO4
【答案】B
【分析】焰色反应为元素的性质,属于物理性质,只要含有同种元素就会显示相同的焰色。
【详解】A.钠元素的焰色为黄色,故Na2CO3的焰色为黄色,A错误;
B.钾元素的焰色为紫色,故KCl的焰色为紫色(透过蓝色钴玻璃),B正确;
C.钙元素的焰色为砖红色,故CaCl2的焰色为砖红色,C错误;
D.铜元素的焰色为绿色,故CuSO4的焰色为绿色,D错误;
故答案选B。
3.以下表示的是碳及其化合物的转化关系,其中涉及的基本反应类型依次是
CCO2H2CO3CaCO3
A.化合、置换、分解 B.置换、复分解、化合
C.置换、化合、分解 D.置换、化合、复分解
【答案】D
【详解】在加热的条件下碳置换出氧化铜中的铜,属于置换反应;二氧化碳溶于水生成碳酸,是化合反应;碳酸和氢氧化钙发生中和反应,属于复分解反应。
答案选D。
4.某无色透明的酸性溶液中能大量共存的是
A.、、 B.、、
C.、、 D.、、
【答案】C
【详解】A.在溶液中显蓝色,与无色透明溶液不相符,选项A错误;
B.酸性溶液中不能大量存在,会反应产生二氧化碳气体,选项B错误;
C.、、各离子及氢离子之间相互不反应,且均无色,符合条件,选项C正确;
D.、均能与反应生成沉淀而不能大量共存,且与氢离子反应生成水而不能大量存在于酸性溶液中,选项D错误;
答案选C。
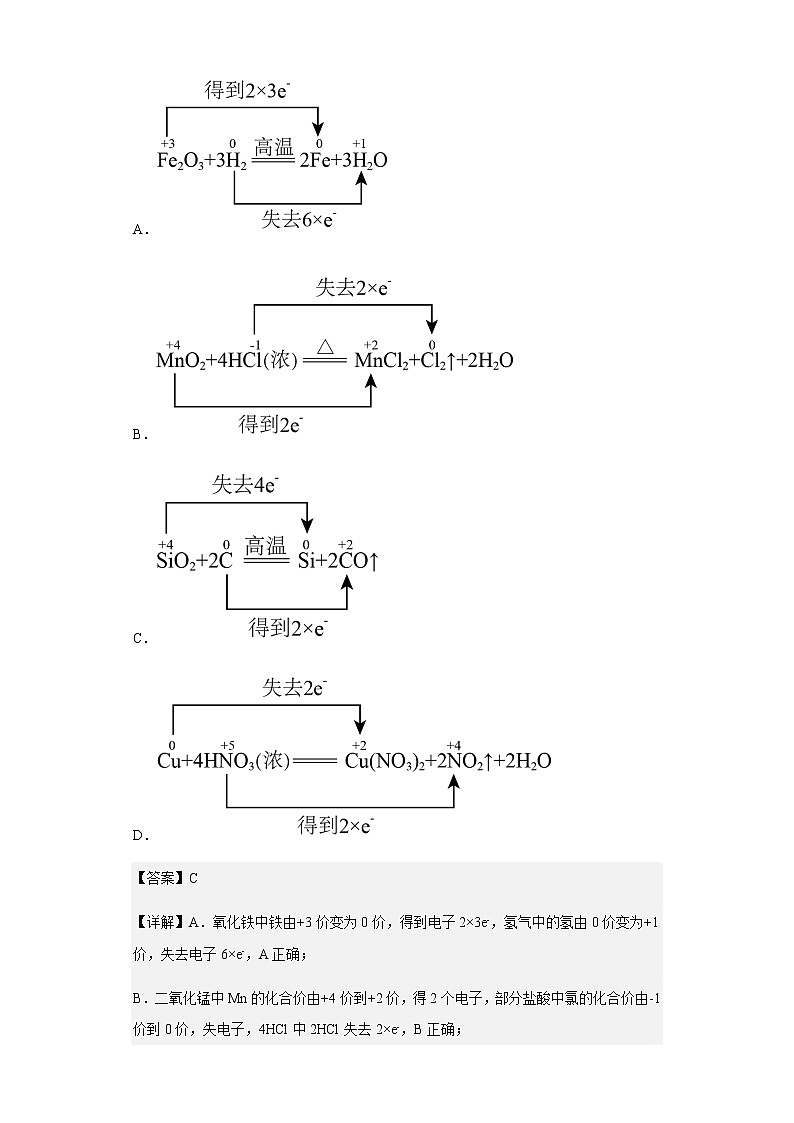
5.下列氧化还原反应中电子的转移表示错误的是
A.
B.
C.
D.
【答案】C
【详解】A.氧化铁中铁由+3价变为0价,得到电子2×3e-,氢气中的氢由0价变为+1价,失去电子6×e-,A正确;
B.二氧化锰中Mn的化合价由+4价到+2价,得2个电子,部分盐酸中氯的化合价由-1价到0价,失电子,4HCl中2HCl失去2×e-,B正确;
C.二氧化硅中的硅为+4价,应得到4个电子变为0价的硅;碳单质的化合价为0价,应该失去2×2e-电子,C错误;
D.铜由0价变为+2价,失去1×2e-电子,硝酸中部分氮由+5价变为+4价,得到2×e-电子,D正确;
故选C。
6.对于反应3Cl2+6NaOH(热)=5NaCl+NaClO3+3H2O,下列叙述正确的是
A.Cl2是氧化剂,NaOH是还原剂
B.被氧化的氯原子和被还原的氯原子的个数之比为1∶5
C.H2O是还原产物
D.氧化剂的得电子数与还原剂的失电子数之比为5∶1
【答案】B
【分析】对于反应3Cl2+6NaOH(热)=5NaCl+NaClO3+3H2O,Cl元素化合价一部分升高、一部分降低;Cl2中Cl显0价,NaCl中Cl显-1价,NaClO3中Cl显+5价。
【详解】A.由分析可知,反应中只有Cl元素价态发生改变,所以Cl2既是氧化剂又是还原剂,NaOH中不存在价态发生改变的元素,既不是还原剂也不是氧化剂,A不正确;
B.由反应方程式可知,被氧化的氯原子(生成NaClO3)和被还原的氯原子(生成NaCl)的个数之比为1∶5,B正确;
C.H2O中不存在价态变化的元素,所以不是还原产物,C不正确;
D.依据得失电子守恒的原则,氧化剂的得电子数与还原剂的失电子数相等,二者得失电子数之比为1∶1,D不正确;
故选B。
7.根据下列反应:(1)2Fe3++2I-=2Fe2++I2;(2)Br2+2Fe2+=2Br-+2Fe3+,判断离子的还原性由强到弱的顺序是
A.Br->I->Fe2+ B.I->Fe2+>Br-
C.Fe2+>I->Br- D.Br->Fe2+>I-
【答案】B
【详解】反应2Fe3++2I-=2Fe2++I2中,I-是还原剂,Fe2+是还原产物,则还原性I->Fe2+;反应Br2+2Fe2+=2Br-+2Fe3+中,Fe2+是还原剂,Br-是还原产物,则还原性Fe2+>Br-;从而得出还原性I->Fe2+>Br-,故选B。
8.能正确表示下列反应的离子方程式的是
A.Cu与溶液反应:Cu + Ag+ =Cu2+ +Ag
B.钠与溶液反应:
C.大理石与稀盐酸反应:
D.稀硫酸滴在铜片上:
【答案】C
【详解】A.Cu与溶液发生置换反应,反应离子方程式为Cu + 2Ag+ =Cu2+ +2Ag,故A项错误;
B.钠单质属于非常活泼的金属单质,能与水发生置换反应,因此钠单质不能将中Cu置换出来,故B项错误;
C.大理石中碳酸钙能与盐酸发生复分解反应生成氯化钙、水、二氧化碳,反应离子方程式为,故C项正确;
D.铜与稀硫酸不反应,故D项错误;
综上所述,正确的是C项。
9.下列物质的保存方法不正确的是
A.新制氯水保存在棕色试剂瓶中 B.金属钠保存在煤油中
C.过氧化钠应密封保存 D.漂白粉可以露置于空气中
【答案】D
【详解】A.新制氯水中的次氯酸稳定性较差,见光易分解,因此新制氯水需避光保持,常保存在棕色试剂瓶中,故A项正确;
B.钠单质活泼性较好,易与空气中氧气、水发生反应,不能暴露于空气,根据钠单质密度大于煤油,因此金属钠常保存在煤油中,故B项正确;
C.过氧化钠能与空气中二氧化碳、水发生反应,因此需密封保存,故C项正确;
D.漂白粉中次氯酸钙能与空气中二氧化碳、水发生反应,因此不能暴露于空气中,故D项错误;
综上所述,不正确的是D项。
10.有两个无标签的试剂瓶,分别装有Na2CO3和NaHCO3固体,有4位同学为鉴别它们采用了以下不同的方法,其中可行的是
A.分别配成溶液,再加入澄清石灰水
B.分别配成溶液,再加入NaOH溶液
C.分别加热,再检验是否有使澄清石灰水变浑浊的气体产生
D.分别配成溶液,再进行焰色试验
【答案】C
【详解】A.碳酸钠和碳酸氢钠都会与澄清石灰水反应生成碳酸钙沉淀,无法鉴别,A错误;
B.碳酸钠不与氢氧化钠反应,无现象;碳酸氢钠与氢氧化钠要反应,但也无明显现象,无法鉴别,B错误;
C.加热,碳酸钠受热不反应;碳酸氢钠受热产生二氧化碳使石灰水变浑浊,现象不同,可以鉴别,C正确;
D. 由于都是钠盐,焰色反应都是黄色,无法鉴别,D错误;
故选C。
11.下列叙述正确的是
A.1 mol H2O的质量为18 g∙mol−1
B.CH4的摩尔质量为16 g
C.3.01×1023个SO2分子的质量为32g
D.标准状况下,1 mol任何物质体积均为22.4 L
【答案】C
【详解】A.1 mol H2O的质量为18 g,故A错误;
B.CH4的摩尔质量为16 g∙mol−1,故B错误;
C.3.01×1023个SO2分子的物质的量为0.5mol,质量为32g,故C正确;
D.标准状况下,1 mol任何气体的体积都约为22.4 L,不能是任何物质,故D错误。
综上所述,答案为C。
12.同温同压下,用等质量的CH4、CO2、N2、SO2四种气体分别吹出四个气球(同一种气球),其中气体为SO2的是
A. B. C. D.
【答案】A
【详解】同温同压下,气体的物质的量之比等于气体的体积之比,根据可知,等质量气体的摩尔质量越小,气体的物质的量越大,气体的体积越大,,因此SO2的体积最小,故答案为A。
二、填空题
13.现有以下物质:①Na;②O2;③H2SO4;④KOH;⑤蔗糖;⑥H2O;⑦NaCl;⑧空气;⑨NaHSO4;⑩Na2CO3;按要求填空:
(1)属于氧化物的是:_______;属于酸的是:_______;属于电解质的是_______;写出一种与②互为同素异形体的物质的化学式_______。
(2)写出③在水溶液中电离的电离方程式_______。
(3)NaCl分散在酒精中可形成胶体,则区别该分散系和氯化钠溶液最简单的方法是该分散系可出现_______。
(4)检验NaCl中是否含有,需选择的化学试剂及实验方法为_______。
A.加入浓溶液加热,观察现象 B.加稀HNO3和AgNO3溶液,观察现象
C.加入溶液,观察现象 D.滴加酚酞试液,观察现象
(5)写出①与水反应的化学方程式为_______。
(6)防烟面具中氧气的来源是过氧化钠,写出Na2O2与二氧化碳反应的化学方程式:_______。
(7)Na2CO3溶液中Na+的浓度为 0.3 mol•L-1,则该溶液中c(Na2CO3)_______ mol•L-1。
【答案】(1) ⑥ ③ ③④⑥⑦⑨⑩ O3
(2)
(3)丁达尔效应
(4)B
(5)
(6)
(7)0.15
【详解】(1)电解质是溶于水溶液中或在熔融状态下自身能够导电的化合物,一般为酸、碱、盐、典型的金属氧化物和某些非金属氢化物。
①Na是金属单质,既不是电解质也不是非电解质;②O2是非金属单质,既不是电解质也不是非电解质;③H2SO4为酸,属于电解质;④KOH是碱,属于电解质;⑤蔗糖不能电离、不能导电,属于非电解质;⑥H2O是氧化物,能电离,属于电解质;⑦NaCl为盐,溶于水导电,属于电解质;⑧空气是混合物,既不是电解质也不是非电解质;⑨NaHSO4为盐,属于电解质;⑩Na2CO3为盐,属于电解质;
氧化物是指氧元素与另外一种化学元素组成的二元化合物,上述物质中属于氧化物的是⑥H2O;电离时生成的阳离子全部是氢离子(H⁺)的化合物叫做酸,上述物质中属于酸的是③H2SO4;属于电解质的是③H2SO4、④KOH、⑥H2O、⑦NaCl、⑨NaHSO4、⑩Na2CO3;同素异形体是指由同样的单一化学元素组成,因排列方式不同,而具有不同性质的单质,O2是由氧元素形成的单质,与O2互为同素异形体的为O3,故答案为:⑥;③;③④⑥⑦⑨⑩;O3。
(2)③H2SO4为酸,在水溶液中电离出H+和,电离方程式为。
(3)当一束光线透过胶体,从垂直入射光方向可以观察到胶体里出现的一条光亮的“通路”,因此鉴别胶体与溶液最简单的方法是利用丁达尔效应。
(4)A.加入NaOH浓溶液加热,Cl-不反应,无明显现象,故A不选;
B.加稀HNO3和AgNO3溶液,Cl-与Ag+反应生成白色AgCl沉淀,可检验Cl-,故B选;
C.加入KSCN溶液,Cl-不反应,无明显现象,故C不选;
D.滴加酚酞试液,无明显现象,故D不选;
故答案为B。
(5)Na为活泼金属单质,能与水发生置换反应,反应方程式为。
(6)过氧化钠与二氧化碳发生氧化还原反应生成碳酸钠和氧气,反应方程式为。
(7)Na2CO3在水中完全电离出Na+、,Na2CO3溶液中Na+的浓度为 0.3 mol•L-1,则该溶液中c(Na2CO3)=。
三、元素或物质推断题
14.某无色透明溶液中可能大量存在Ag+、Ca2+、Cu2+、Fe3+、Na+中的几种。请填写下列空白:
(1)不做任何实验就可以肯定原溶液中不存在的离子是___________。
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。说明原溶液中肯定存在的离子是___________。
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,说明原溶液中肯定有___________,有关的离子方程式为___________。
(4)原溶液可能大量共存的阴离子是___________(填字母)。
A.OH- B.SO C.NO D.Cl-
【答案】(1)Cu2+、Fe3+
(2)Ag+
(3) Ca2+ Ca2++CO=CaCO3↓
(4)C
【详解】(1)含有Fe3+的溶液呈黄色,含有Cu2+的溶液呈蓝色;无色溶液中一定不含Cu2+、Fe3+;所以不做任何实验就可以肯定原溶液中不存在的离子是Cu2+、Fe3+;
(2)取少量原溶液,加入过量稀盐酸,有白色沉淀生成;再加入过量的稀硝酸,沉淀不消失。,说明原溶液中肯定存在的离子是Ag+;
(3)取(2)中的滤液,加入过量的碳酸钠溶液,出现白色沉淀,,所以说明原溶液中肯定有Ca2+;
(4)A. OH-与Ag+反应生成沉淀,氢氧化钙微溶, OH-与Ca2+、Ag+不能大量共存,故不选A;
B. 硫酸银、硫酸钙微溶,SO与Ca2+、Ag+不能大量共存,故不选B;
C. NO与Ag+、Ca2+、Na+不反应,能大量共存,故选C;
D. Cl-与Ag+反应生成氯化银沉淀,不可能含有Cl-,故不选D;
选C。
四、实验题
15.下图为实验室制取纯净、干燥的氯气,并验证氯气性质的装置。其中E瓶放有干燥红色布条,F中为红色的铜网,其右端出气管口放有脱脂棉。
(1)瑞典化学家舍勒将软锰矿(主要成分是MnO2)与浓盐酸混合加热,在世界上首先取得了氯气。目前实验室依然采用此法制取氯气,请写出化学方程式:_______。
(2)装置C中盛装的溶液是_______,D的作用是_______。
(3)E中红色布条是否褪色?_______,原因是_______;F中的生成物质为_______。(化学式)
(4)若H中选用NaOH溶液进行尾气处理,则发生的反应是(用离子方程式表示)_______。
(5)实验结束时,应先熄灭_______(填“①”或“②”)处酒精灯。
【答案】(1)
(2) 饱和食盐水 干燥氯气
(3) 不褪色 氯气不具有漂白性 CuCl2
(4)
(5)②
【分析】装置B中发生MnO2与浓盐酸在加热的条件下反应,生成氯化锰、氯气、水,方程式为,浓盐酸具有挥发性导致生成的氯气中含有HCl,装置C除去氯气中的HCl,氯气在饱和食盐水中溶解度较低,因此除杂试剂是饱和食盐水;装置D是干燥氯气,干燥剂是浓硫酸,装置E中放有干燥红色布条,布条不褪色,装置F中为红色的铜网,加热条件下,发生反应,右端出气管口放有脱脂棉,防止生成的CuCl2冷却后堵塞导管,装置G采用向上排空法收集氯气,装置H盛有氢氧化钠溶液,吸收多余的氯气,防止污染空气。
【详解】(1)由上述分析可知,制取氯气的化学方程式为。
(2)由上述分析可知,装置C中盛装的溶液是饱和食盐水;因装置F为加热装置,不能让水蒸气进入,因此装置D的作用是干燥氯气。
(3)氯气不具有漂白性,因此装置E中红色布条不会褪色;装置F中氯气与铜在加热条件下发生化合反应生成CuCl2。
(4)Cl2与NaOH溶液发生歧化反应生成氯化钠、次氯酸钠、水,反应的离子方程式为。
(5)实验结束后,应先熄灭②处酒精灯,防止发生倒吸。
16.在疫情防控中,常使用次氯酸钠溶液对环境消毒。已知某“84消毒液”瓶体部分标签如图所示。请回答下列问题:
商品名称:84消毒液 【有效成分】NaClO 【NaClO摩尔质量】74.5g/mol 【规格】500mL 【质量分数】7.45% 【密度】约为1 g/mL |
(1)该“84消毒液”的物质的量浓度为_______mol•L-1。
(2)小明某次实验需要配置该浓度的“84消毒液” 950 mL,需选用的容量瓶规格为_______mL,小明需用托盘天平称量该固体的质量为_______g。
(3)以下有关配制该溶液的说法正确的是_______(填字母)。
① | ② | ③ |
A.定容时的操作如图①所示
B.溶解NaClO固体不能用如图②所示的操作
C.定容操作可以用图③表示
D.定容过程向容量瓶加蒸馏水至接近刻度线1—2cm时,改胶头滴管滴加蒸馏水至刻度线
(4)下列情况会导致所配制的“84消毒液”的物质的量浓度偏高的是_______(填字母)。
A.容量瓶用蒸馏水洗后未干燥
B.配制过程中未洗涤烧杯和玻璃棒
C.定容时俯视刻度线
D.称量NaClO固体时所用的砝码生锈了
【答案】(1)1
(2) 1000 74.5
(3)BD
(4)CD
【详解】(1)该“84消毒液”的物质的量浓度。
(2)配制950mL溶液需选用1000mL容量瓶定容;配制1L1mol/L NaClO溶液需称量NaClO固体质量为。
(3)A.定容操作视线与刻度线相平,图示操作错误,故A错误;
B.容量瓶不能用于溶解固体,应在烧杯中溶解,故B正确;
C.定容操作最后应用胶头滴管逐滴滴加,图示操作错误,故C错误;
D.定容过程中向容量瓶内加蒸馏水至接近刻度线1~2cm时,改用胶头滴管滴加蒸馏水至刻废线,故D正确;
故答案为:BD。
(4)所配溶液浓度,根据操作对数据影响分析对结果的影响。
A.定容过程中还需向容量瓶中加入蒸馏水,容量瓶用蒸馏水洗后未干燥,对溶质的物质的量和溶液体积都不产生影响,溶液浓度无影响,故A不选;
B.配制过程中未洗涤烧杯和玻璃棒,导致溶质部分损耗,溶质的物质的量浓度偏低,故B不选;
C.定容时俯视刻度线,导致溶液体积偏小,溶液浓度偏高,故C选;
D.称量NaClO固体时所用的砝码生锈了,所称量固体质量偏大,导致溶质的物质的量偏大,溶液浓度偏高,故D选;
故答案为:CD。
【期中真题】天津市八校联考2022-2023学年高一上学期期中考试化学试题.zip: 这是一份【期中真题】天津市八校联考2022-2023学年高一上学期期中考试化学试题.zip,文件包含期中真题天津市八校联考2022-2023学年高一上学期期中考试化学试题原卷版docx、期中真题天津市八校联考2022-2023学年高一上学期期中考试化学试题解析版docx等2份试卷配套教学资源,其中试卷共17页, 欢迎下载使用。
2022-2023学年河北省邢台市六校联考高一上学期期中考试化学试题含解析: 这是一份2022-2023学年河北省邢台市六校联考高一上学期期中考试化学试题含解析,共20页。试卷主要包含了单选题,多选题,实验题,填空题等内容,欢迎下载使用。
2022-2023学年天津市八校联考高三上学期期中考试化学试题含解析: 这是一份2022-2023学年天津市八校联考高三上学期期中考试化学试题含解析,共17页。试卷主要包含了单选题,元素或物质推断题,填空题,实验题等内容,欢迎下载使用。












