






还剩26页未读,
继续阅读
鲁教版(五四制)九年级化学 第2单元 整理与复习 课件
展开
这是一份鲁教版(五四制)九年级化学 第2单元 整理与复习 课件,共34页。
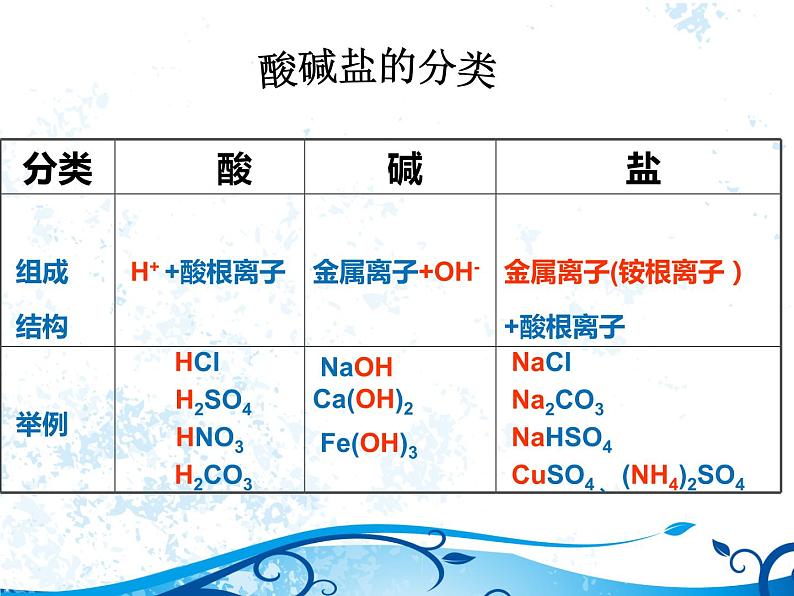
初四 化学 九年级《酸碱盐化学性质》专题复习醋 酸宏观、微观和化学符号三重表征有机结合,是化学学科特有的思维方式宏观:食盐这种物质氯化钠由钠元素、氯元素组成微观:由Na+ 、Cl-构成化学符号:NaCl醋 酸从微观的角度分析: 将物质分类为酸碱盐,其分类的依据是什么?酸碱盐的分类将氢氧化钠分类为碱你运用了哪种科学方法?常见的科学方法:归纳与演绎归纳是从个别到一般的推理方法,即从许多个别事实中概括出一般原理。演绎是从一般到个别的推理方法,即用已知的一般原理考察某一特殊的对象,推演出有关这个对象的结论标目习学1、学会用归纳与演绎等科学方法理解酸碱盐的化学性质,构建酸碱盐知识体系. 2.会用化学方程式表示常见酸碱盐的化学变化,能初步了解复分解反应的实质,能将宏观世界、微观世界和化学符号三重表征有机联系,理解宏观的化学变化是由于构成物质的粒子重新组合的结果,形成微粒观、变化观。3、明确认识物质的角度应从物质的组成、结构、性质及应用等方面,形成物质的组成结构决定性质,性质决定用途的科学的物质观。益广思集 实验教师在整理药品时,有两瓶试剂因标签被腐蚀,无法正确归橱,一瓶是稀盐酸,一瓶是氢氧化钙溶液,你能帮老师鉴别出来吗?小组讨论,看看哪组同学想的办法多。描述实验现象和结论请各小组将不同方案所用到的物质以盐酸和氢氧化钙为核心画出脉络图。 【帮老师解决问题】酸的化学性质1、酸+酸碱指示剂2、酸+某些活泼金属 →盐+氢气3、酸+金属氧化物→盐+水 4、酸+碱→盐+水5、酸+某些盐→新酸+新盐酸的通性总结提升:探究物质的化学性质可以采用分类的思想:从不同类别的物质中选用代表物质进行探究。微观解释酸的通性1、Fe+ 2HCl = FeCl2 + H2↑2、Fe2O3+ 6HCl = 2FeCl3+ 3H2O3、2NaOH + H2SO4 = Na2SO4 +2H2O4、Na2CO3+2HCl = 2NaCl + H2O +CO2↑ Cl-、SO42-在反应前后依然自由移动,并没有真正参与反应。H+氢离子在反应前自由移动,反应后进入氢分子、水分子,不能自由移动了, H+真正参与反应,体现酸的通性。酸的特性① HCl +AgNO3= HNO3 +AgCl↓②H2SO4+BaCl2 =2HCl +BaSO4↓H+在反应前后依然自由移动,并没有真正参与反应,反应不体现酸的通性。Cl-、SO42-在反应前自由移动,反应后进入生成的沉淀中,真正参与反应,体现个别酸的特性。碱的化学性质1、碱+酸碱指示剂2、碱+非金属氧化物→盐+水3、碱+酸→盐+水4、碱+某些盐→新碱+新盐碱的通性Ca(OH)2 +CuCl2 =CaCl2+ Cu(OH)2↓Ca(OH)2+ Na2CO3 =2NaOH+ CaCO3↓OH-在反应前自由移动,反应后转化为沉淀,真正参与反应,体现碱的通性。Ca2+在反应前自由移动,反应后进入生成的沉淀中,真正参与反应,体现个别碱的特性。益广思集你能帮妈妈在厨房里鉴别纯碱和氯化钠吗?实验室里你能用更多的方法来鉴别吗?写出相关反应方程式. 【帮妈妈解决问题】1、盐+酸→新盐+新酸Na2 CO3 + 2HCl =2 NaCl+ H2O + CO2↑盐的化学性质2、可溶性盐+可溶性碱→新盐+新碱 Na2 CO3 + Ca(OH)2= CaCO3 ↓+ 2 NaOH3、可溶性盐+可溶性盐→ 新盐+新盐 NaCl + AgNO3 =AgCl↓+ NaNO3 Na2 CO3 + BaCl2 = BaCO3↓ + 2 NaCl4、可溶性盐+金属→金属+盐CuSO4+ Fe = Cu + FeSO41、下图是酸与不同类别物质之间反应的知识网络图。(1)图中A若代表金属氧化物,请举一个例子______。 (2)举例写出金属与稀H2SO4反应的化学方程式:____(3)酸能除铁锈,写出稀硫酸除铁锈的化学方程式:_______;B代表______(填物质的类别)。(4)酸有一些相似的化学性质,是因为在不同的酸溶液中都含有相同的 _____(填离子符号)。练习提升:2、小红同学用下图总结了NaOH的四条化学性质I.依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:________________________II.为了验证反应③能够发生,你选择的物质是____________a.Na2CO3 b.HCl c.CuCl2 d.Ba(NO3)2练习提升:点拨释疑2NaOH +CuCl2 =2NaCl+ Cu(OH)2↓ 2NaOH+Ba(NO3)2=2NaNO3+ Ba(OH)2↓Na+、OH-、Ba2+、NO3-、复分解反应发生的条件1.酸 + 碱 → 盐 + 水2.酸 + 金属氧化物 →盐 + 水3.酸 + 盐 → 新酸 + 新盐4.碱 + 盐 → 新碱+ 新盐 5.盐 + 盐 → 新盐+另一种新盐生成物有沉淀、气体或水反应物:如果没有酸参加则反应物都要可溶或微溶.归纳本质原因:溶液中自由移动的离子数目减少1、下列不属于复分解反应的是( )A、CuO+2HCl =CuCl2+ H2O B、Na2CO3+2HCl=2NaCl+H2O+ CO2 ↑ C、 Ca(OH)2 + CO2 = CaCO3↓ + H2O D、Cu(OH)2+2HCl=CuCl2+ 2H2O 2、写出下列反应的实质(用符号表示)(1)HCl+ NaOH = NaCl +H2O(2)Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑(3)Ca(OH)2+ Na2CO3 =2NaOH+ CaCO3↓跟踪练习:稀HCl或稀H2SO4产生气泡已变质澄清石灰水或Ba(OH)2溶液白色沉淀已变质BaCl2 溶液或Ba(NO3)2溶液白色沉淀已变质典例剖析 小丽带着快乐的心情来到实验室时,意外地发现实验桌上有瓶敞口放置已久的NaOH溶液。由此,激发了她的探究欲望。 (1) “这瓶NaOH溶液是否变质了呢?” 请大家帮助小丽选择三种不同类别(酸、碱、盐)的试剂进行实验。取少量NaOH溶液样品于试管中,先滴加足量的BaCl2溶液或Ba(NO3)2溶液;白色沉淀存在Na2CO3,NaOH溶液已变质再过滤,向滤液中滴加无色酚酞试液。溶液变红存在NaOH,NaOH溶液部分变质 (2)“这瓶NaOH溶液的变质程度如何呢?” 小丽猜想NaOH溶液部分变质,请大家帮助 小丽设计实验方案。益广思集某硫酸厂环保监测不达标,原因是废气中的二氧化硫及废水中的硫酸超标,你能帮助厂主想个金点子吗? 【帮厂主解决问题】【思考】若不及时对废气和废水进行处理, 将会产生什么危害?【问题】熟石灰改良酸性废水的原理是什么? 重要化学观念:组成结构性质用途 今天你智慧的背囊里都获取哪些宝藏?还存在哪些疑惑? 让我们一起来分享!感悟与收获标目习学1、学会用归纳与演绎等科学方法理解酸碱盐的化学性质,构建酸碱盐知识体系. 2.会用化学方程式表示常见酸碱盐的化学变化,能初步了解复分解反应的实质,能将宏观世界、微观世界和化学符号三重表征有机联系,理解宏观的化学变化是由于构成物质的粒子重新组合的结果,形成微粒观、变化观。3、明确认识物质的角度应从物质的组成、结构、性质及应用等方面,形成物质的组成结构决定性质,性质决定用途的科学的物质观。示1、2008年诺贝尔化学奖授予发明和研究绿色荧光蛋白的三位科学家。绿色荧光蛋白分子中含有氨基(-NH2,具有碱的性质)和羧基(-COOH,具有酸的性质)。则绿色荧光蛋白具有的性质是( )A.既能与盐酸反应,又能与氢氧化钠反应 B.只能与氢氧化钠反应,不能与盐酸反应C.只能与盐酸反应,不能与氢氧化钠反应D.既不能与盐酸反应,又不能与氢氧化钠反应示【2015威海】只有正确认识了物质,才能合理改造和应用物质.请你运用归纳/演绎、实验等科学方法认识氯化钠.(1)用归纳演绎法认识氯化钠的性质已知下列反应:HCl+AgNO3=AgCl↓+HNO3 MgCl2+2AgNO3=2AgCl↓+Mg(NO3)①上述反应属于四种基本反应类型中的______,运用(填“归纳”或“演绎”)______法得到这组反应发生的原因是______.②由①中得到的规律可以推测“氯化钠溶液也能跟硝酸银溶液反应”,运用的是(填“归纳”或“演绎”)______法.(2)用实验法认识氯化钠的性质①要验证(1)②中“氯化钠溶液也能跟硝酸银溶液反应”的推断,需要进行实验,实验方法是______,反应的化学方程式是______. 【链接中考】地展能学3、2011年是国际化学年,主题是“化学——人类的生活,人类的未来。”下表列出了几种与人类省会和未来密切相关的物质:(1)请按要求填写表格:物质名称烧碱盐酸硫酸铜熟石灰干冰石油物质组成(用化学式表示)构成微粒(用符号表示)(2)从上表选择两种物质,说明其与人类生活的密切关系:________________________________,___________________。(3)在(2)中两种物质分别利用了物质的哪些性质?________________________________,____________________。(4)上述6种物质中属于同一类的两种物质是________________,从物质的组成和结构的角度分析,原因是_________________________。(5)从上表选择两种能发生复分解反应的物质,写出其反应的化学方程式:______________________________________________。地学校实验室的废液缸中收集了学生在实验室制取CO2后残留的废液。[提出问题]废液中的溶质是什么物质?[作出猜想]小红认为废液中溶质只有CaCl2。你认为还可能含有的溶质是 。[查阅资料]CaCl2溶液呈中性。[实验与结论](1)小红取少量CaCl2溶液和废液分别加入到两支试管中,并向其中分别滴入无色酚酞试液作对比实验,结果两试管中溶液均无色,于是小红认为自己的猜想是正确的。(2)你认为小红的实验 (填“能”或“不能”)证明她的猜想,理由是 。(3)如果要证明你的猜想是正确的,你选择的试剂是 ,实验中可以看到的现象是 。谢谢大家
初四 化学 九年级《酸碱盐化学性质》专题复习醋 酸宏观、微观和化学符号三重表征有机结合,是化学学科特有的思维方式宏观:食盐这种物质氯化钠由钠元素、氯元素组成微观:由Na+ 、Cl-构成化学符号:NaCl醋 酸从微观的角度分析: 将物质分类为酸碱盐,其分类的依据是什么?酸碱盐的分类将氢氧化钠分类为碱你运用了哪种科学方法?常见的科学方法:归纳与演绎归纳是从个别到一般的推理方法,即从许多个别事实中概括出一般原理。演绎是从一般到个别的推理方法,即用已知的一般原理考察某一特殊的对象,推演出有关这个对象的结论标目习学1、学会用归纳与演绎等科学方法理解酸碱盐的化学性质,构建酸碱盐知识体系. 2.会用化学方程式表示常见酸碱盐的化学变化,能初步了解复分解反应的实质,能将宏观世界、微观世界和化学符号三重表征有机联系,理解宏观的化学变化是由于构成物质的粒子重新组合的结果,形成微粒观、变化观。3、明确认识物质的角度应从物质的组成、结构、性质及应用等方面,形成物质的组成结构决定性质,性质决定用途的科学的物质观。益广思集 实验教师在整理药品时,有两瓶试剂因标签被腐蚀,无法正确归橱,一瓶是稀盐酸,一瓶是氢氧化钙溶液,你能帮老师鉴别出来吗?小组讨论,看看哪组同学想的办法多。描述实验现象和结论请各小组将不同方案所用到的物质以盐酸和氢氧化钙为核心画出脉络图。 【帮老师解决问题】酸的化学性质1、酸+酸碱指示剂2、酸+某些活泼金属 →盐+氢气3、酸+金属氧化物→盐+水 4、酸+碱→盐+水5、酸+某些盐→新酸+新盐酸的通性总结提升:探究物质的化学性质可以采用分类的思想:从不同类别的物质中选用代表物质进行探究。微观解释酸的通性1、Fe+ 2HCl = FeCl2 + H2↑2、Fe2O3+ 6HCl = 2FeCl3+ 3H2O3、2NaOH + H2SO4 = Na2SO4 +2H2O4、Na2CO3+2HCl = 2NaCl + H2O +CO2↑ Cl-、SO42-在反应前后依然自由移动,并没有真正参与反应。H+氢离子在反应前自由移动,反应后进入氢分子、水分子,不能自由移动了, H+真正参与反应,体现酸的通性。酸的特性① HCl +AgNO3= HNO3 +AgCl↓②H2SO4+BaCl2 =2HCl +BaSO4↓H+在反应前后依然自由移动,并没有真正参与反应,反应不体现酸的通性。Cl-、SO42-在反应前自由移动,反应后进入生成的沉淀中,真正参与反应,体现个别酸的特性。碱的化学性质1、碱+酸碱指示剂2、碱+非金属氧化物→盐+水3、碱+酸→盐+水4、碱+某些盐→新碱+新盐碱的通性Ca(OH)2 +CuCl2 =CaCl2+ Cu(OH)2↓Ca(OH)2+ Na2CO3 =2NaOH+ CaCO3↓OH-在反应前自由移动,反应后转化为沉淀,真正参与反应,体现碱的通性。Ca2+在反应前自由移动,反应后进入生成的沉淀中,真正参与反应,体现个别碱的特性。益广思集你能帮妈妈在厨房里鉴别纯碱和氯化钠吗?实验室里你能用更多的方法来鉴别吗?写出相关反应方程式. 【帮妈妈解决问题】1、盐+酸→新盐+新酸Na2 CO3 + 2HCl =2 NaCl+ H2O + CO2↑盐的化学性质2、可溶性盐+可溶性碱→新盐+新碱 Na2 CO3 + Ca(OH)2= CaCO3 ↓+ 2 NaOH3、可溶性盐+可溶性盐→ 新盐+新盐 NaCl + AgNO3 =AgCl↓+ NaNO3 Na2 CO3 + BaCl2 = BaCO3↓ + 2 NaCl4、可溶性盐+金属→金属+盐CuSO4+ Fe = Cu + FeSO41、下图是酸与不同类别物质之间反应的知识网络图。(1)图中A若代表金属氧化物,请举一个例子______。 (2)举例写出金属与稀H2SO4反应的化学方程式:____(3)酸能除铁锈,写出稀硫酸除铁锈的化学方程式:_______;B代表______(填物质的类别)。(4)酸有一些相似的化学性质,是因为在不同的酸溶液中都含有相同的 _____(填离子符号)。练习提升:2、小红同学用下图总结了NaOH的四条化学性质I.依据反应④说明NaOH必须密封保存,否则在空气中要变质,其化学反应方程式为:________________________II.为了验证反应③能够发生,你选择的物质是____________a.Na2CO3 b.HCl c.CuCl2 d.Ba(NO3)2练习提升:点拨释疑2NaOH +CuCl2 =2NaCl+ Cu(OH)2↓ 2NaOH+Ba(NO3)2=2NaNO3+ Ba(OH)2↓Na+、OH-、Ba2+、NO3-、复分解反应发生的条件1.酸 + 碱 → 盐 + 水2.酸 + 金属氧化物 →盐 + 水3.酸 + 盐 → 新酸 + 新盐4.碱 + 盐 → 新碱+ 新盐 5.盐 + 盐 → 新盐+另一种新盐生成物有沉淀、气体或水反应物:如果没有酸参加则反应物都要可溶或微溶.归纳本质原因:溶液中自由移动的离子数目减少1、下列不属于复分解反应的是( )A、CuO+2HCl =CuCl2+ H2O B、Na2CO3+2HCl=2NaCl+H2O+ CO2 ↑ C、 Ca(OH)2 + CO2 = CaCO3↓ + H2O D、Cu(OH)2+2HCl=CuCl2+ 2H2O 2、写出下列反应的实质(用符号表示)(1)HCl+ NaOH = NaCl +H2O(2)Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑(3)Ca(OH)2+ Na2CO3 =2NaOH+ CaCO3↓跟踪练习:稀HCl或稀H2SO4产生气泡已变质澄清石灰水或Ba(OH)2溶液白色沉淀已变质BaCl2 溶液或Ba(NO3)2溶液白色沉淀已变质典例剖析 小丽带着快乐的心情来到实验室时,意外地发现实验桌上有瓶敞口放置已久的NaOH溶液。由此,激发了她的探究欲望。 (1) “这瓶NaOH溶液是否变质了呢?” 请大家帮助小丽选择三种不同类别(酸、碱、盐)的试剂进行实验。取少量NaOH溶液样品于试管中,先滴加足量的BaCl2溶液或Ba(NO3)2溶液;白色沉淀存在Na2CO3,NaOH溶液已变质再过滤,向滤液中滴加无色酚酞试液。溶液变红存在NaOH,NaOH溶液部分变质 (2)“这瓶NaOH溶液的变质程度如何呢?” 小丽猜想NaOH溶液部分变质,请大家帮助 小丽设计实验方案。益广思集某硫酸厂环保监测不达标,原因是废气中的二氧化硫及废水中的硫酸超标,你能帮助厂主想个金点子吗? 【帮厂主解决问题】【思考】若不及时对废气和废水进行处理, 将会产生什么危害?【问题】熟石灰改良酸性废水的原理是什么? 重要化学观念:组成结构性质用途 今天你智慧的背囊里都获取哪些宝藏?还存在哪些疑惑? 让我们一起来分享!感悟与收获标目习学1、学会用归纳与演绎等科学方法理解酸碱盐的化学性质,构建酸碱盐知识体系. 2.会用化学方程式表示常见酸碱盐的化学变化,能初步了解复分解反应的实质,能将宏观世界、微观世界和化学符号三重表征有机联系,理解宏观的化学变化是由于构成物质的粒子重新组合的结果,形成微粒观、变化观。3、明确认识物质的角度应从物质的组成、结构、性质及应用等方面,形成物质的组成结构决定性质,性质决定用途的科学的物质观。示1、2008年诺贝尔化学奖授予发明和研究绿色荧光蛋白的三位科学家。绿色荧光蛋白分子中含有氨基(-NH2,具有碱的性质)和羧基(-COOH,具有酸的性质)。则绿色荧光蛋白具有的性质是( )A.既能与盐酸反应,又能与氢氧化钠反应 B.只能与氢氧化钠反应,不能与盐酸反应C.只能与盐酸反应,不能与氢氧化钠反应D.既不能与盐酸反应,又不能与氢氧化钠反应示【2015威海】只有正确认识了物质,才能合理改造和应用物质.请你运用归纳/演绎、实验等科学方法认识氯化钠.(1)用归纳演绎法认识氯化钠的性质已知下列反应:HCl+AgNO3=AgCl↓+HNO3 MgCl2+2AgNO3=2AgCl↓+Mg(NO3)①上述反应属于四种基本反应类型中的______,运用(填“归纳”或“演绎”)______法得到这组反应发生的原因是______.②由①中得到的规律可以推测“氯化钠溶液也能跟硝酸银溶液反应”,运用的是(填“归纳”或“演绎”)______法.(2)用实验法认识氯化钠的性质①要验证(1)②中“氯化钠溶液也能跟硝酸银溶液反应”的推断,需要进行实验,实验方法是______,反应的化学方程式是______. 【链接中考】地展能学3、2011年是国际化学年,主题是“化学——人类的生活,人类的未来。”下表列出了几种与人类省会和未来密切相关的物质:(1)请按要求填写表格:物质名称烧碱盐酸硫酸铜熟石灰干冰石油物质组成(用化学式表示)构成微粒(用符号表示)(2)从上表选择两种物质,说明其与人类生活的密切关系:________________________________,___________________。(3)在(2)中两种物质分别利用了物质的哪些性质?________________________________,____________________。(4)上述6种物质中属于同一类的两种物质是________________,从物质的组成和结构的角度分析,原因是_________________________。(5)从上表选择两种能发生复分解反应的物质,写出其反应的化学方程式:______________________________________________。地学校实验室的废液缸中收集了学生在实验室制取CO2后残留的废液。[提出问题]废液中的溶质是什么物质?[作出猜想]小红认为废液中溶质只有CaCl2。你认为还可能含有的溶质是 。[查阅资料]CaCl2溶液呈中性。[实验与结论](1)小红取少量CaCl2溶液和废液分别加入到两支试管中,并向其中分别滴入无色酚酞试液作对比实验,结果两试管中溶液均无色,于是小红认为自己的猜想是正确的。(2)你认为小红的实验 (填“能”或“不能”)证明她的猜想,理由是 。(3)如果要证明你的猜想是正确的,你选择的试剂是 ,实验中可以看到的现象是 。谢谢大家
相关资料
更多









