






2021学年第四单元 金属2 金属的化学性质示范课ppt课件
展开利用金属的哪些物理性质可以鉴别黄金、黄铜(Cu-Zn合金)?
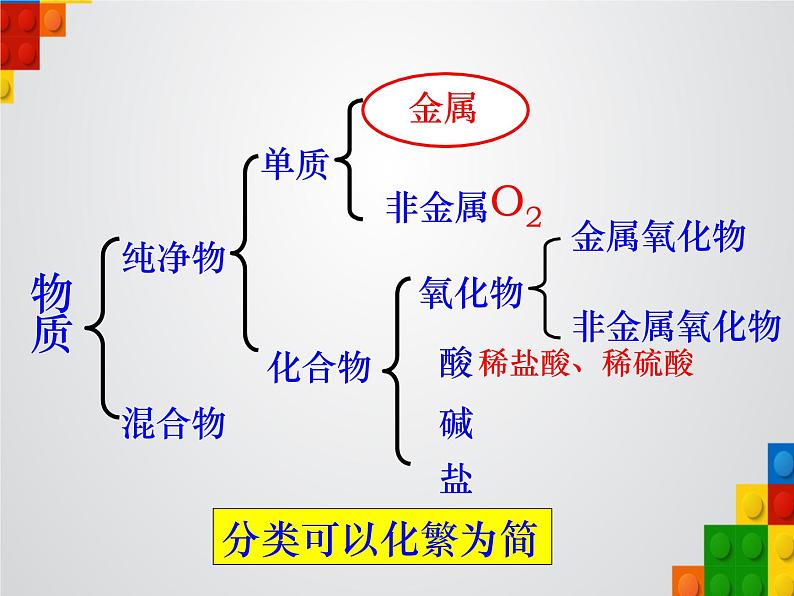
金属能与哪些物质发生反应呢?
金属氧化物非金属氧化物
铝片 (能或不能)燃烧
发出白光,放热,生成白色固体
常温下易被氧化表面生成一层氧化膜。
剧烈燃烧,火星四射,放热,生成黑色固体
剧烈燃烧,发出白光,放热,生成白色固体。
燃烧更加剧烈,发出白光,放热,生成白色固体。
。.。
。.。
为什么铝粉在氧气中燃烧,而铝片不能在氧气中燃烧呢?
请写出镁、铁、铜、铝与氧气反应的化学方程式
金属与氧气反应的难易和剧烈程度受哪些因素影响?
金属与氧气反应的难易和剧烈程度的影响因素
铝在常温下就很容易跟氧气发生反应,生成一层致密而坚固的氧化铝薄膜,可以阻止内层的铝进一步氧化,起到保护作用。
生活中铝制品表面的污渍能不能用钢丝球打磨?为什么?(钢丝球主要成分是铁,硬度较大,拥有强大的摩擦力所以一般用于表面不容易被摩坏的物质 )
不能,会破坏铝制品表面致密而坚固的氧化膜,使铝制品进一步被腐蚀。
铝与氧气常温生成致密坚固的氧化膜
镁与氧气反应:燃烧有强光
“真金不怕火炼”
金属都能与氧气反应吗?
金属与酸反应的难易和剧烈程度有差异吗?
设计方案思考:1. 选择哪些药品? 2. 哪些因素会影响金属与酸反应的速率?
探究未知金属X、铁、铜与酸反应的难易及剧烈程度
药品: 铁粉、铁丝、铜丝、未知金属丝、 5%稀盐酸、 10%稀盐酸、10%硫酸仪器和用品:试管、砂纸
你会区分铁丝、铜丝吗?
3. 观察什么现象来获得结论?
实验方案:1、取两滴管的同浓度、同种酸于三支试管中。2、用砂纸打磨金属丝。3、将打磨好的金属丝同时插入三支试管中,对比观察实验现象
1.请用砂纸打磨金属丝,除去金属表面的氧化膜。2.稀盐酸、稀硫酸有腐蚀性,使用时请注意安全。3.请注意观察金属丝表面是否产生气泡以及产生气泡的速率,并观察溶液颜色是否发生变化。4.要注意控制变量,例如:酸的浓度、酸的种类、金属与酸的接触面积。
有气泡产生,且产生气泡较慢
有气泡产生,且产生气泡较快
由一种单质与一种化合物反应,生成另一种单质与另一种化合物
Na2CO3+Ca(OH)2=CaCO3↓+2NaOH
Fe+2HCl = FeCl2+H₂
4Al+3O2=2Al2O3
2Al2O3= 4Al+3O2↑
下列反应是哪些基本反应类型?分类的依据是什么?
Fe+H2SO4 = FeSO4+H₂
Fe+2HCl =FeCl2+H₂
物质种类 物质类别
Fe2O3+3CO 2Fe+3CO2
1.能与稀盐酸、稀硫酸反应的金属是 不能与稀盐酸,稀硫酸反应的金属是 。2.能反应的金属反应剧烈程度依次是 > 。 3.X、铁、铜三种金属的反应剧烈程度顺序是是 > > 。
X Fe Cu
1865年,贝开托夫在实验的基础上首先确定了金属活动性顺序。因为氢可以被位于它前面的金属从稀酸里置换出来,而氢后面的金属不能从酸中置换出氢。贝开托夫当时区分金属的活泼与不活泼,是以氢作为标准的。
K Ca Na Mg Sn Pb
能与酸溶液反应产生氢气
资料链接: 已知铝丝和等量、等浓度、同种酸反应,产生气泡的速率比未知金属丝X快。
Hg Ag Pt Au
2.排在氢前面的金属能与酸反应放出氢气,而排在后面的金属不能与酸反应放出氢气。
K Ca Na Mg Al Zn Fe Sn Pb(H) Cu Hg Ag Pt Au
强————————————弱
1.金属的位置越靠前,活动性就越强。
金属活动性顺序表能表示什么意义呢?
以铁和稀硫酸反应为例:1、铁原子____(得到/失去)电子变成______。 2、稀硫酸中的H+____(得到/失去)电子变成___, 然后结合成______逸出。
1、铁原子_____(得到/失去)电子变成_________。 2、稀硫酸中的H+_____(得到/失去)电子变成______,然后结合成______逸出。
共性的微观原因: 金属原子都 ______________。
差异性的微观原因:金属原子 _____________不同。
舌尖上的中国:章丘铁锅
国内贫血发生率较高,特别儿童贫血约占50%。要让铁锅溶出铁质,在锅中加入酸性物质,这样会使活性铁的吸收量增加十倍。因此,用铁锅烹饪食物时,番茄酱、醋和柠檬都是最好的调味料。
世界卫生组织推荐使用传统中国铁锅
1.水处理,絮凝净化水2.医药上,治贫血症3.农业上,促使叶绿素形成
鉴别方法:黄金与黄铜(铜、锌合金)
K Ca Na Mg Al Zn Fe Sn Pb(H)Cu Hg Ag Pt Au
最外层电子数小于4,易失电子
结构决定性质,性质决定用途
本节课是怎样获得金属活动性顺序的?
金属与酸溶液反应,观察反应的难易及剧烈程度。
观察法 实验法控制变量法
化繁为简
为新时代喝彩!为伟大的祖国点赞!
初中化学鲁教版 (五四制)九年级全册2 金属的化学性质备课课件ppt: 这是一份初中化学鲁教版 (五四制)九年级全册2 金属的化学性质备课课件ppt,共25页。PPT课件主要包含了动脑筋,--金属活动性顺序,动脑回顾,一金属与氧气的反应,交流展示,倒入稀盐酸HCl,结论金属活动性,CuAg,不反应,猜想正确等内容,欢迎下载使用。
初中化学鲁教版 (五四制)九年级全册2 金属的化学性质教学演示课件ppt: 这是一份初中化学鲁教版 (五四制)九年级全册2 金属的化学性质教学演示课件ppt,共16页。PPT课件主要包含了本节目录,学习目标,本节课的重难点,新课导入,金属与氧气反应,学习新课,自己动手哦,④实验现象,锌铁铜,无明显现象等内容,欢迎下载使用。
初中化学鲁教版 (五四制)九年级全册2 金属的化学性质课前预习课件ppt: 这是一份初中化学鲁教版 (五四制)九年级全册2 金属的化学性质课前预习课件ppt,共28页。PPT课件主要包含了回顾与讨论,情景再现,铜丝在空气中加热,铜丝由红色变为黑色,实验现象,信息提示,交流共享,拓展延伸,*金属本身的性质,生活应用等内容,欢迎下载使用。













