






高中化学人教版 (2019)必修 第一册实验活动1 配制一定物质的量浓度的溶液精品课件ppt
展开在实验室中有一瓶氢气,我们应该如何得到该气体的物质的量呢?
我们已经学习了两个计算物质的量的公式
应用以上的公式是不是可以计算氢气的物质的量?
不可以,因为既不可能得到氢气的分子数,也不可能称量出氢气的质量
那么我们能得到氢气的什么物理量呢?
已知氢气的体积,能否求解氢气的物质的量?
根据摩尔质量的定义,你能不能说出摩尔体积的定义
单位物质的量的物质所具有的体积
可以得到物质的量的计算公式:
如何才能得到物质的摩尔体积呢?
摩尔体积就是指每1ml物质的体积,那么1ml铁的体积是多少呢?
1ml铁的质量为56g,其体积可以用质量除以密度得到:56g÷7.874g·cm-3=7.112cm3
由上述计算可以得到 即摩尔体积等于摩尔质量除以密度。
但是这种计算方法显然不是很方便,如何才能方便的得到摩尔体积呢?
宏观上讲,一种物质的摩尔体积就是每1ml该物质在空间上占据的体积,同学们能不能从微观上理解,什么是物质的摩尔体积?
微观上讲,物质的摩尔体积就是指NA个物质粒子在空间上所能占据的体积
二、影响物质摩尔体积的因素:
【思考与交流】摩尔体积就是每1ml物质的体积,或者说是大约6.02×1023个粒子在空间能占据的体积,这样一定数量的粒子在空间上能占据多大的体积由什么决定呢?请同学们互相交流讨论一下。
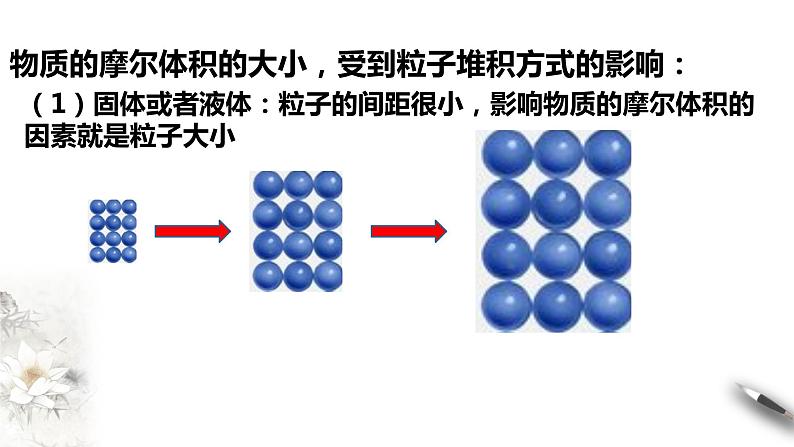
物质的摩尔体积的大小,受到粒子堆积方式的影响:
(1)固体或者液体:粒子的间距很小,影响物质的摩尔体积的因素就是粒子大小
铁和铜的摩尔体积为什么不一样?
这是因为铁原子和铜原子的大小不一样
显然我们不可能再根据粒子的大小来取得到物质的摩尔体积,所以研究固体和液体的摩尔体积就没有太大的意义。
(2)气体:粒子间距远大于粒子的直径,所以影响气体的摩尔体积的主要因素就是粒子间距
气体间距相同时,所有气体的摩尔体积是一样的
气体的粒子间距受什么物理量的影响?
气体间距相同时,所有气体的摩尔体积是一样的,所以气体间距相同时,气体摩尔体积与气体种类无关,研究气体摩尔体积就是有价值的
根据初中物理的学习,气体体积的变化就是因为气体的粒子间距在发生改变,气体的粒子间距与什么物理量相关?
相同温度和压强下,任何气体粒子的间距是相同的,所以一定具有相同的摩尔体积
相同温度和相同压强下,相同体积的任何气体一定具有相同的分子数(物质的量)
结论:同温同压下,任何气体一定具有相同的气体摩尔体积
同温同压下,任何气体一定具有相同的气体摩尔体积
1、阿伏加德罗定律:相同温度和相同压强下,相同体积的任何气体一定具有相同的分子数(物质的量)
【练习】 同温同压下,氢气和氧气的体积比为2:1,其物质的量的比为 。
2:1
推论:同温同压下,气体的体积比等于其物质的量的比
相同温度和相同压强下,质量相同的CO和CO2气体,其物质的量的比为 ,其体积比为 ,其密度比为 ,含有的氧原子数量比为 。
CO的摩尔质量为28g/ml,CO2的摩尔质量为44g/ml
设两者质量均为mg,则CO的物质的量为m/28 ml,CO2的物质的量为m/44 ml,物质的量的比为11:7
根据阿伏加德罗定律的推论,体积比等于物质的量的比,所以体积比也是11:7
两者质量相同,体积比为11:7,所以其密度比为体积比的反比,密度比为7:11
同学们可以理解:氯气密度大于空气,氢气密度小于空气
CO和CO2的物质的量的比为11:7,所以含有的氧原子数量比为1×11:2×7=11:14
2、标准状况下的气体摩尔体积:
一般规定0℃和101 kPa的条件为标准状况
标准状况下,任何气体的摩尔体积都约为22.4L/ml
【练习】填写下列空白(气体都处于标准状况):(1)0.1ml O2的体积为 L(2)3.36L的H2其质量为 g(3)1.12L的CH4中氢元素的质量为 g
高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量教学ppt课件: 这是一份高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第三节 物质的量教学ppt课件,共14页。PPT课件主要包含了数目不同,粒子大小不同,粒子间距离不同,a粒子的数目,b粒子的大小,c粒子间的距离,固体物质,液体物质,粒子间距离都很小,气体物质等内容,欢迎下载使用。
高中人教版 (2019)第三节 物质的量课文内容课件ppt: 这是一份高中人教版 (2019)第三节 物质的量课文内容课件ppt,共18页。PPT课件主要包含了不相等,物质体积的影响因素,气体摩尔体积,Vm特例,特别注意,阿伏伽德罗定律及推论,概念理解,不一定,均为气体,相同的条件等内容,欢迎下载使用。
高中化学必修一 专题2.3.2气体摩尔体积: 这是一份高中化学必修一 专题2.3.2气体摩尔体积,共22页。













