






初中化学人教版九年级下册课题 2 金属的化学性质教学演示课件ppt
展开1.大多数金属能与氧气反应生成________________,但反应的难易和剧烈程度不同。(1)镁、铝等金属在常温下能与氧气反应,其反应的化学方程式分别为:______________________________、_____________________。
2Mg+O2===2MgO
4Al+3O2===2Al2O3
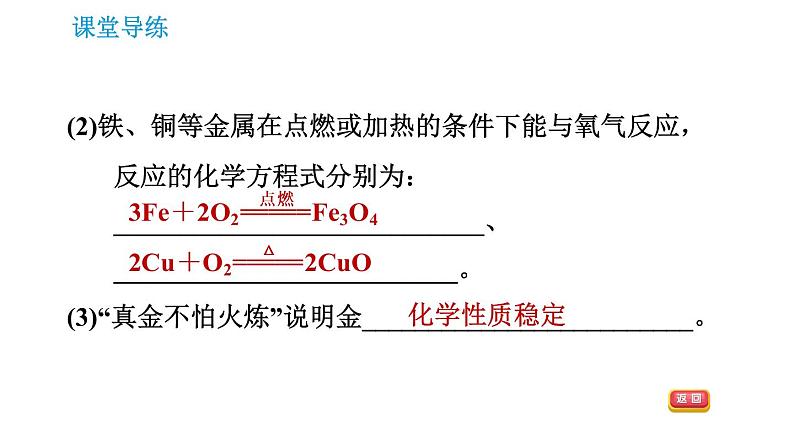
(2)铁、铜等金属在点燃或加热的条件下能与氧气反应,反应的化学方程式分别为:____________________________、__________________________。(3)“真金不怕火炼”说明金_________________________。
2.下列金属能在空气中燃烧的是( ) A.铜 B.银 C.镁 D.铁
3.清代的铝制佛像,至今仍能保存完好,铝制品不易锈蚀的原因是 ( ) A.铝的化学性质不活泼,在空气中不与氧气反应 B.铝在常温下不与氧气反应,在高温时才能反应 C.铝易被氧化,其表面的氧化膜有保护内部铝的作用 D.铝的氧化物易发生还原反应
4.下列关于金属与氧气反应的说法正确的是( ) A.所有的金属在常温下都能与氧气反应 B.金属与氧气反应都必须点燃或加热 C.铁在空气中燃烧,火星四射 D.铜在空气中加热,表面变黑
【点拨】本题采用举例法解答。不同的金属与氧气反应的条件是不同的,有的在常温下就能与氧气反应,如Al、Mg,有的需在点燃或加热的条件下才能反应,如Fe、Cu,有的即使在高温时也不能反应,如Au,故A、B错误;铁在空气中不能燃烧,故C错误;铜在空气中加热生成氧化铜,表面变黑,故D正确。。
5.将大小、形状相同的镁、锌、铁、铜放入稀硫酸中。(1)可观察到:表面没有气泡产生的是____________,反应结束后得到浅绿色溶液的是________,反应最剧烈且放出大量热的是________。
(2)写出镁、铝、锌、铁与稀硫酸反应的化学方程式。①______________________________________;②_______________________________________;③______________________________________;④____________________________________。
Fe+H2SO4===FeSO4+H2↑
Mg+H2SO4===MgSO4+H2↑
2Al+3H2SO4===Al2(SO4)3+3H2↑
Zn+H2SO4===ZnSO4+H2↑
6.(2020·北京)下列不能与稀盐酸反应的金属是( ) A.Cu B.Zn C.Al D.Mg
【点拨】Fe与盐酸反应生成FeCl2和H2。
8.向下列试管中分别加入稀盐酸,用序号填空:(1)其中没有气泡产生的是________,产生气泡速率最快的是________。
(2)写出④中发生反应的化学方程式____________________________,反应后得到的溶液呈________色。(3)由上述实验现象可知,四种金属活动性顺序为________________________________________。
Fe+2HCl===FeCl2+H2↑
Mg>Zn>Fe>Cu
9.由一种________与一种________反应,生成另一种________和另一种________的反应,叫做置换反应。注意:①有单质和化合物生成的反应______________(填“一定”或“不一定”,下同)是置换反应;②置换反应中____________有元素的化合价发生改变。
【点拨】B项的反应物是两种化合物,不属于置换反应,其余三个反应均属于置换反应。
11.按要求写出下列反应的化学方程式。(1)有气体单质生成的置换反应___________________________________________;(2)有铜生成的非置换反应___________________________________________;(3)有二氧化碳生成的置换反应__________________________________________。
12.(中考·贵州)关于下列实验现象,描述错误的是( ) A.光亮的铜丝放入稀硫酸中,溶液变为蓝色,产生大量气泡 B.镁条在空气中剧烈燃烧,发出耀眼的白光,生成白色固体 C.铁丝在氧气中剧烈燃烧,火星四射,生成黑色固体 D.将锌片、铁片分别放入相同浓度的稀盐酸中,锌片上产生气泡的速率比铁片快
【点拨】在金属活动性顺序中,铜位于氢的后面,故将铜丝放入稀硫酸中不能发生反应,没有气泡产生。
13.铁、镁、铝等金属在日常生活中都有广泛的用途。(1)镁在空气中燃烧能发出耀眼的白光,可以用来制造镁闪光灯。其反应的化学方程式为_______________________________。(2)铝制品有较强的抗腐蚀性,其原因是(用化学方程式表示)__________________________,日常生活中能不能用钢丝球等硬物擦拭铝制品?________。
(3)市售的补血麦片中常含有微量颗粒细小的还原性铁粉。铁粉可与胃液中的少量盐酸反应,生成可溶于水的氯化亚铁而被人体吸收,从而达到“补血”的作用,其中有关反应的化学方程式是____________________________________________。
14.(中考·铁岭)下列金属化合物可由金属和盐酸反应直接制得的是( ) A.CuCl2 B.AlCl3 C.FeCl3 D.AgCl
【点拨】在金属活动性顺序中,Cu、Ag位于H后,不能与稀盐酸反应直接制得CuCl2和AgCl;Fe位于H前,与稀盐酸反应生成物是FeCl2而不是FeCl3;Al与稀盐酸反应能直接生成AlCl3。
15.下列有关金属的说法正确的是( ) A.铁钉与稀硫酸充分反应后得到黄色溶液 B.铝与稀硫酸反应的化学方程式为:Al+H2SO4===AlSO4+H2↑ C.镁条与稀盐酸混合后,产生大量气泡,放热 D.可用铁、镁代替锌用于实验室制取氢气
【点拨】铁与稀硫酸反应得到的溶液呈浅绿色,不是黄色,A错误;铝与稀硫酸反应的化学方程式为2Al+3H2SO4===Al2(SO4)3+3H2↑;镁与酸反应时,反应速率快,且放出大量热,C正确;镁与酸反应速率过快,铁与酸反应的速率较慢,都不宜用于实验室制取氢气。
16.黄铜(锌和铜的合金)、生铁是两种常见的合金。(1)将黄铜放入足量的稀盐酸中,现象是________________________________,发生反应的化学方程式是____________________________,最后残留的固体是________。
黄铜表面产生大量无色气泡
Zn+2HCl===ZnCl2+H2↑
(2)将生铁放入足量的稀硫酸中,反应的化学方程式是________________________,所属基本反应类型是____________,最后残留的固体主要是________。
17.下列金属各2 g,分别与足量的稀盐酸反应,产生氢气最多的是( ) A.铝 B.锌 C.镁 D.铁
18.(2019·眉山)将质量相等的镁粉和铁粉分别投入等质量等浓度的稀硫酸中,所得H2质量与稀硫酸质量关系曲线正确的是( )
【点拨】反应的稀硫酸质量相等时,生成氢气质量也相等,最终镁和稀硫酸反应生成的氢气多,B项对应关系正确。
19.(2020•滨州)现有质量相等的甲、乙、丙三种金属,分别放入三份浓度相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是( ) A.完全反应所需时间:丙>甲>乙 B.生成氢气的质量:甲>乙>丙 C.相对原子质量:乙>丙>甲 D.消耗硫酸的质量:甲>乙>丙
初中化学人教版九年级下册第十一单元 盐 化肥实验活动8 粗盐中难溶性杂质的去除备课ppt课件: 这是一份初中化学人教版九年级下册第十一单元 盐 化肥实验活动8 粗盐中难溶性杂质的去除备课ppt课件,共28页。PPT课件主要包含了答案呈现,见习题,纯金属,金属钨的熔点高,铁的硬度比铝大,金属材料,密度小,铜制的,不可以等内容,欢迎下载使用。
2020-2021学年课题 2 金属的化学性质习题ppt课件: 这是一份2020-2021学年课题 2 金属的化学性质习题ppt课件,共39页。PPT课件主要包含了答案呈现,碳或C,铜或Cu,置换反应等内容,欢迎下载使用。
初中化学人教版九年级下册实验活动8 粗盐中难溶性杂质的去除课文内容ppt课件: 这是一份初中化学人教版九年级下册实验活动8 粗盐中难溶性杂质的去除课文内容ppt课件,共30页。PPT课件主要包含了答案呈现,见习题,1物理2a,非金属,混合物,抗腐蚀性,答案C,组成它的纯金属,含碳量,答案B等内容,欢迎下载使用。













