





初中化学到实验室去:粗盐中难溶性杂质的去除集体备课ppt课件
展开1.【中考•海南】在“粗盐中难溶性杂质的去除”实验中,不需要进行的操作是( )A.溶解 B.过滤 C.蒸发 D.蒸馏
【点拨】粗盐的主要成分是氯化钠,粗盐提纯是通过溶解、过滤、蒸发得到精盐的过程,无需进行蒸馏。
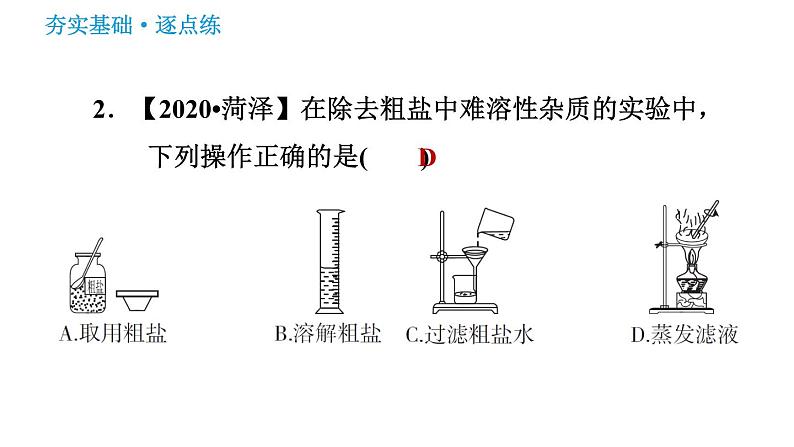
2.【2020•菏泽】在除去粗盐中难溶性杂质的实验中,下列操作正确的是( )
【点拨】量筒只能用来量取液体体积,不能用来溶解固体;称量药品应“左物右码”。
3.【中考•滨州】欲将粗盐提纯并用所得精盐配制一定溶质质量分数的氯化钠溶液,下列说法正确的是( )A.过滤时,用玻璃棒搅拌,加快过滤速度B.蒸发时,待蒸发皿中晶体全部析出后停止加热C.配制溶液时必须使用的仪器有托盘天平、酒精灯、量筒、烧杯、玻璃棒等D.配制溶液需要经过计算、称量、溶解、装瓶存放等步骤
【点拨】过滤时,不能用玻璃棒搅拌,以防捅破滤纸,A错误;蒸发时,待蒸发皿中出现较多量的固体时,停止加热,利用余热将剩余液体蒸干,B错误;配制一定溶质质量分数的氯化钠溶液,无需使用酒精灯,C错误;D正确。
4.【中考•淄博】海水“晒盐”得到的是粗盐,粗盐提纯的步骤可简单概括为溶解、过滤、蒸发,下列说法错误的是( )A.实验前需要查阅资料,了解食盐在室温时的溶解度B.粗盐若未能充分溶解,则实验结果中食盐的含量将偏低C.过滤后得到的滤渣是粗盐中的难溶性杂质D.蒸发时需将滤液全部蒸干再停止加热
5.【中考•丹东】用下列实验操作可分别完成“粗盐中难溶性杂质的去除”和“一定溶质质量分数的氯化钠溶液的配制”两个实验。(1)操作E中得到的滤液仍浑浊,其原因可能是____________________________________________________________________________________ (答出一点即可)。
滤纸破损(或漏斗内液面高于滤纸边缘或承接滤液的烧杯不洁净)
(2)若图B所用的烧杯内壁沾有水,导致配制溶液中溶质的质量分数会________(填“偏大”“偏小”或“不变”)。
(3)图D中玻璃棒的作用是____________________________________________。(4)图C中有一处明显的错误,请你改正:____________________________________________。
搅拌,防止局部温度过高,造成液滴飞溅
视线应与凹液面最低处保持水平
6.【中考•河南】为除去氯化钠中的泥沙和CaCl2、MgCl2、Na2SO4杂质,某化学兴趣小组的同学先将粗盐样品溶解、过滤,除去泥沙后,取粗盐水按以下流程进行实验探究。
(1)溶解、过滤、蒸发操作中都要用到的一种玻璃仪器是________。(2)写出一个加入Na2CO3溶液时所发生反应的化学方程式__________________________________________________________________________________。
Na2CO3+CaCl2===CaCO3↓+2NaCl(或BaCl2+Na2CO3===BaCO3↓+2NaCl)
(3)上述流程中,若将过滤和加盐酸的操作顺序颠倒,所得精盐产品中含哪些杂质?(BaSO4不溶于水,也不溶于酸)__________________________。
氯化钙、氯化镁、氯化钡
【点拨】(1)溶解、过滤、蒸发操作中都要用到的一种玻璃仪器是玻璃棒。(2)加入Na2CO3溶液时,碳酸钠和氯化钙反应生成白色沉淀碳酸钙和氯化钠,碳酸钠和氯化钡反应生成白色沉淀碳酸钡和氯化钠,发生反应的化学方程式为Na2CO3+CaCl2===CaCO3↓+2NaCl,BaCl2+Na2CO3===BaCO3↓+2NaCl。
(3)上述流程中,若将过滤和加盐酸的操作顺序颠倒,盐酸和碳酸钙反应生成氯化钙、水和二氧化碳,和氢氧化镁反应生成氯化镁和水,和碳酸钡反应生成氯化钡、水和二氧化碳,所得精盐产品中的杂质有氯化钙、氯化镁、氯化钡。
7.在“粗盐提纯”实验中,将提纯后的氯化钠与粗盐作比较,以计算精盐的产率。下列可能引起产率偏高的原因是( )A.粗盐未完全溶解B.溶解粗盐的烧杯壁上还沾有水C.过滤时液面高于滤纸边缘D.蒸发时有液滴飞溅出去
【点拨】过滤时液面高于滤纸边缘,会使部分待过滤液通过滤纸与漏斗之间的缝隙进入烧杯中,使精盐中含有难溶的杂质,造成产率偏高。
8.【中考•巴中】某化学兴趣小组的同学做粗盐提纯实验,如图是同学们做粗盐提纯实验的示意图,请回答下列问题:(1)操作③中玻璃棒搅拌的作用是____________________。
(2)操作⑥中的错误是___________________________。(3)粗盐提纯实验的操作顺序为_____________________ (填操作序号),以及称量精盐并计算产率。(4)操作④中,当观察到蒸发皿内__________________时,停止加热,利用余热蒸干。
【点拨】(1)操作③是溶解操作,玻璃棒搅拌的作用是加快粗盐的溶解速率。(2)操作⑥是过滤操作,图中缺少玻璃棒引流。(3)粗盐的主要成分是氯化钠,粗盐提纯的步骤为溶解、过滤(把不溶物除去)、蒸发、称量精盐、计算产率,操作步骤的先后顺序是①⑤②③⑥④。(4)蒸发时,待蒸发皿中出现较多量的固体时,即停止加热,利用余热将剩余液体蒸干。
9.【中考•菏泽】粗盐中含有难溶性杂质(泥沙等)和多种可溶性杂质(氯化镁、氯化钙等)。某班同学在粗盐提纯实验中,为把少量可溶性杂质CaCl2、MgCl2一并除去,将教材中实验方案修改设计如下,请据此回答问题:
(1)实验操作A的名称是________,该操作的目的是__________________________________________。
(2)写出步骤③中发生反应的主要化学方程式______________________________________;步骤⑥的作用是__________________________。
MgCl2+2NaOH===Mg(OH)2↓+2NaCl
除去过量的NaOH和Na2CO3
小刚同学认为该方案实际得到的氯化钠可能比粗盐中含有的氯化钠要多,请你为他找出理由:____________________________________________。
在实验过程中有NaCl生成
10.【中考•怀化】某学习小组对粗盐中杂质(难溶性和可溶性)的去除展开相关探究。(1)粗盐中难溶性杂质去除的实验步骤为①溶解,②过滤,③________(写操作名称),④计算产率。(2)步骤②中需要用到的玻璃仪器有玻璃棒、烧杯、______(写仪器名称),其中玻璃棒的作用是________。
(3)【提出猜想】甲同学:该粗盐中除含有难溶性杂质外,是否还含有可溶性杂质?(4)【查阅资料】①粗盐中可能含有镁盐(Mg2+)和硫酸盐(SO2-4)等可溶性杂质;②一些物质的溶解性表如下:
③Mg(OH)2为白色物质,不溶于氢氧化钠溶液;BaSO4为白色物质,不溶于盐酸;MgCO3、BaCO3为白色物质,都能溶于盐酸。(5)【实验设计】①取少量除去难溶性杂质后的盐,溶于水配成溶液;
②取少量所配溶液于试管中,滴加氢氧化钠溶液,产生白色沉淀,继续滴加氢氧化钠溶液,沉淀不溶解,说明该盐中含有可溶性的________盐;③另取少量所配溶液于试管中,滴加氯化钡溶液,产生白色沉淀,再加稀盐酸,沉淀不溶解,说明该盐中含有可溶性的________盐。
(6)【实验结论】该盐含有可溶性杂质____________。(7)【实验拓展】以下为乙同学设计的去除粗盐中可溶性杂质的实验流程:
①该实验过程中,除杂试剂都要过量,原因是_____________________________________________;②过量Na2CO3溶液用来除__________(填离子符号)。
初中化学人教版九年级下册实验活动8 粗盐中难溶性杂质的去除课文内容ppt课件: 这是一份初中化学人教版九年级下册实验活动8 粗盐中难溶性杂质的去除课文内容ppt课件,共30页。PPT课件主要包含了答案呈现,见习题,1物理2a,非金属,混合物,抗腐蚀性,答案C,组成它的纯金属,含碳量,答案B等内容,欢迎下载使用。
化学九年级下册第八单元 海水中的化学综合与测试图片ppt课件: 这是一份化学九年级下册第八单元 海水中的化学综合与测试图片ppt课件,共49页。PPT课件主要包含了答案呈现,甲乙丙,降温结晶,加入溶质或升温,∶19,溶解度相等,①③④⑤⑥,不饱和等内容,欢迎下载使用。
化学九年级下册第八单元 海水中的化学第二节 海水“晒盐“图文ppt课件: 这是一份化学九年级下册第八单元 海水中的化学第二节 海水“晒盐“图文ppt课件,共45页。PPT课件主要包含了答案呈现,乙>甲=丙,丙>甲=乙,KNO3,不饱和,加溶质,氢氧化钙,蒸发结晶,NaCl,CaOH2等内容,欢迎下载使用。













