



专题07 金属的化学性质-2021年中考化学二轮专题课件(人教版)
展开反应的剧烈程度或反应先后顺序
考点1:金属的化学性质
许多金属都能与氧气反应,但是反应的难易和剧烈程度不同。
金属镁在空气中表面逐渐变暗
金属铝在空气中表面逐渐变暗
2Mg+O2═2MgO
4Al+3O2═2Al2O3
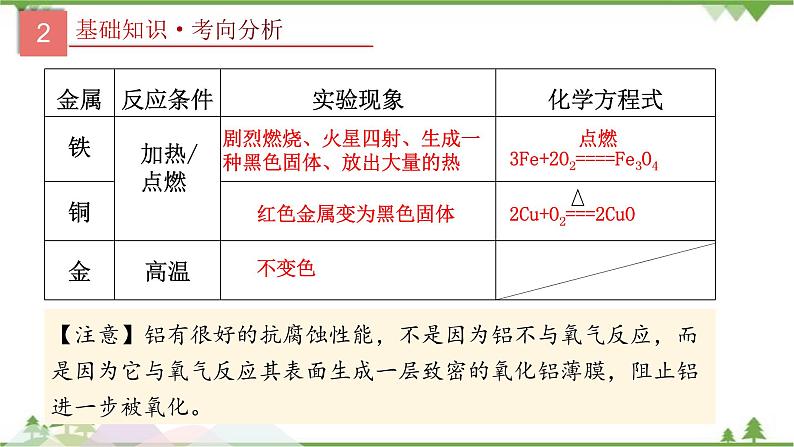
剧烈燃烧、火星四射、生成一种黑色固体、放出大量的热
3Fe+2O2====Fe3O4
2Cu+O2===2CuO
【注意】铝有很好的抗腐蚀性能,不是因为铝不与氧气反应,而是因为它与氧气反应其表面生成一层致密的氧化铝薄膜,阻止铝进一步被氧化。
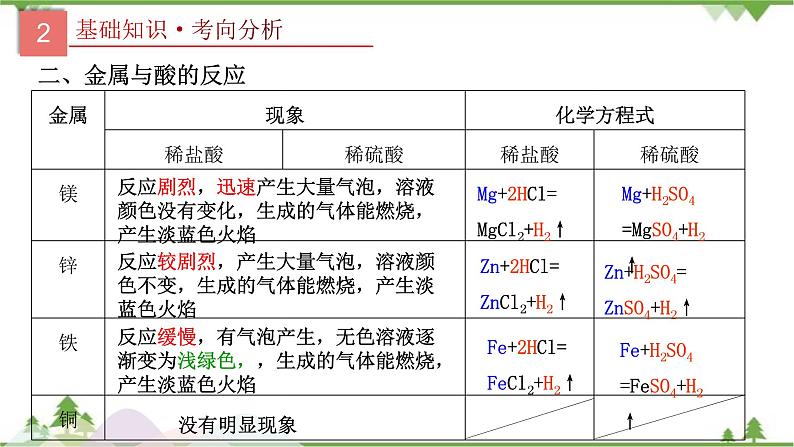
反应较剧烈,产生大量气泡,溶液颜色不变,生成的气体能燃烧,产生淡蓝色火焰
反应缓慢,有气泡产生,无色溶液逐渐变为浅绿色,,生成的气体能燃烧,产生淡蓝色火焰
Zn+2HCl=ZnCl2+H2↑
Fe+2HCl=FeCl2+H2↑
Mg+2HCl=MgCl2+H2↑
Mg+H2SO4=MgSO4+H2↑
Fe+H2SO4=FeSO4+H2↑
Zn+H2SO4=ZnSO4+H2↑
反应剧烈,迅速产生大量气泡,溶液颜色没有变化,生成的气体能燃烧,产生淡蓝色火焰
【注意】1.不是所有的酸都能与金属发生置换反应放出氢气,这里的酸指的是稀盐酸和稀硫酸,浓硫酸和硝酸等具有强烈的氧化性,与金属反应不会放出氢气。 2.在金属活动性顺序里,位于____前面的金属能置换出盐酸、稀硫酸中的_____,且金属活动性越强,反应速率越快;位于氢后面的金属不能与盐酸、稀硫酸反应。
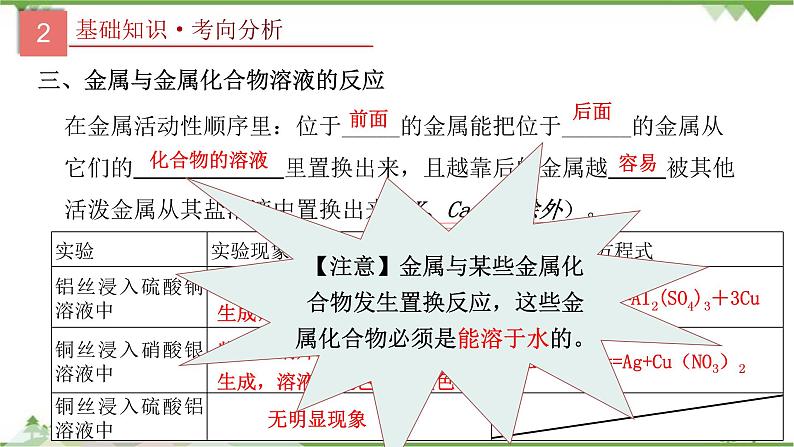
三、金属与金属化合物溶液的反应
在金属活动性顺序里:位于_____的金属能把位于______的金属从它们的 里置换出来,且越靠后的金属越 被其他活泼金属从其盐溶液中置换出来(K、Ca、Na除外)。
银白色铝片表面有紫红色物质生成,溶液由蓝色变为无色
2Al+3CuSO4==Al2(SO4)3+3Cu
紫红色铜片表面有银白色物质生成,溶液由无色变为蓝色
Cu+AgNO3===Ag+Cu(NO3)2
【注意】金属与某些金属化合物发生置换反应,这些金属化合物必须是能溶于水的。
A类型:金属与氧气的反应
【例1】中考组合题下列说法正确的是( ) A.“金入于猛火,色不夺精光”﹣﹣金在加热的条件下能与氧气反应(2020•烟台) B.通常情况下铝制品耐腐蚀,原因是铝不易发生化学反应(2019•泰州) C.“真金不怕火炼”说明黄金的化学性质非常稳定(2020•泰安) D.铁丝在空气中剧烈燃烧,火星四射,放出大量的热,生成黑色固体(2019•鸡西改编)
B类型:金属与酸的反应
【例2】(2020•淄博)手机的某些部件里含有Mg、Al、Cu、Ag等金属,将废旧手机的部件粉碎并浸入足量稀硫酸中充分反应后,所得溶液中含有的金属离子是( )A.Mg2+、Al3+B.Cu2+、Ag+C.Al3+、Cu2+D.Mg2+、Ag+
【变式训练】(2020•甘孜州)如图是包含物质a、b、c、d和盐酸卡片的“化学拼图”,相邻两张卡片所标的物质(或其溶液)间能发生化学反应。单质a不可能是( )
A.Mg B.FeC.Ag D.Zn
C类型:金属与金属化合物的反应
【例3】(2020•无锡)将一根洁净的铜丝放入AgNO3溶液中,一段时间后,溶液从无色变为蓝色,铜丝表面生长出如图所示的白色“树枝”,下列叙述错误的是( )
A.白色“树枝”的成分是银B.溶液变为蓝色,表明Cu转变为Cu2+C.所得溶液中肯定不含有Ag+D.铜的金属活动性比银的强
考点2:金属活动性顺序
金属活动性由强逐渐减弱
1.常见金属的活动性顺序
2.金属活动性顺序的应用:
(1)比较不同金属的活动性强弱:在金属活动性顺序里:金属的位置越_____,它的活动性就越强。
(2)判断某金属是否能与酸反应以及反应快慢。在金属活动性顺序里:位于氢前面的金属能置换出盐酸、稀硫酸中的氢,且金属活动性越强,反应速率越快。
(3)用于判断金属与混合盐溶液的反应先后顺序。
在金属活动性顺序里:位于_____的金属能把位于______的金属从它们的化合物的溶液里置换出来,且越靠后的金属越容易被其他活泼金属从其盐溶液中置换出来(K、Ca、Na除外!)。
【注意】金属与某些金属化合物发生置换反应,这些金属化合物必须能溶于水。如Fe不能与AgCl(难溶)反应。
3.设计实验验证金属活动性顺序
(1)两种金属的活动性强弱比较(以Fe、Cu为例)
设计依据: ①加稀盐酸或稀硫酸:反应越剧烈金属活动性越强; ②一种金属+另一种金属的化合物溶液。
将Fe、Cu分别放入稀硫酸中
将Fe放入CuSO4溶液中
将Cu放入FeSO4溶液中
【注意】当两种金属均为氢后金属时,只能选用方法②鉴别。
(2)三种金属的活动性强弱比较[以Al(打磨后)、Fe、Cu为例]
设计依据:较活泼的金属能把不活泼的金属从它的盐溶液中置换出来。
将铝片、铜片分别放入等量的FeSO4溶液中
将铁片分别放入Al2(SO4)3和CuSO4溶液中
将铝片、铁片、铜片分别放入等量的稀硫酸中
(3)多种金属的活动性强弱比较 ①先将金属同时放入稀盐酸或稀硫酸中,根据能否与酸发生置换反应将金属分为两组:氢前金属和氢后金属。 ②氢前金属可根据其与酸反应速率的快慢,判断活动性强弱; ③氢后金属用比较两种或三种金属活动性强弱的方案判断活动性强弱。
考察金属活动性顺序及应用
【例4】(2020•上海)下列物质中,金属活动性最强的是( )A.铝B.铁C.铜D.银
A类型:比较金属活动性顺序
【变式训练】(2020•百色)探究铁、铜、镁的金属活动性时,下列现象、分析或结论正确的是( )
A.铜片表面有气泡产生B.有镁片的试管外壁发烫C.铁片与盐酸反应速率最快D.它们的活动性:Cu>Fe>Mg
B类型:判断金属是否与酸反应及反应快慢
【例5】(2020•济宁)在两只烧杯中分别放入相同质量的镁、锌两种金属,然后向两只烧杯中分别倒入相同质量、相同质量分数的稀硫酸,反应产生氢气的质量与消耗硫酸的质量关系见图。综合以上信息得到以下结论,合理的是( )
A.从图象可以看出,金属镁比金属锌的活动性强B.若两种金属都有剩余,二者得到的氢气质量相同C.若硫酸有剩余,二者得到氢气的质量相同D.若两种金属完全溶解,二者消耗硫酸的质量相同
C类型:判断金属是否与金属化合物溶液反应及先后顺序
【变式训练】(2020•黑龙江)将一定量的Zn粉和Cu粉投入到硝酸银溶液中,充分反应后过滤,得到滤渣和蓝色滤液,则滤渣中可能含有 ,滤液中一定含有的溶质是 ,请用化学方程式解释溶液变蓝的原因 。
【例6】(2020•巴中)将一定质量的铁粉和铜粉加入到Zn(NO3)2和AgNO3的混合溶液中,一定会发生的化学反应方程式为 。充分反应后过滤,向滤渣中滴加稀盐酸,有无色气体产生,则滤渣中一定含有 (填化学式),滤液中的溶质一定含有 (填化学式)。
Fe+2AgNO3═Fe(NO3)2+2Ag
Zn(NO3)2、Fe(NO3)2
Cu+2AgNO3═Cu(NO3)2+2Ag
D类型:设计实验验证金属活动性顺序
【例7】(2020•金昌)某同学为验证铁、铜、银三种金属的活动性顺序,他设计了以下四种实验方案,其中能达到目的的是( )A.将Fe丝、Cu丝分别放入AgNO3溶液中B.将Fe丝、Ag丝分别放入CuSO4溶液中C.将Fe丝、Cu丝、Ag丝分别放入稀盐酸中D.将Fe丝分别放入CuSO4溶液、AgNO3溶液中
【变式训练】(2020•恩施州)现有Al、Cu、Ag三种金属,限用一种试剂一次性就可以验证它们的金属活动性强弱,则该试剂是( )A.CuSO4溶液B.稀H2SO4C.AgNO3溶液D.AlCl3溶液
(1)概念:由一种 与一种 反应,生成另一种 和另一种 的反应,叫做置换反应。
(3)通式:A+BC→B+AC
(2)特点:“单换单”。
(4)判断置换反应能否发生要依据金属活动性顺序。
【变式训练】(2020•江北区校级模拟)已知金属锰在金属活动性顺序中位于铝和锌之间。下列化学反应不能发生的是( )A.Mg+MnCl2═MgCl2+MnB.Fe+MnCl2═MgCl2+MnC.Mn+CuCl2═MnCl2+CuD.Mn+H2SO4═MnSO4+H2↑
【例8】(2020•朝阳)下列化学反应属于置换反应的是( )A.H2O+CaO═Ca(OH)2B.Na2SO4+BaCl2═2NaCl+BaSO4↓C.H2+CuO Cu+H2O D.3CO+Fe2O3 2Fe+3CO2
高频一:金属活动性顺序的应用
【例9】(2020•泰安)向AgNO3、Cu(NO3)2、Mg(NO3)2的混合溶液中加入一些锌粉,完全反应后过滤。不可能存在的情况是( )A.滤纸上有Ag,滤液中有Ag+、Cu2+、Zn2+、Mg2+B.滤纸上有Ag、Cu,滤液中有Zn2+、Mg2+C.滤纸上有 Ag、Cu、Zn、Mg,滤液中有Zn2+D.滤纸上有Ag、Cu、Zn,滤液中有Zn2+、Mg2+
高频二:利用金属的化学性质解决除杂问题
【例10】(中考组合题)除去下列物质中的少量杂质(括号内为杂质),所选试剂及操作方法均正确的是( )
A.Cu(NO3)2溶液(FeCl2)--加足量的铜粉、过滤(2020•百色)B.铁粉(木炭粉)--加入适量的稀硫酸、过滤(2020•鞍山)C.FeCl2溶液(CuCl2)--加足量的铁粉、搅拌、过滤(2020•鄂州)D.银粉(锌粉)--加入足量稀盐酸溶解、过滤、洗涤、干燥(2020•荆门)
高频三:有关金属与酸反应的图像问题
【例11】(2020•襄阳)向质量均为m的锌粉和铁粉中分别滴加100g相同质量分数的稀硫酸,反应过程中产生气体的质量与所加稀硫酸的质量关系如图所示,下列叙述正确的是( )
A.反应后均得到无色溶液B.反应结束后两种金属均有剩余C.折线b表示的是铁和稀硫酸反应的情况D.反应结束后所得溶液的质量相等
【例12】(2020•滨州)现有质量相等的甲、乙、丙三种金属,分别放入三份溶质质量分数相同的足量稀硫酸中,生成氢气的质量与反应时间的关系如图所示(已知甲、乙、丙在生成物中均显+2价)。则下列说法错误的是( )
A.完全反应所需时间:丙>甲>乙B.生成氢气的质量:甲>乙>丙C.相对原子质量:乙>丙>甲D.消耗硫酸的质量:甲>乙>丙
高频四:有关金属与酸反应的计算问题
【例13】(2020•巴中)向5.6g含两种杂质的铁粉样品中加入足量的稀盐酸,充分反应后共产生0.2g氢气,则该样品中所含杂质可能是( )A.锌和铜B.锌和镁C.铝和镁D.碳和铜
【例14】(2020•贵港)现有一包由2.4g镁、6.5g锌、1.6g碳混合而成的粉末,把它加入到一定量的硝酸银溶液中,反应结束后,经过滤、洗涤、干燥,测得滤渣含有三种物质。则滤渣的质量可能是( )A.10.5gB.35.6gC.44.8gD.45.8g
【例15】(2019•攀枝花)为了从含有FeSO4、CuSO4的工业废水中回收Cu和硫酸亚铁晶体,某学习小组设计并完成了以下实验。
下列说法正确的是( )A.固体X中只含有Cu B.试剂B是稀硫酸C.溶液Z中的溶质为FeSO4和CuSO4D.操作Ⅰ用到的玻璃仪器只有烧杯和玻璃棒
高频五:化学工艺与流程分析
【例16】(2019•大庆)某化学兴趣小组的同学想从含有Al2(SO4)3、CuSO4的废液中回收金属铜,设计流程如图:
(1)过滤操作中用到的所有玻璃仪器为 。(2)Ⅰ中有关反应的化学方程式 。(3)溶液B中所含的溶质是 ;固体A的成分是 。(均填化学式)(4)Ⅱ中加入过量的稀硫酸的目的是 。
Fe+CuSO4═FeSO4+Cu
Al2(SO4)3、FeSO4
题型1 金属的化学性质
1.(2020•昆明)北宋沈括《梦溪笔谈》中记载:“信州铅山有苦泉,流以为涧。挹其水熬之则成胆矾,烹胆矾则成铜。熬胆矾铁釜,久之亦化为铜”。下列有关叙述错误的是( )A.“烹胆矾则成铜”是物理变化B.胆矾可用于配制波尔多液C.“熬之则成胆矾”是蒸发结晶过程D.“熬胆矾铁釜,久之亦化为铜“发生反应Fe+CuSO4═Cu+FeSO4
2.(2020•金华)取一定质量的锌粒和铜片于同一敞口容器中,再逐渐加入稀硫酸。加入稀硫酸的质量与有关量的变化关系图正确的是( )
3.(2020•十堰)某学习小组同学做完铁与稀硫酸反应实验后,将反应后的混合物M全部倒入盛有一小块铜锌合金的烧杯中,发现有大量气泡产生。待充分反应后过滤,得到滤液和滤渣。他们得出的现象或结论如下:①M中一定不含铁单质;②烧杯中溶液由浅绿色变成蓝色;③滤液中一定含有ZnSO4;④滤渣中可能含有三种金属单质;⑤滤液中可能含有两种金属离子。其中正确的个数有( )A.4个B.3个C.2个D.1个
4.(2020•永州)将用砂纸打磨后的铁丝插入CuSO4溶液中,一段时间后,下列叙述正确的是( )A.溶液的质量增加 B.溶液由蓝色变成无色C.溶液中产生大量气泡 D.溶液中铁丝表面有红色物质生成
5.(2019•济南)现有ZnSO4和CuSO4的混合溶液100g,加入5g铁粉,充分反应后过滤,得到一定温度下的不饱和溶液和滤渣,下列有关说法中,不合理的是( )A.滤渣的质量一定大于5gB.整个过程中ZnSO4的质量不变C.滤渣中一定含有单质Fe和单质CuD.所得溶液中一定含有Zn2+和Fe2+
6.(2019•兴安盟)下列金属不能和FeSO4溶液反应的是( )A.ZnB.MgC.CuD.Al
7.(2020•黑龙江)某兴趣小组在研究Zn﹣Cu合金、Zn﹣Fe合金、Fe﹣Al合金、Fe﹣Cu合金时,发现其中一种合金6.5g与足量稀盐酸充分反应产生了0.5g气体,该合金可能是( )A.Zn﹣Cu合金B.Zn﹣Fe 合金C.Fe﹣Al合金D.Fe﹣Cu合金
8.(2019•常德)印刷电路板常用氯化铁溶液作为“腐蚀液”,发生的反应为2FeCl3+Cu═2FeCl2+CuCl2,向盛有氯化铁溶液的烧杯中同时加入铁粉和铜粉,反应结束后,剩余固体的成分不可能是( )A.有铁无铜B.有铜无铁C.铁、铜都有D.铁、铜都无
9.(2018•郴州)“药金”是锌和铜的合金,因外形似黄金而得名。下列厨房用品可用来鉴别“药金”为假黄金的是( )A.食盐水B.白醋C.料酒D.酱油
10.(2020•湘西州)下列化学反应中不属于置换反应的是( )A.Fe+H2SO4═FeSO4+H2↑ B.CO+CuO Cu+CO2C.Cl2+2NaI═2NaCl+I2D.Fe+CuSO4═FeSO4+Cu
题型2 金属活动性顺序
11.(2020•常德)向盛有AgNO3和Cu(NO3)2混合溶液的试管中加入一定量的铁粉,充分反应后过滤,滤液呈蓝色。下列判断正确的是( )A.滤渣可能含有铜B.滤液的质量可能比原溶液的质量大C.滤液中可能含有Fe(NO3)3和Cu(NO3)2D.向滤渣中加入稀盐酸,可能有气泡产生
12.(2019•西藏)下列可用于验证Fe、Cu、Ag三种金属的活动性顺序的一组药品是( )A.Fe、Cu、H2SO4溶液B.Cu、Ag、FeSO4溶液C.Fe、Ag、CuSO4溶液D.Ag、FeSO4溶液、CuSO4溶液
13.(2018•陕西)将等质量且形状大小相同的甲、乙两种金属分别加入到等质量且溶质质量分数相同的稀盐酸中,产生氢气的质量随反应时间的变化关系如图所示。下列说法不正确的是( )
A.甲的金属活动性比乙强B.甲可能是镁,乙可能是铝C.反应结束时,甲一定无剩余,乙可能有剩余D.甲的相对原子质量一定小于乙
14.(2020•日照)有甲、乙、丙、丁四种金属,只有丙在自然界能以单质形态存在。含甲化合物的水溶液不能用乙制的容器盛放。将甲和丁分别放入硝酸铜溶液中,在甲表面有铜析出,而丁没有变化。这四种金属活动性顺序由弱到强的是( )A.丙<丁<甲<乙B.乙<甲<丁<丙C.丁<甲<乙<丙D.丙<乙<甲<丁
15.(2020•昆明)为验证Mg、Cu、Sn的金属活动性顺序,不可选用的一组物质是( )A.MgCl2溶液、Cu、SnB.Mg、Cu、SnCl2溶液C.Mg、Sn、Cu、盐酸D.MgCl2溶液、Sn、CuCl2溶液
16.(2020•黄冈)已知金属R和Fe、H活动性强弱关系为:Fe>R>H,下列说法正确的是( )A.金属R放入Zn(NO3)2溶液中,有锌析出B.金属R放入CuSO4溶液中,金属表面有红色固体析出C.金属铁(足量)放入R(NO3)2溶液中,溶液变黄色D.金属铁放入AgNO3溶液中,一段时间后溶液质量变大
17.(2019•宁夏)金属钛被誉为21世纪的“明星”金属,具有很多优良性能,被广泛应用于各行各业。为探究钛与镁、铜金属活动性的强弱,选取的下列各组试剂中正确的是(提示:钛的活动性在镁和氢之间)( )①钛 镁 铜 稀盐酸②镁 钛 硫酸铜溶液③镁 铜 氯化钛溶液④钛 铜 硫酸镁溶液 ⑤钛 硫酸镁溶液 硫酸铜溶液⑥铜 硫酸镁溶液 氯化钛溶液A.①②③⑤B.②③④⑥C.①②⑤⑥D.①③④⑤
18.(2019•十堰)为探究金属活动性顺序,学习小组设计并进行实验I和Ⅱ.实验结束,将两实验的废液全部倒入一洁净烧杯中,反应后得到溶液A和固体B.实验过程及现象如图所示:
据此得出以下结论:①通过实验I和Ⅱ能验证Al、Ag、Cu的金属活动性顺序;②实验反应后固体中一定含有Cu; ③若A是无色溶液,A中可能含有AgNO3;④若A呈蓝色,溶液A中至少有两种溶质⑤若A呈蓝色,固体B中一定不含Cu;其中正确结论的个数有( )A.1个B.2个C.3个D.4个
19.(2019•临沂)某同学为了探究相关金属的化学性质,做了下列实验:
(1)A试管中实验现象是 。(2)只通过A和B实验尚不能证明铜、银两种金属的活动性强弱,需补充一个实验来证明,补充实验所用试剂合理的是 。A.Cu、Ag、稀盐酸 B.Cu、AgNO3溶液(3)实验C中物质充分反应后,某同学对试管中固体的成分提出以下四种猜想:A.Zn、Cu、Ag B.Zn、Cu C.Cu、Ag D.Ag这四种猜想中明显不合理的是 (填编号)。
锌片的表面有红色物质生成,溶液由蓝色逐渐变为无色
1.(2020•固始县一模)将等质量镁、铝、锌、铁的单质分别投入质量相等且足量的稀硫酸中,反应结束后,所得溶液的质量由大到小的顺序是( )A.Al>Mg>Fe>ZnB.Al=Mg=Fe=ZnC.Zn>Fe>Mg>AlD.Mg>AI>Zn>Fe
2.(2020•包头模拟)天平两边各放质量相等的烧杯,分别盛有等质量等质量分数的稀硫酸(左)和稀盐酸(右),此时天平平衡。现将相同质量的金属锌分别加入到两个烧杯里,充分反应后。下列说法正确的是( )A.若天平平衡,两烧杯中的酸一定都反应完了B.若天平不平衡,左边的锌一定有剩余C.若天平不平衡,指针一定偏向稀盐酸的一边D.若天平平衡,两烧杯中的酸一定都有剩余
3.(2020•镇平县模拟)将一定质量的铁粉加入到含有Cu(NO3)2和AgNO3的混合溶液中,充分反应后过滤,再向滤渣中加入稀盐酸,无气泡产生。下列判断正确的是( )A.滤渣中一定含有Ag和Cu,滤液中一定含有Fe(NO3)2B.滤渣中一定含有Ag,滤液中可能含有Cu(NO3)2和AgNO3C.滤渣中一定不含Fe,滤液中一定含有Fe(NO3)2和Cu(NO3)2D.如滤液颜色为蓝色,则反应后溶液质量增加
4.(2020•盐池县一模)金属R与硫酸铜溶液反应的化学方程式是R+CuSO4═Cu+RSO4,从该化学方程式你能获得的正确信息是( )A.该金属可以是金属铝 B.金属R的活泼性比Cu要强C.该反应不是置换反应 D.该金属一定是锌
5.(2020•鱼台县模拟)质量相同质量分数相同的稀H2SO4与足量Mg、Al、Zn、Fe充分反应,生成氢气质量与金属质量的关系如图所示,分析图象信息,得出结论正确的是( )
A.四种金属都能与酸反应生成H2B.四种金属的活动性顺序:Al>Mg>Fe>ZnC.相同质量的四种金属与稀H2SO4反应,消耗酸的质量相等D.相同质量的四种金属与足量稀H2SO4反应氢气质量:Zn>Fe>Mg>Al
6.(2020•嘉鱼县二模)现有X、Y、Z三种金属,如果把X、Y金属分别放入稀硫酸中,X没有明显现象,Y表面有气泡产生,如果把X和Z分别放入硝酸银溶液中,过一会,在X表面有银析出,而Z没有变化。根据以上实验实验事实,判断X、Y和Z三种金属的活动性顺序为( )A.X>Y>ZB.Y>Z>X C.Z>Y>XD.Y>X>Z
7.(2020•安次区模拟)下列物质不能直接由金属和稀酸反应制取的是( )A.AlCl3B.ZnSO4C.FeCl3D.MgCl2
8.(2020•铁岭模拟)要证明Cu、Zn、Ag的金属活动性顺序,下列必须要做的实验是( )
A.①②③B.②③C.①③D.①②
9.(2020•永城市一模)在Cu(NO3)2、AgNO3、Zn(NO3)2的混合溶液中加入一定量的铁粉,充分反应后,可能有以下情况:若反应后溶液呈蓝色,则溶液中一定含有的阳离子是 ;若向反应后的滤渣中加入盐酸,有气泡放出,则反应后的滤液中一定含有的溶质是 。写出铁粉加入混合溶液中一定发生的一个反应的化学方程式: 。
锌离子、亚铁离子、铜离子
Fe+2AgNO3=Fe(NO3)2+2Ag
10.(2020•成武县校级模拟)向一定量的硝酸银、硝酸铝和硝酸铜的混合溶液中加入一定量的锌,溶液质量与加入锌的质量关系如图所示。(1)A点所发生反应的化学方程式为 。
(2)B点对应的溶液中含有的金属离子有 。(3)当加入锌的质量在m1~m2g时,溶液的质量增加的原因是 。
Zn+2AgNO3═Zn(NO3)2+2Ag
Al3+、Cu2+、Zn2+
每65份质量的锌能置换出64份质量的铜,反应后溶液质量增加
2024山东中考化学二轮专题复习 微专题 化学用语(课件): 这是一份2024山东中考化学二轮专题复习 微专题 化学用语(课件),共23页。PPT课件主要包含了Na+,Ca2+,Fe3+,Fe2+,Mg2+,Zn2+,Al3+,Cl-,OH-,H2O等内容,欢迎下载使用。
2024宁夏中考化学二轮重点专题突破 主题7 金属的化学性质(课件): 这是一份2024宁夏中考化学二轮重点专题突破 主题7 金属的化学性质(课件),共27页。PPT课件主要包含了宁夏近年真题及拓展,Cr2O3,Zn2+,硫酸反应的剧烈程度,硫酸锌或氯化锌,插入硫酸铜,Zn>Fe>Cu,Zn>Cu>Ag,与氧气反应,点燃或加热等内容,欢迎下载使用。
2024贵州中考化学二轮专题复习 主题6 金属的化学性质(课件): 这是一份2024贵州中考化学二轮专题复习 主题6 金属的化学性质(课件),共17页。PPT课件主要包含了金属的化学性质,与氧气反应,放出热量,加热铜,红色固体变黑,稀硫酸反应,化学方程式,有气泡产生,与某些盐溶液反应,铁与硫酸铜溶液等内容,欢迎下载使用。













