




2021年人教版九年级化学中考知识点专题复习:金属的化学性质 教学课件PPT
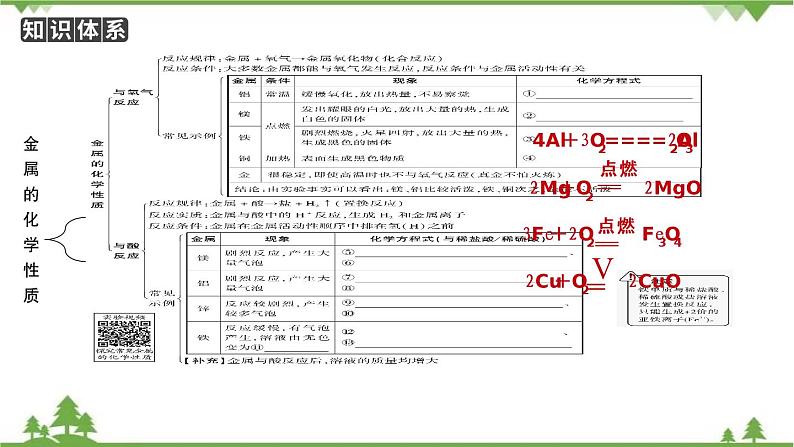
展开4Al+3O2====2Al2O3
2Mg+O2 2MgO
3Fe+2O2 Fe3O4
2Cu+O2 2CuO
2Al+3CuSO4====
Al2(SO4)3+3Cu
Cu+2AgNO3====
Cu(NO3)2+2Ag
Fe+CuSO4====
1.铝比铁活泼,所以通常情况下铁的抗腐蚀性能比铝强。( )2.金属与稀酸发生反应后,所得溶液的质量比反应前均增加。( )3.铝、锌、镁、铁四种金属与稀酸反应后,所得溶液均为无色。( )4.铁(Fe)与盐酸、稀硫酸或盐溶液发生置换反应时,生成+2价亚铁盐。( )
5.氧化铁(Fe2O3)与盐酸、稀硫酸发生复分解反应时,生成+3价铁盐。( )6.铁丝在氧气中燃烧时生成Fe2O3。( )7.位于氢前的金属能置换出盐溶液中的金属,位于氢后的金属则不能置换。( )
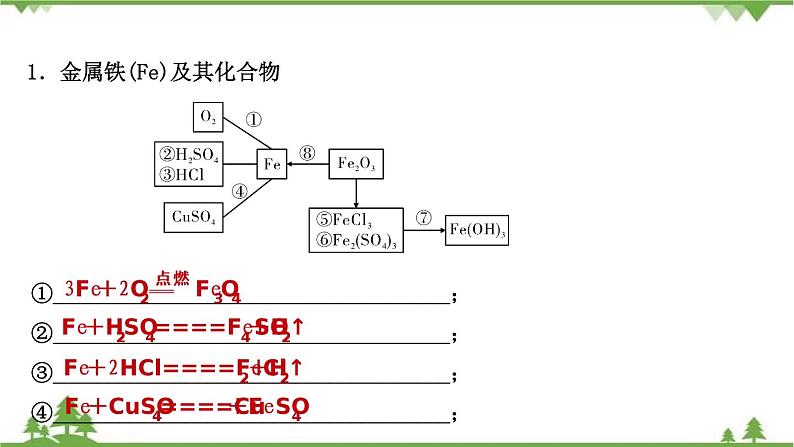
1.金属铁(Fe)及其化合物
①____________________________________;②____________________________________;③____________________________________;④____________________________________;
3Fe+2O2 Fe3O4
Fe+H2SO4====FeSO4+H2↑
Fe+2HCl====FeCl2+H2↑
Fe+CuSO4====Cu+FeSO4
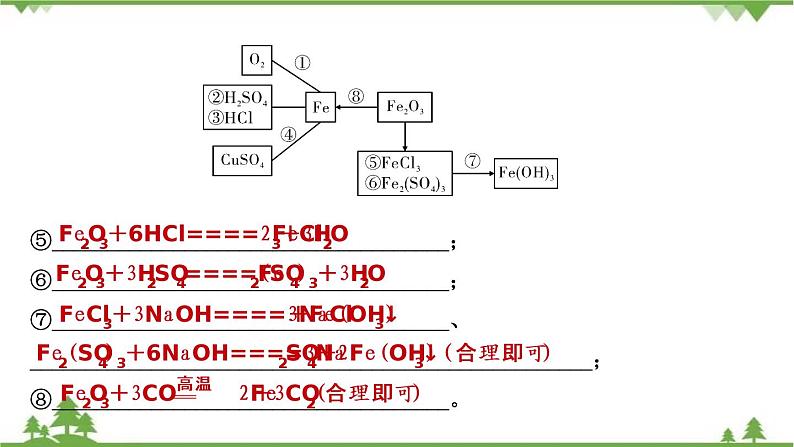
⑤____________________________________;⑥____________________________________;⑦____________________________________、___________________________________________________;⑧____________________________________。
Fe2O3+6HCl====2FeCl3+3H2O
Fe2O3+3H2SO4====Fe2(SO4)3+3H2O
FeCl3+3NaOH====3NaCl+Fe(OH)3↓
Fe2(SO4)3+6NaOH====3Na2SO4+2Fe(OH)3↓(合理即可)
Fe2O3+3CO 2Fe+3CO2(合理即可)
2.金属铜(Cu)及其化合物
2Cu+O2 2CuO
CuO+CO Cu+CO2(合理即可)
CuO+H2SO4====CuSO4+H2O
CuSO4+Fe====FeSO4+Cu(合理即可)
⑤_____________________________________;⑥___________________________________________;⑦____________________________;⑧____________________________;⑨_______________________________。
Cu+2AgNO3====Cu(NO3)2+2Ag(合理即可)
CuSO4+2NaOH====Cu(OH)2↓+Na2SO4(合理即可)
Cu(OH)2+H2SO4====CuSO4+2H2O
Cu(OH)2+2HCl====CuCl2+2H2O
Cu(OH)2+2HNO3====Cu(NO3)2+2H2O
金属与酸反应的图像分析
金属与酸反应,由化学方程式知,m(氢气)=m(金属)×
一、纵坐标为H2质量1.横坐标为反应时间分别向等质量的Mg、Al、Fe中逐滴滴入等体积、等浓度的稀盐酸。(1)反应速率:金属越活泼,产生氢气的速率越快,曲线越陡。
(2)产生氢气质量:①酸不足,产生氢气质量由酸的质量决定,最终生成的氢气的质量相等(如图1)。
②酸足量,产生氢气质量由金属质量决定,金属的相对原子质量越小(Al等效为+2价,相对原子质量等效成18),产生氢气的质量越大(如图2)。
2.横坐标为金属的质量分别向等质量的Mg、Al、Fe中逐滴滴入等质量、等浓度的稀盐酸(如图3)。金属足量,酸消耗完,最终生成氢气的质量由酸的质量决定。当m(金属)≤a时,生成氢气的质量由金属决定,金属的相对原子质量越小,生成氢气的质量越大。生成相同质量的氢气时,消耗金属的质量关系是Fe>Mg>Al。注:此曲线不能判断金属活动性强弱。
3.横坐标为酸的质量分别向等质量的Mg、Al、Fe中逐滴滴入等浓度的稀盐酸(如图4)。当稀盐酸质量≤a时,生成氢气的质量相等。随着稀盐酸的不断滴加,稀盐酸过量,金属的量不足,产生氢气的质量由金属的质量决定。金属的相对原子质量越小,生成的氢气越大(Al等效为+2价,相对原子质量等效为18)。注:此曲线不能判断金属活动性强弱。
二、其他图像1.纵坐标为反应物质量分别向等质量的Mg和Fe中逐滴滴入等质量、等浓度的稀盐酸。在金属足量,酸消耗完的情况下,剩余固体质量随反应时间的变化如图5,剩余酸的质量随反应时间的变化如图6。
2.纵坐标为溶液质量以Al与稀盐酸为例,两者发生如下反应:2Al+6HCl====2AlCl3+3H2↑,溶液中的溶质由HCl变为AlCl3,所以溶质质量逐渐增大,溶剂质量不变,所以溶液质量逐渐增大,至反应完全后保持不变(如图7)。
3.纵坐标为溶液温度金属与酸反应放热,溶液的温度逐渐升高,恰好完全反应时,温度最高,然后逐渐降低至室温状态,最后保持不变(如图8)。
(2021·原创题)下列图像与对应实验相符合的是( )
A.①分别向等质量Al和Cu中加入足量的、等浓度的稀硫酸B.②分别向等质量且足量的Zn中加入等质量、不同浓度的稀硫酸C.③分别向等质量的Mg和Fe中加入足量的、等浓度的稀盐酸D.④分别向等质量且足量的Mg和Zn中加入等质量、等浓度的稀硫酸
1.(2020·重庆北碚模拟)用相同质量的镁和铁分别与稀盐酸反应,横坐标表示加入盐酸的体积,则生成氢气的质量符合实际的是( )
2.(2018·重庆A)常温下向一定质量的稀盐酸中逐渐加入镁条,充分反应(忽略挥发)。下列图像正确的是( )
A.①② B.②③ C.①④ D.②④
人教版九年级下册课题 2 金属的化学性质复习ppt课件: 这是一份人教版九年级下册课题 2 金属的化学性质复习ppt课件,共5页。PPT课件主要包含了练一练等内容,欢迎下载使用。
中考化学一轮复习金属的化学性质课件PPT: 这是一份中考化学一轮复习金属的化学性质课件PPT,共19页。PPT课件主要包含了②作照明弹,④真金不怕火炼,差异性,设计该实验的依据,Cu>Ag,Al>Cu,Fe>H,H>Cu,Fe>Cu,两金夹一盐两盐夹一金等内容,欢迎下载使用。
2021年人教版九年级化学中考知识点复习: 水、氢气 教学课件PPT: 这是一份2021年人教版九年级化学中考知识点复习: 水、氢气 教学课件PPT,共21页。PPT课件主要包含了H2O2,思路分析,电解水实验,实验装置,增强导电性,淡蓝色,氧两种元素,2微观反应等内容,欢迎下载使用。












