




人教版九年级上册课题2 原子的结构课文内容课件ppt
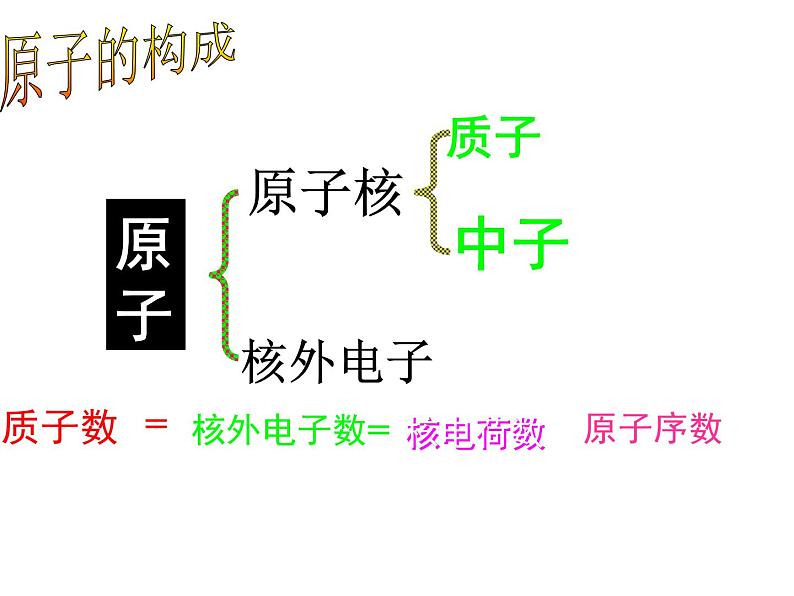
展开具有相同核电荷数(即核内质子数)的一类原子的总称
2.为什么元素的概念里不把(核外电子数)也放入概念里呢?
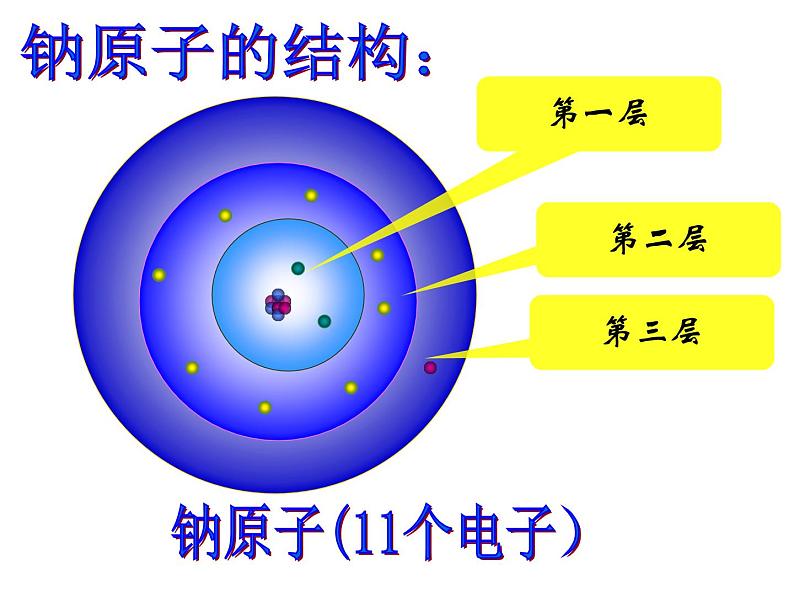
电子在原子核外一定区域内出现,这些区域叫作叫做“电子层”
核外电子是分层排布的:电子层:1 2 3 4 5 6 7 K L M N O P Q离核:近 远能量:低 高能量低的在离核近的区域运动,能量高的在离核远的区域运动
下图是1-18号元素的原子结构示意图,看图你能找出什么规律吗?
核外电子的排布规律:
⑴ 先排满内层, 后排外层;⑵ 第一层上最多排2个电子;⑶ 第二层上最多排8个电子;⑷ 最外层上最多排8个电子.
稀有气体元素的原子结构示意图
最外层具有8个电子(只有一个电子层的具有2个电子)的结构,属于相对稳定结构。
金属元素原子的结构示意图
金属元素,最外层电子一般少于4个,在化学反应中易失去电子,形成相对稳定结构
非金属元素原子结构示意图
非金属元素,最外层电子一般多于4个,在化学反应中易得到电子,形成相对稳定结构。
相对稳定结构不易得失电子
元素的化学性质与最外层电子数关系密切
根据下列结构示意图判断
其中属于稀有气体的是________属于金属元素的是______,属于非金属元素的是_______
练习:1、磷原子的结构示意图为: (1)磷原子核内有 个质子。共有____个电子层,最外层上有____电子。 (2)铝原子核外电子层数与磷原子的电子层数相同,但最外层电子数比磷原子最外层电子数少2个,则铝原子结构示意图为 。
钠在氯气中点燃生成氯化钠的形成过程:
1、离子:带电荷的原子或原子团
阳离子:带正电荷的原子叫做阳离子。 如: H+ 、Na+、 Mg2+ 、Al3+
阴离子:带负电荷的原子叫做阴离子。 如: O2- 、S2-、 F- 、Cl-、
写法:先写元素符号,再在元素符号右上角标所带电荷数及电性.例:
注意:只有1个电荷时,1省略不写
2、离子所带电荷数由该元素原子得失电子数目决定。
右上角“2+”的意义:
镁离子带2个单位的正电荷
你能说出4Mg2+的意义吗?
练一练:填空带3个正电荷的铁离子_____ 4O2-表示 _______ ,7个钠离子_____
注意: 原子和离子的联系和区别
议一议:物质与其构成粒子之间的关系
相同核电荷数的一类原子
[例1]六种粒子结构示意图分别为:(1)A、B、C、D、E、F共表示 种元素。(2)表示原子的粒子是 (填序号,下同)。(3)表示阳离子的粒子是 。(4)表示阴离子的是___________。
[2]某粒子结构示意图为
(1)x表示 ,该粒子有 个电子层,y与粒子的 关系非常密切。(2)当x=10+Y,该粒子为 (填类别)。(3)y=8时,该粒子带有2个单位的负电荷,该粒子的符号为 。(4)NaCl是由__________________构成。
(3)下列符号表示阳离子的是 ( )
下列各对微粒中,质子数相同,电子数也相同的是 ( ) A.S和S2- B.F-和Mg2+ C.Ne和H2O D.Na和Na+
金属元素在化学反应中一般较易_____电子,变成 离子,这是因为金属原子最外层电子数目一般 4个。
4.(2010·广东佛山)回答下列问题: (1)金属铁是由 (填“原子”、“分子”或“离子”,下同)构成的,氯化钠是由____ 构成的。 (2)原子得到或失去电子后形成离子。某离子的结构示意图为 ①当a= 时,该粒子是原子。 ②当a=8时,该粒子是 (填“原子”、“阳离子”或“阴离子”),其符号为 。 (3)氯化氢是一种无色有刺激性气味的气体,走进实验室就闻到了这种气味。从分子的角度解释这种象: 。
某离子带3个单位的正电荷,质子数为13,该离子的核外电子数为_____,该离子的名称是______,符号是____,该离子的结构示意图是:
初中化学课题2 原子的结构教课内容课件ppt: 这是一份初中化学课题2 原子的结构教课内容课件ppt,共25页。PPT课件主要包含了钠原子结构示意图,知识回顾,学生活动,知识点1离子的形成,例O2-,一个镁离子,Mg2+,表示3个镁离子,练一练,相对原子质量等内容,欢迎下载使用。
化学课题2 原子的结构示范课ppt课件: 这是一份化学课题2 原子的结构示范课ppt课件,共19页。PPT课件主要包含了原子体积很小,原子可以再分吗,现代原子构成,原子核,原子核比原子小得多,钠原子结构示意图,快速抢答,学生活动P54,面包里的葡萄干等内容,欢迎下载使用。
初中化学人教版九年级上册第五单元 化学方程式课题 2 如何正确书写化学方程式教课课件ppt: 这是一份初中化学人教版九年级上册第五单元 化学方程式课题 2 如何正确书写化学方程式教课课件ppt,共41页。