






人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构精品作业ppt课件
展开1.分子:保持物质化学性质的最小粒子;2.原子:化学变化中最小粒子;
课本P48:1滴水中大约有1.67×1021个水分子,说明分子很小。
阅读:课本P53看一下原子有多小?
问题:原子是最小的粒子吗? 它的内部是什么样子的?
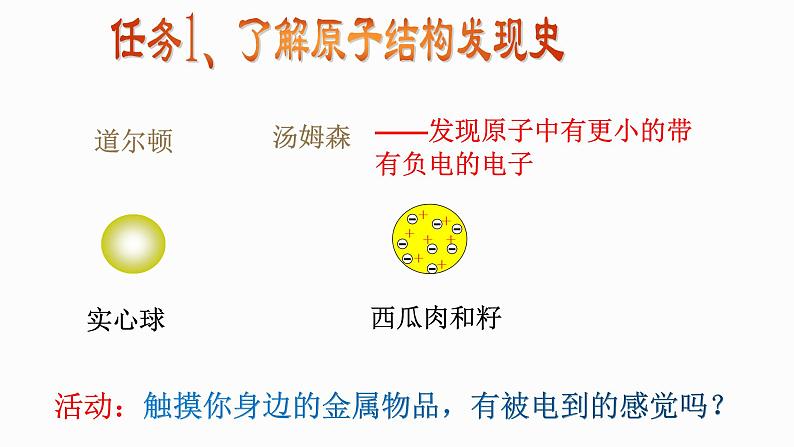
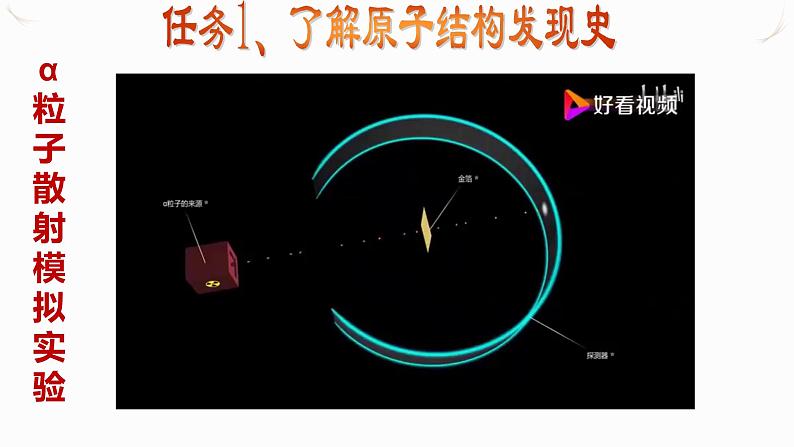
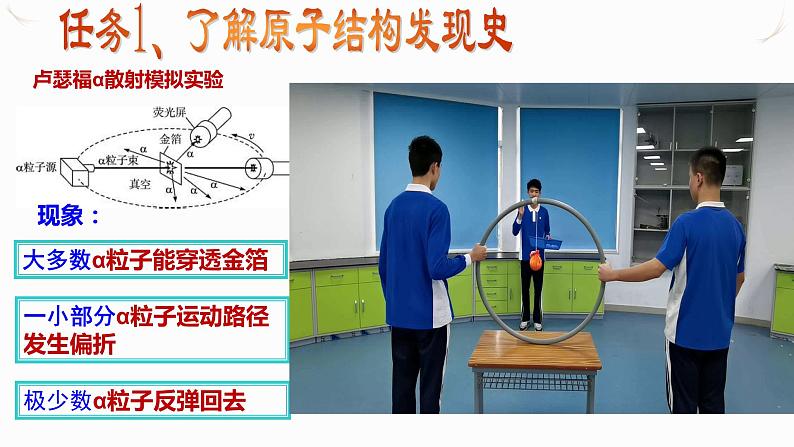
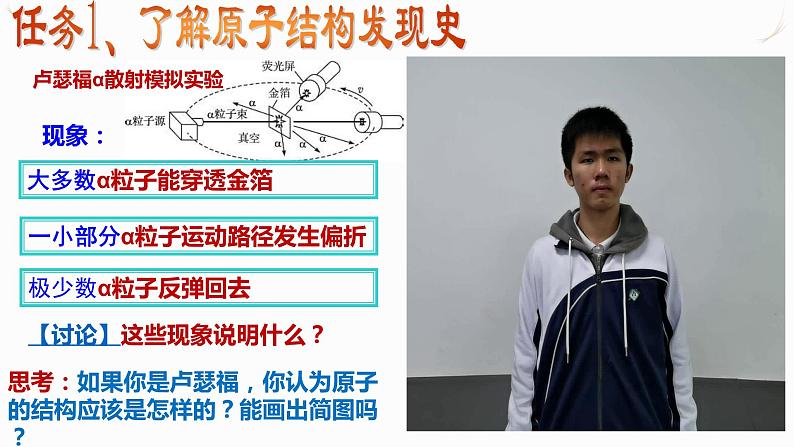
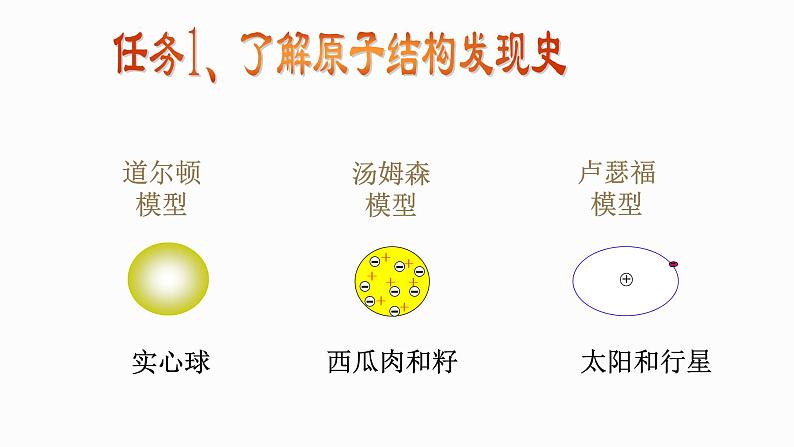
任务1、了解原子结构发现史
——发现原子中有更小的带有负电的电子
活动:触摸你身边的金属物品,有被电到的感觉吗?
一小部分α粒子运动路径发生偏折
大多数α粒子能穿透金箔
【讨论】这些现象说明什么?
思考:如果你是卢瑟福,你认为原子的结构应该是怎样的?能画出简图吗?
带 电
m很 v很 。
任务2、认识原子的构成
活动:根据科学家的模型完成学案中原子的构成部分内容
: 每个质子带一个单位正电荷(+)
: 每个电子带一个单位负电荷
问题:原子中质子和电子都带电,为什么原子不带电呢?
任务3、认识原子内部各粒子及关系
分析表格,能得到哪些信息?
1、在原子中:质子数 =核外电子数
2、原子核内不一定有中子
3、原子核内质子数不一定等于中子数
4、不同种类的原子质子数不同
原子的种类是由质子数所决定
任务4、研究原子核外电子的排布
原子核半径只有原子半径的万分之一至十万分之一。
如果把原子比作一个体育场,原子核只相当于一只蚂蚁
电子绕核以接近光速的速度作高速运动
原子核外电子运动的特征
电子在原子核外一定区域内出现,这些区域叫作叫做“电子层”,核外电子是在不同的电子层内运动的,此现象叫做核外电子的分层排布。
1、核外电子的分层排布
电子能量越低,离核越近;能量越高,离核越远。
最少有1层,最多有7层。
2、核外电子分层排布的规律
(1)由内向外,第一层排满才能排第二层,依次类推。
(2)第一层最多排2个,第二层最多排8个,
(3)最外层电子数最多排8个。(只有一个电子层,此时最外层电子数不超过两个)
那我们如何更简单方便的表示核外电子的这种排布规律呢?
2 8 1
3、Na原子结构示意图
请画出镁原子和氯原子的原子结构示意图:
1、原子中,质子数=核外电子数=核电荷数2、质子的个数决定原子的种类
( )1.下列有关原子结构的说法中正确的是A.原子由质子和电子构成 B.原子核一定由质子和中子构成C.原子核内的质子数与其核电荷数相等 D.原子核内的质子数与中子数一定相等
( )2.某原子结构示意图如图所示,该原子A.核电荷数为32 B.核外电子数为6 C.最外层电子数为2 D.核外电子层数为3
( )3.如图为某原子结构模型的示意图,其中a、b、c是构成该原子的三种不同粒子。下列说法正确的是 A.该原子有四个电子层B.原子中b与c的数目一定相同C.a表示电子,b表示质子D.原子中a与c的数目一定相同
( )4.某原子的结构示意图为 则核电荷数n为A.18 B.16 C.8 D.2
n=x+y+3x=16
( )5.推理是研究和学习的一种重要方法。正电子、负质子都是反粒子,它们跟通常所说的电子、质子相比较,质量相等,但电性相反。科学家已发现反氢原子,你推测反氢原子的结构可能是A.由一个带负电的质子和一个带正电的电子构成B.由一个带正电的质子和一个带正电的电子构成C.由一个带负电的质子和一个带负电的电子构成D.由一个带正电的质子和一个带负电的电子构成
初中化学人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构教课ppt课件: 这是一份初中化学人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构教课ppt课件,共21页。PPT课件主要包含了课前导入,课堂探究,原子的质量测定值,碳原子质量,碳原子质量的112,Ar=,定义式,近似值,测定出来绝对的,比较得出相对的等内容,欢迎下载使用。
化学第三单元 物质构成的奥秘课题2 原子的结构示范课课件ppt: 这是一份化学第三单元 物质构成的奥秘课题2 原子的结构示范课课件ppt,共32页。PPT课件主要包含了微粒构成物质,金箔-黄金锤成的薄片,原子还能再分吗,请说出你的猜想,请说出你的证据,原子不能再分的证据,原子能再分的证据,电子的发现,建立模型,科学实验等内容,欢迎下载使用。
人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构多媒体教学课件ppt: 这是一份人教版九年级上册第三单元 物质构成的奥秘课题2 原子的结构多媒体教学课件ppt,共46页。PPT课件主要包含了核外电子的排布,原子结构示意图,离子的形成,基础练习,能力提高等内容,欢迎下载使用。













