


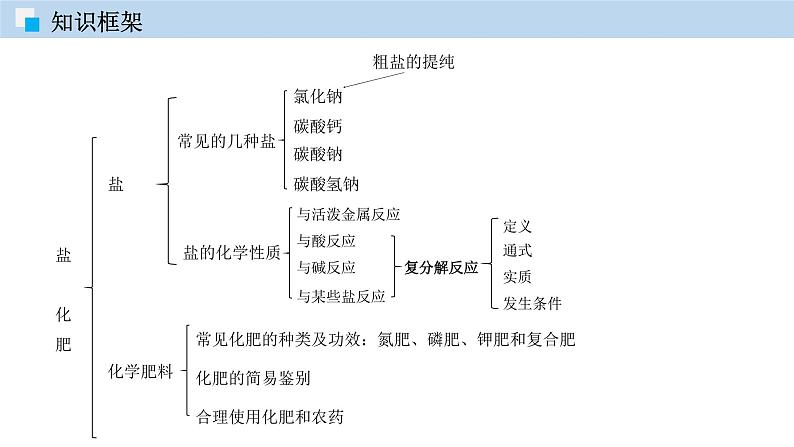



人教版九年级下册第十一单元 盐 化肥综合与测试复习课件ppt
展开常见化肥的种类及功效:氮肥、磷肥、钾肥和复合肥
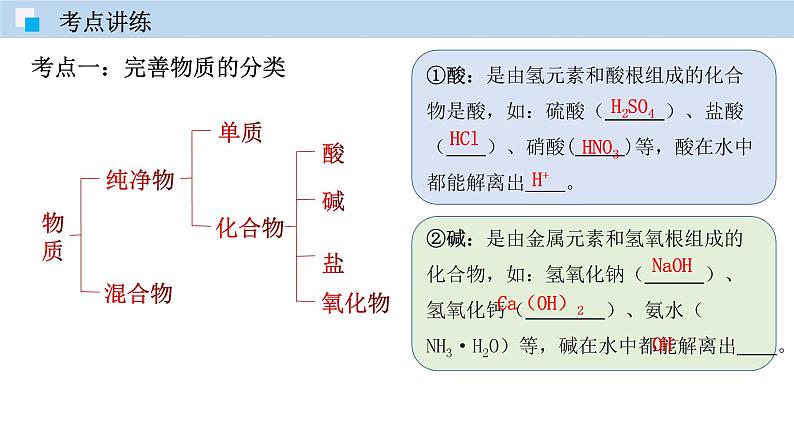
考点一:完善物质的分类
1.(2020•奉贤区二模)关于酸、碱、盐组成的说法一定正确的是( )A.酸和碱一定含氢元素 B.酸和盐一定含氧元素C.碱和盐一定含金属元素 D.酸、碱、盐一定都含原子团
2.(2020•百色模拟)实验室制取二氧化碳的化学反应为:2HCl+CaCO3═CaCl2+CO2↑+H2O 中,其中没有涉及到的物质类别是( )A.酸B.碱 C.盐 D.氧化物
3.按一定的特点或规律对物质进行分类,给化学学习与研究带来很大的方便。下列各组物质中,符合“氧化物一酸一碱一盐”顺序排列的是( )A.CO2一H2CO3一CaCO3一Ca(HCO3)2B.H2O一HNO3一NH3•H2O一NH4NO3C.HClO一HCl一Mg(OH)2一MgCl2D.SO3一NaHSO4一NaOH一Na2SO4
大理石、石灰石主要成分
1.(2020秋•沂源县期中)下列有关酸、碱、盐的用途的说法错误的是( )A.氯化钠是重要的调味品和食品添加剂B.浓硫酸在生产化肥、农药、炸药、医药等领域广泛应用C.小苏打可用于焙制糕点、硬水软化、玻璃生产等D.浓盐酸可用于制药、作除锈剂等
2.(2020秋•江北区期中)在日常生活中,下列关于化学试剂的用途描述错误的是( )A.碳酸钙用作补钙剂 B.亚硝酸钠用于腌制食品C.盐酸用于配制药品 D.熟石灰用于配制波尔多液
3.(2020•赤峰)下列物质既可以做治疗胃酸的胃药,又可以做面点发酵剂的是( )A.NaClB.NaOHC.NaHCO3D.Na2SO4
在金属活动性顺序表中,金属单质必须排在盐中金属的______;盐必须________;属于________反应。
(1)盐 + 金属 = 新盐 + 新金属
Fe+CuSO4== ;
(2)盐 + 酸 = 新盐 + 新酸
CaCO3+2HCl== ;
属于________反应
CaCl2+H2O+CO2↑
(3)盐 + 碱 = 新盐 + 新碱
CuSO4+2NaOH== ;
盐和碱都必须____________;属于________反应
(4)盐 + 盐 = 新盐 + 新盐
Na2CO3+BaCl2= ;
两种盐都必须____________;属于________反应
Cu(OH)2↓+Na2SO4
BaCO3↓+2NaCl
1.(2020•凤凰县模拟)春秋末期齐国的工艺官书《考工记》中载有“涑帛”的方法,即利用“灰”(草木灰主要成分碳酸钾)和“蜃”(贝壳灰:主要成分氢氧化钙)混合加水所得液体来洗涤丝帛。这种液体能洗涤丝帛主要是因为其中含有( )A.CaCO3 B.Ca(OH)2C.KOHD.K2CO3
2.(2020•长春模拟)小明欲探究石灰石与一定量的稀盐酸反应后的废液成分,向其中逐滴加入碳酸钠溶液,测得反应过程中产生沉淀的质量滴加入碳酸钠溶液的质量变化的关系如图所示。
(1)石灰石主要成分的化学式为 ;(2)生成沉淀的化学方程式为 ;(3)根据图象判断,废液中溶质的化学式为 。
CaCl2+Na2CO3═CaCO3↓+2NaCl
1.定义:两种化合物互相交换成分生成另外两种化合物,像这样的反应叫做复分解反应。
AB + CD ==
CB + AD
酸、碱、盐所电离出的离子相互结合生成沉淀、气体或水的过程。
4.复分解反应发生的条件:
有沉淀生成或有气体放出或有水生成。
1.(2020•铁岭模拟)下列各组物质中,能发生反应且反应前后溶液总质量保持不变的是( )A.镁和硫酸亚铁溶液 B.氧化铜固体和稀硫酸C.稀盐酸和烧碱溶液 D.碳酸钠溶液和硝酸钾溶液
2.(2020•柳州模拟)现有Zn、CuO、FeCl3、NaOH、稀盐酸五种物质,在常温下它们两两发生化学反应的个数为( )A.7个B.6个C.5个D.4个
3.(2020秋•芝罘区期中)对化学反应A+B═C+D的下列说法中正确的是( )A.若A是稀硫酸,则生成物质中一定有水B.若C、D是盐和水,则A、B不一定是酸和碱C.若A是可溶性碱,B是可溶性盐,则C、D不可能是两种沉淀D.若A、B各取10g混合,使其充分反应,则C、D质量的总和一定等于20g
考点五:常见化肥的种类和功效
1.常用化肥的种类有______、_____、______、或含有N、P、K三种元素中两种或三种的______。
1.(2020•鞍山)下列化肥属于钾肥的是( )A.K2SO4B.CO(NH2)2C.NH4H2PO4 D.Ca(H2PO4)2
2.(2020•绥化)同学们夏季郊游时,发现稻田里的水稻叶子发黄并倒下了一片,都认为应该向稻田中施用的复合肥是( )A.NH4NO3 B.KNO3 C.Ca3(PO4)2D.KCl
考点六:化肥的简易区分
大多数不溶于水或部分溶于水
【注意】除了尿素以外的其它氮肥都可以和熟石灰研磨产生刺激性气味。
化学方程式:______________________________________________________________________________________。
铵态氮肥不能与碱性肥料一起使用的原因: 。
(NH4)2SO4+Ca(OH)2===CaSO4+2H2O+2NH3↑;2NH4Cl+Ca(OH)2===CaCl2+2H2O+2NH3↑
能与碱性物质反应,降低肥效
1.(2020•广东模拟)下列化肥从气味即可与其他化肥区分开的是( )A.NH4HCO3 B.NH4Cl C.KNO3 D.(NH4)2SO4
2.(2019•河池)下列化肥中,从外观即可与其他化肥相区别的是( )A.硫酸钾B.硝酸铵C.磷矿粉D.尿素
3.(2020秋•肇州县期末)实验室有三瓶化肥未贴标签,只知道它们分别是碳酸氢铵(NH4HCO3)、氯化铵(NH4Cl)和尿素[CO(NH2)2]中的一种。为鉴别三种化肥,某同学分别取少量样品编号为A、B、C,并进行如图实验(此处箭头表示得出实验结论):
根据上述实验回答:(1)写出三种化肥的名称:A ;B ;C 。(2)如果实验Ⅱ中B、C两种样品没有另取,对实验结果 (填“有”或“无”)影响。(3)常温下如要鉴别B、C两种样品, (填“能”或“不能”)采取闻气味的方法。(4)写出操作Ⅱ中涉及的化学反应的方程式: 。
NH4HCO3+HCl═NH4Cl+H2O+CO2↑
难点一 物质的共存问题
【变式训练】(2020•常德)化学实验探究活动中,小明对某溶液溶质成分的几种猜测中合理的是( )A.H2SO4 NaOH NaClB.KNO3 NaCl CuSO4C.Na2CO3 NH4Cl HClD.MgCl2 Na2SO4 KOH
【例1】(2020•鞍山)下列各组物质在水中能大量共存,且形成无色透明溶液的是( )A.CuSO4、KCl、HCl B.K2SO4、NaOH、NH4ClC.HNO3、NaCl、Ca(OH)2 D.KNO3、Na2SO4、NaCl
难点二 物质的除杂
【例2】(2020•鞍山)除去下列物质中的少量杂质,所用操作方法正确的是( )
【变式训练】(2020•赤峰)除去下列物质中的少量杂质(括号内为杂质),其操作不正确的是( )A.Cu粉(Fe粉)﹣﹣用磁铁吸引B.N2(O2)﹣﹣将混合气体通过灼热的铜丝网C.CO(CO2)﹣﹣将混合气体通过灼热的氧化铁粉末D.MnO2(KCl)﹣﹣将混合物溶解于水、过滤、洗涤、干燥
难点三 物质的推断
【例3】(2020•南宁)甲、乙、丙、丁是初中化学常见的物质,它们的转化关系如图所示(反应条件已省略)。下列说法正确的是( )
A.若丁是水,则该反应一定属于中和反应B.若丙是沉淀,则甲、乙中一定有一种物质是盐C.若甲、丁均为单质,乙和丙均为化合物,则该反应一定属于置换反应D.若乙是一种碱、丁是一种盐,则该反应一定属于复分解反应
【变式训练】(2020•呼和浩特)现有一包固体粉末,可能是由CaCO3、Na2CO3、Na2SO4、NaCl、Ba(NO3)2中的一种或几种组成。为确定其成分,进行下列实验(微溶物质按可溶处理)。①取少量固体粉末于试管中,加足量的水溶解,静置后得到白色沉淀A和无色溶液B;②过滤,将白色沉淀A放入试管中,滴加过量的稀硝酸,有气泡产生,沉淀部分溶解;③取无色溶液B少许于试管中,滴加过量的稀硝酸,有气泡产生,得到溶液C;④在溶液C中滴加硝酸银溶液,有白色沉淀产生。以下说法正确的是( )A.白色沉淀A的成分是BaSO4和CaCO3B.该固体粉末中一定有CaCO3、Na2SO4、Na2CO3和Ba(NO3)2C.无色溶液B中的溶质一定有NaNO3、Na2CO3和NaClD.该固体粉末中一定有Na2SO4、Ba(NO3)2和Na2CO3,可能有CaCO3和NaCl
难点四 物质的鉴别
【例4】(2020•天水)下列各组物质的溶液,不用其他试剂,无法将其一一区别的是( )A.(NH4)2SO4 NaCl NH4Cl Ba(OH)2B.H2SO4 NaOH Na2SO4 FeCl3C.CaCl2 Na2SO4 Na2CO3 NaNO3D.HCl H2SO4 BaCl2 K2CO3
【变式训练4】(2020•湘西州)能将硝酸银、碳酸钠、氯化钾三种溶液鉴别出来的试剂是( )A.铜丝B.硝酸钠溶液C.稀盐酸D.氢氧化钠溶液
难点五 物质的相互转化和制备
【例5】(2020•赤峰)下列物质间的转化只通过一步反应就能实现的是( )A.H2O2→H2B.NaCl→AgClC.Fe→Fe2(SO4)3D.CuO→Cu(OH)2
1.(2020春•振安区校级期中)分类法是初中化学学习的一种重要方法,下列各组物质分类正确的是( )A.氧化物:P2O5 KClO3 O2B.碱:Cu(OH)2 Ba(OH)2C.酸:H2CO3 H2SO4 H2O2D.盐:NaNO3 CO(NH2)2
2.(2020•兴宁区校级模拟)“庄稼一枝花,全靠肥当家”,下列属于钾肥的是( )A.NH4NO3B.NH4H2PO4C.CO(NH2)2D.KHCO3
4.(2020秋•周村区期中)下列各组溶液混合后能发生反应且无明显现象的一组是( )A.NaNO3、NaCl、AgNO3B.CuSO4、H2SO4、BaCl2C.HCl、Na2SO4、NaOH D.HCl、NaHCO3、NaNO3
3.(2020•吴江区校级模拟)下列各组物质在同一无色溶液中能大量共存的一组是( )A.H2SO4、Na2SO4、KClB.CuSO4、MgCl2、NaOHC.KOH、NaCl、HClD.H2SO4、Na2CO3、NaNO3
5.(2020•老城区校级模拟)NaCl是重要的资源,其应用与生产如图所示。下列说法不正确的是( )
A.应用①操作的主要步骤为:计算、称量、溶解、装瓶、贴标签B.应用②在制备烧碱的过程中,水参与了反应C.应用③为提高产率应先通NH3,再通CO2,制备过程中还能得到一种化肥D.生产中提纯粗盐时可依次加入过量的BaCl2、NaOH、Na2CO3溶液,再过滤、蒸发
6.(2020•益阳模拟)学完酸碱盐知识,我们应该知道不少鉴别物质的方法。下列各组物质的溶液,不另加试剂就能将他们鉴别出来的是( )A.KCl KNO3 Na2CO3 Na2SO4B.BaCl2 Na2SO4 Na2CO3 NaClC.AgNO3 HCl NaCl HNO3D.CuCl2 NaOH HCl MgCl2
7.(2020•灌云县一模)下列反应不属于复分解反应的是( )A.H2SO4+Ca(OH)2═CaSO4+2H2OB.Ca(OH)2+CO2═CaCO3↓+H2OC.HCl+AgNO3═AgCl↓+HNO3D.H2SO4+BaCl2═BaSO4↓+2HCl
8.(2020•广东模拟)向AgNO3溶液中滴入NaCl溶液至恰好完全反应,如图表示反应前后溶液中存在的主要离子。(1)实验过程中观察到的现象是 。(2)写出该反应的化学方程式 。(3)写出“ ”表示的粒子的符号 。
NaCl+AgNO3═NaNO3+AgCl↓
(4)从图中可以看出该反应的本质是 。
银离子结合氯离子生成氯化银白色沉淀
9.(2020•安阳县模拟)向盐酸和氯化钙的混合溶液中逐滴滴入碳酸钠溶液,并用pH传感器连续监测,得到pH随时间的变化曲线如图所示。
(1)如果在原混合溶液中滴入少量紫色石蕊溶液,则AB段溶液的颜色变化为 。(2)请分析图示,写出BC段发生反应的化学方程式: ;图中CD段pH上升的原因是 。
碳酸钠溶液过量且碳酸钠溶液显碱性(合理即可)
安徽中考复习 人教版化学 教材基础 第十一单元 盐 化肥 课件: 这是一份安徽中考复习 人教版化学 教材基础 第十一单元 盐 化肥 课件,共30页。PPT课件主要包含了安徽中考考情,思维导图·建体系,知识清单·理脉络,金属离子,小苏打,NaCl,Na2CO3,NaHCO3,白色固体,易溶于水等内容,欢迎下载使用。
第十一单元 盐 化肥-中考化学一轮单元复习课件PPT: 这是一份第十一单元 盐 化肥-中考化学一轮单元复习课件PPT,共25页。PPT课件主要包含了思维导图,盐化肥,纯碱苏打,小苏打,NaHCO3,Na2CO3,金属离子或铵根离子,酸根离子,大理石,新盐+新金属等内容,欢迎下载使用。
人教版化学中考复习 11.第十一单元 盐 化肥 PPT课件+练习: 这是一份人教版化学中考复习 11.第十一单元 盐 化肥 PPT课件+练习,文件包含01第十一单元盐化肥pptx、05专项突破中和反应及反应后溶质成分的探究pptx、06专项突破碱变质的探究pptx、07专项突破无明显反应现象的探究pptx、03专项突破物质的检验和鉴别pptx、02专项突破物质的共存pptx、04专项突破物质的分离与除杂pptx、01第十一单元盐化肥docx、03专项突破物质的检验和鉴别docx、04专项突破物质的分离与除杂docx、05专项突破中和反应及反应后溶质成分的探究docx、06专项突破碱变质的探究docx、07专项突破无明显反应现象的探究docx、02专项突破物质的共存docx等14份课件配套教学资源,其中PPT共156页, 欢迎下载使用。














