
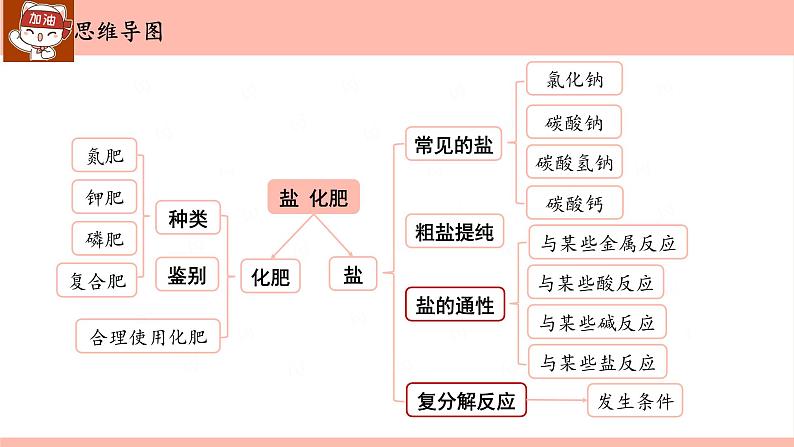



第十一单元 盐 化肥-中考化学一轮单元复习课件PPT
展开定义:组成里含有____________________和__________的化合物。 即酸→金属离子(或铵根离子) +酸根离子
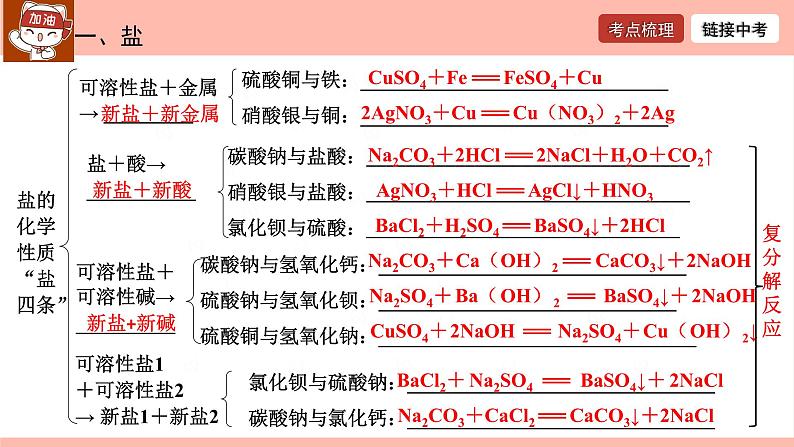
盐的化学性质“盐四条”
可溶性盐+金属→ _________
硫酸铜与铁:_______________________________硝酸银与铜:_______________________________
盐+酸→ ___________
可溶性盐+可溶性碱→ __________
碳酸钠与盐酸:_________________________________硝酸银与盐酸:_________________________________氯化钡与硫酸:________________________________
碳酸钠与氢氧化钙:_______________________________硫酸钠与氢氧化钡:______________________________硫酸铜与氢氧化钠:________________________________
可溶性盐1+可溶性盐2→ 新盐1+新盐2
氯化钡与硫酸钠:_______________________________碳酸钠与氯化钙:_______________________________
2AgNO3+Cu ══ Cu(NO3)2+2Ag
CuSO4+Fe ══ FeSO4+Cu
Na2CO3+2HCl ══ 2NaCl+H2O+CO2↑
AgNO3+HCl ══ AgCl↓+HNO3
BaCl2+H2SO4 ══ BaSO4↓+2HCl
Na2CO3+Ca(OH)2 ══ CaCO3↓+2NaOH
Na2SO4+Ba(OH)2 ══ BaSO4↓+2NaOH
CuSO4+2NaOH ══ Na2SO4+Cu(OH)2↓
BaCl2+Na2SO4 ══ BaSO4↓+2NaCl
Na2CO3+CaCl2 ══ CaCO3↓+2NaCl
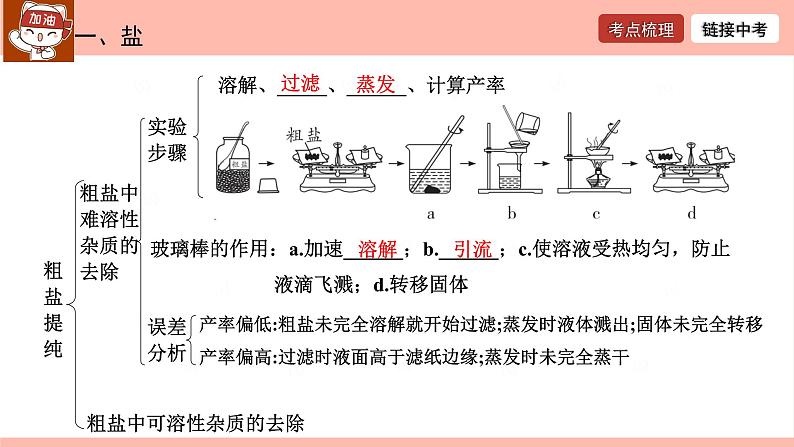
粗盐中难溶性杂质的去除
溶解、_____、______、计算产率
玻璃棒的作用:a.加速______;b.______;c.使溶液受热均匀,防止 液滴飞溅;d.转移固体
粗盐中可溶性杂质的去除
产率偏低:粗盐未完全溶解就开始过滤;蒸发时液体溅出;固体未完全转移产率偏高:过滤时液面高于滤纸边缘;蒸发时未完全蒸干
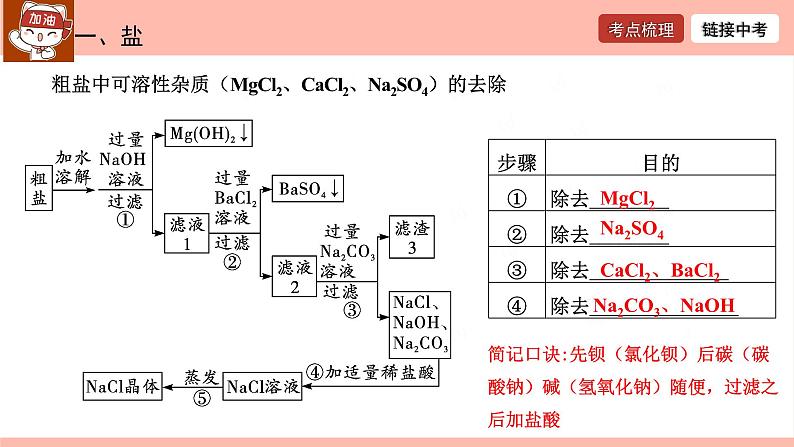
粗盐中可溶性杂质(MgCl2、CaCl2、Na2SO4)的去除
CaCl2、BaCl2
Na2CO3、NaOH
简记口诀:先钡(氯化钡)后碳(碳酸钠)碱(氢氧化钠)随便,过滤之后加盐酸
定义:由两种________相互交换成分,生成另外两种_______的反应表达式:AB+CD→AD+CB特点:“双交换,价不变”条件
生成物:有 或 或 生成
①酸+金属氧化物→盐+水②酸+碱→盐+水③酸+盐→新酸+新盐④碱+盐→新碱+新盐⑤盐1+盐2→盐3+盐4
当反应物中有酸时,另一种反应物可不溶于水当反应物中没有酸时,两种反应物必须都可溶于水
难溶性碱:Cu(OH)2(蓝色)、Fe(OH)3(红褐色)、Mg(OH)2(白色)等难溶性盐:AgCl、BaSO4、CaCO3、BaCO3均为白色沉淀溶解性口诀:钾钠铵硝皆可溶,盐酸盐中银不溶;硫酸盐不溶钡和铅,碳酸盐只溶钾钠铵。多数酸溶碱少溶,只有钾钠氨钡溶
Cl-——Ag+(AgCl↓)SO42-——Ba2+(BaSO4↓)HCO3-——H+(H2O+CO2↑)OH-
Ca2+、Ba2+等(生成沉淀)H+(H2O+CO2↑)
常见的不能共存的离子对
氮肥(含氮元素),如尿素[CO(NH2)2]、铵盐(如NH4Cl)和硝酸盐(如NH4NO3)磷肥(含磷元素),如磷矿粉[Ca3(PO4)2]、磷酸二氢钙[Ca(H2PO4)2]等钾肥(含钾元素),如硫酸钾(K2SO4)、氯化钾(KCl)等复合肥料(同时含有氮、磷、钾中的两种或三种营养元素), 如硝酸钾(KNO3)、磷酸二氢铵(NH4H2PO4)等
看外观:氮肥、钾肥为____色晶体,磷肥为______色粉末加水溶解:钾肥和氮肥都易溶,磷肥大多不溶或部分可溶
与熟石灰混合研磨,有________气味的气体产生与碱溶液共热,产生能使湿润的红色石蕊试纸______的气体
注意:铵态氮肥不能与 物质(如草木灰)混合施用,否则会放出有刺激性气味的氨气,降低肥效
化肥和农药对环境的影响
化肥:土壤污染或土壤退化(使土壤酸化、板结)、水体污染(使水体富营养化)、大气污染(产生氮化物和硫化物气体)农药:本身就是有毒物质,使用不当会污染环境、危害人体健康做法:合理施用化肥和农药,以尽量少的化肥和农药的投入、尽量小的对环境的影响来保持尽量高的农产品产量及保障食品品质
1.(2022成都)自然界中含氮化合物种类较多,下列物质属于盐的是( ) A.NO2 B.NH3C.NH4NO3 D.HNO32.(2022江西)合理使用食品添加剂可成就美食,维护健康。下列食 品添加剂与其作用不相符的是( ) A.食盐—调味剂B.蔗糖—甜味剂 C.碳酸钙—预防骨质疏松D.小苏打—预防甲状腺肿大3.(2022湖北宜昌)我国化学家侯德榜学成归国,发明了制碱新法“侯氏制碱法”,所制纯碱属于( ) A. 氧化物 B. 酸 C. 碱 D. 盐
命题点1 盐的性质和用途
4.(2022河南)如图是某胃药标签的部分文字说明。碳酸氢钠与胃酸(含盐酸)作用的化学方程式为_____________________________;如果将该胃药中的碳酸氢钠用相同质量的碳酸镁代替,则每次用药量应______(填“增加”“减少”或“不变“)。5.(2022扬州)石灰石的主要成分是CaCO3,下列说法不正确的是( ) A.CaCO3属于碳酸盐B.贝壳和珍珠中含有CaCO3 C.CaCO3易溶于水D.CaCO3可用作补钙剂
NaHCO3+HCl=NaCl+H2O+CO2↑
6.(2022湖南荆州)“天宫课堂”上航天员做的泡腾片实验,让同学们再次感受到化学的魅力。泡腾片中含有碳酸钠或碳酸氢钠等物质,化学兴趣小组决定对它们的某些性质进行探究。 实验一:探究碳酸钠和碳酸氢钠溶液的酸碱度【实验探究1】用pH试纸测得等浓度的碳酸氢钠溶液的pH为9,碳酸钠溶液的pH为11。【实验结论1】两者均显碱性,且溶液碱性较强的是 _________。
实验二:探究碳酸钠和盐酸的反应【实验探究2】向盛有碳酸钠溶液的烧杯中,逐滴加入一定浓度的稀盐酸并充分搅拌,测得pH变化与时间的关系如图1所示。观察到ab段无气泡产生,从b点开始产生气泡。经测定b点溶质只有碳酸氢钠和氯化钠,c点pH为7。【实验结论2】碳酸钠和盐酸的反应是分两步发生的,ab段发生反应的化学方程式为 ______________________________,c点溶液中的溶质为 __________。
Na2CO3+HCl=NaCl+NaHCO3
实验三:探究碳酸钠和碳酸氢钠的热稳定性【查阅资料】①碳酸氢钠受热分解成碳酸钠、水和二氧化碳; ②碳酸钠受热不分解。【实验验证】取一定量的碳酸氢钠放入试管中加热,如图2所示。【交流反思】试管A管口向下倾斜的原因是 ______________________________, 试管B中出现 _______________现象,证明有二氧化碳生成。【实验结论3】碳酸钠的热稳定性强于碳酸氢钠。【拓展应用】溶洞内钟乳石的形成原理与碳酸氢钠受热分解相似﹣﹣溶有碳酸氢钙[Ca(HCO3)2]的地下水,遇热或当压强突然变小时,碳酸氢钙会分解成碳酸钙沉积下来,天长日久就形成了千姿百态的钟乳石。请写出碳酸氢钙分解的化学方程式 _____________________________________________。
防止反应生成的水倒流使试管炸裂
7.(2022山东泰安)下列各组离子在pH大于7的溶液中,能大量共存的是( ) A.H+、Ba2+、 、 B.Mg2+、K+、 、Cl- C.Na+、Ba2+、 、 D.Na+、Ba2+、OH-、Cl-8.(2022齐齐哈尔)下列各组离子在pH=4的溶液中能大量共存,且形成无色溶液的是( ) A. Na+、Ca2+、Cl-B. 、K+、 C. Cu2+、C1-、D. Ba2+、A13+、
命题点2 复分解反应及其应用
9.(2022湖北)下列各组离子,在指定的溶液中能大量共存的是( ) A. pH=3的溶液中: Mg2+ B. pH=11的溶液中:Na+ K+ Cl- C. 无色溶液中:Cu2+ Al3+ Cl- D. 含有大量 的溶液中:Ba2+ H+ Cl- 10.(2022湖南常德)下列各组物质在水中能大量共存且溶液为无色、透明的是( ) A. NaOH、KNO3、MgCl2B. Na2CO3、HCl、BaCl2 C. KNO3、NaCl、H2SO4D. FeCl3、KCl、HCl
11.(2022四川眉州)某无色水溶液中可能含有以下离子中的几种:H+、Mg2+、Cu2+、C1-、 、 ,为确定其成分,小芳进行了以下实验: ①经测定,溶液pH=1; ②取部分未知溶液加入过量NaOH溶液,有白色沉淀产生,过滤; ③取②的部分滤液加入BaC12溶液,有白色沉淀产生。 分析上述实验,下列收对溶液中含有离子的判断正确的是( ) A. 一定含有H+、Mg2+,可能含有 B. 一定含有H+、Mg2+、 ,可能含有C1- C. 一定含有H+、Mg2+,可能含有Cu2+ D. 一定含有H+、Mg2+、 ,可能含有Cu2+、C1-
12.(2022广东中考)侯德榜是我国制碱工业的先驱,为纯碱和氮肥工业的发展作出了杰出贡献。工业纯碱中可能混有少量NaC1,同学们对工业纯碱样品展开探究。 探究一:确定纯碱样品中是否含有NaCI 有同学认为该实验方案有错误,正确方案应选用___(填字母)代替稀盐酸。 a.CaCl2溶液 b.稀硝酸 c.BaC12溶液
探究二:测定纯碱样品中Na2CO3的质量分数【方案1】将样品溶解,加入过量CaC12溶液,搅拌至反应完全。该反应的化学方程式为______________________________。过滤、洗涤、干燥,称量沉淀的质量,计算Na2CO3的质量分数。【方案2】如1图所示,取样品于锥形瓶中,加入足量稀盐酸。反应结束后,根据干燥管增重计算Na2CO3的质量分数。若结果大于100%,可能的原因是______________________________。【讨论】上述两个方案中,你认为方案______更优。
氢氧化钠固体吸收水蒸气或氯化氢气体
【拓展】2图为Na2CO3和NaC1的溶解度曲线。为提纯含少量NaC1的纯碱样品,将其浓溶液从t1℃冷却至t2℃,t1---t2的最优范围是______(填字母)。 a.40-10 b.60-30 c.70-40
13.(2022河南)粮食产量增长的主要动力是化肥。下列化肥(用化学式表示)属于复合肥料的是( ) A. CO(NH2)2 B. K2SO4 C. KNO3 D. Ca(H2PO4)214.(2022昆明)下列不属于氮肥的是( ) A.K2SO4 B.(NH4)2SO4C.NH4HCO3 D.CO(NH2)215.(2022长沙)棉花地里的棉花因为缺氮导致叶片发黄,我们应该施用的化学肥料是( ) A. KCl B. NH4NO3C. Ca3(PO4)2D. K2CO316.(2022邵阳)下列化肥中,从外观即可与其他化肥区别的是( ) A. 磷矿粉 B. 硫酸钾 C. 氯化钾D. 硝酸铵
17.(2022苏州)在粗盐初步提纯实验中,下列有关装置和操作正确的是( ) A. 溶解粗盐B. 过滤粗盐水 C. 蒸发结晶D. 趁热取下蒸发皿18.(2022安徽)完成“一定溶质质量分数的氯化钠溶液的配制”和“粗盐中难溶性杂质的去除”两个实验,都必须用到的仪器是( )A.玻璃棒 B.酒精灯C.漏斗 D.试管
中考化学一轮单元总复习课件 第十一单元 盐 化肥 (含答案): 这是一份中考化学一轮单元总复习课件 第十一单元 盐 化肥 (含答案),共58页。PPT课件主要包含了核心知识·建构脉络图,主干回顾·厚积知识力,金属离子,酸根离子,白色沉淀,CO2,稀盐酸,澄清石灰水,复分解反应,浅绿色等内容,欢迎下载使用。
中考化学一轮单元总复习课件 第十一单元 盐 化肥 (含答案): 这是一份中考化学一轮单元总复习课件 第十一单元 盐 化肥 (含答案),共58页。PPT课件主要包含了核心知识·建构脉络图,主干回顾·厚积知识力,金属离子,酸根离子,白色沉淀,CO2,稀盐酸,澄清石灰水,复分解反应,浅绿色等内容,欢迎下载使用。
中考总复习化学(安徽地区)第十一单元单元 盐 化肥课件: 这是一份中考总复习化学(安徽地区)第十一单元单元 盐 化肥课件,共60页。PPT课件主要包含了目录安徽·中考,实验粗盐提纯,常见盐的性质和用途,命题点1,澄清石灰水,不正确,复分解反应,蒸发溶剂合理即可,分解反应,用作化肥合理即可等内容,欢迎下载使用。












