




化学选修4 化学反应原理第四章 电化学基础第一节 原电池多媒体教学课件ppt
展开电化学:指研究化学能与电能之间相互转 换的装置、过程和效率的科学。
过程及装置分按电化学反应
2. 借助电流而发生反应及装置 (如:电解池)
1. 产生电流的化学反应及装置 (如:原电池等)
1、原电池的定义:2、原电池反应的本质:3、构成原电池的条件:
将化学能转化为电能的装置叫做原电池。
①两个活动性不同的金属(或其中一种为 非金属,即作导体用)作电极。②电解质溶液③形成闭合回路④在这种电解质溶液中能自发地进行氧化还原反应
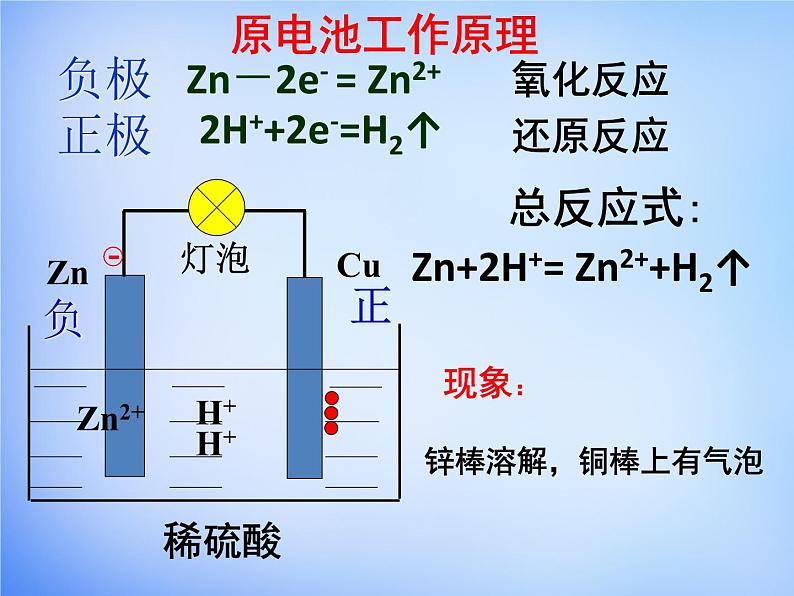
Zn-2e- = Zn2+
2H++2e-=H2↑
Zn+2H+= Zn2++H2↑
锌棒溶解,铜棒上有气泡
活泼金属失电子变阳离子
总反应:负极金属与电解质溶液的离子反应
5、原电池的正负极的判断方法
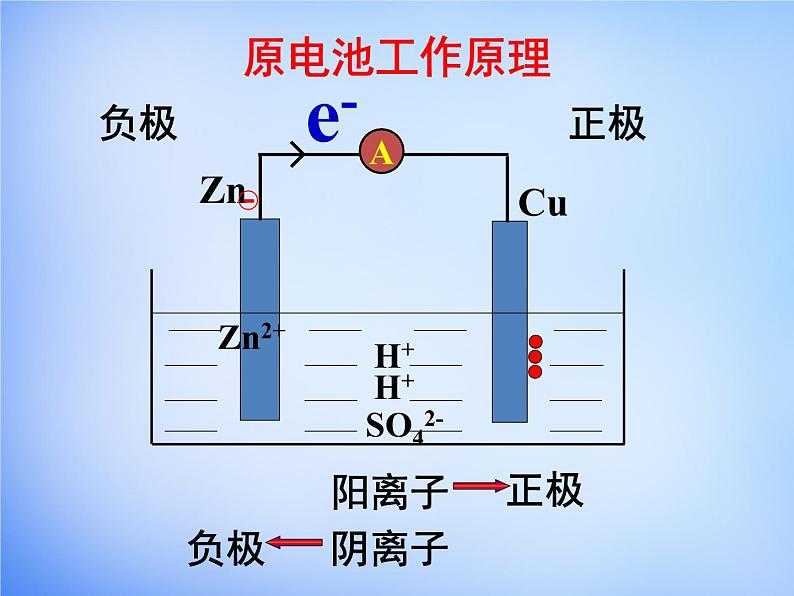
微观判断(根据电子流动方向)
电子流出的极电子流入的极
较活泼的电极材料较不活泼的电极材料
质量增加的电极工作后 质量减少的电极
工作后,有气泡冒出的电极为正极
发生氧化反应的极发生还原反应的极
宏观判断:①根据电极材料②根据原电池电极发生的反应③根据电极质量的变化④根据电极有气泡冒出:
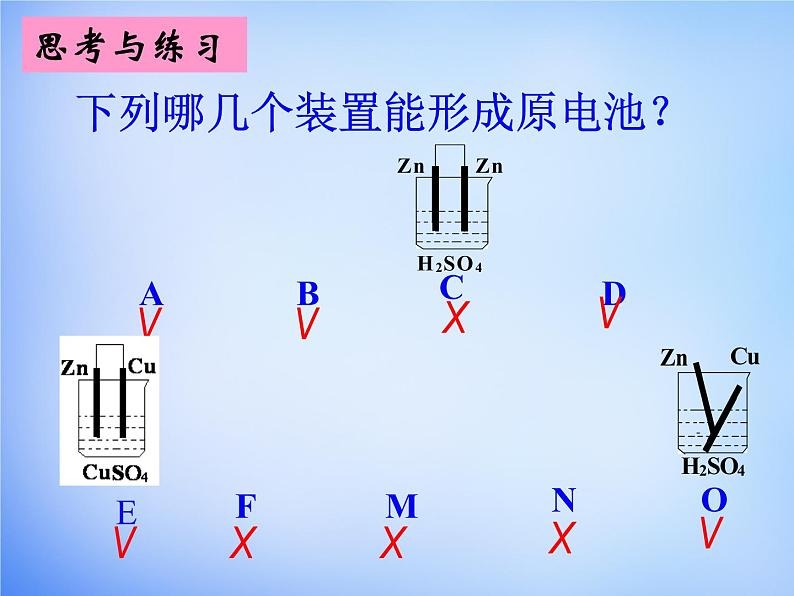
下列哪几个装置能形成原电池?
思考:如何才能得到持续稳定的电流?
分析: 由于锌片与硫酸铜溶液直接接触,铜在锌片表面析出,锌表面也构成了原电池,进一步加速铜在锌表面析出,致使向外输出的电流强度减弱。当锌片表面完全被铜覆盖后,不再构成原电池,也就没有电流产生。
对锌铜原电 池工作原理的进一步探究
在原有实验基础上进行改进,设计成一个能产生持续稳定电流的原电池。
由两个半电池组成,锌和锌盐组成锌半电池,铜和铜盐组成铜半电池;每个半电池中的电极与电解质溶液互不反应,中间通过盐桥连接形成闭合回路。
(1)是离子通道,与外电路的电子通道相衔接;(2)是离子库,为保持溶液电中性,氧化作用产生的Zn2+需要阴离子来补充,Cu2+发生还原反应,需要阳离子来补充;而作为KCl饱和溶液盐桥有足够的离子供给,所以是离子库。
盐桥制法:将热的琼胶溶液倒入U形管中(注意不要产生裂隙),将冷却后的U形管浸泡在KCl或NH4NO3的饱和溶液中即可。
Zn-2e-= Zn2+
Cu2++2e- = Cu
Zn+Cu2+= Zn2++Cu
Zn-2e-=Zn2+
失e-,沿导线传递,有电流产生
Cu2++2e- =Cu
铜锌双液原 电 池 原 理
①活泼性不同 的两种金属。如锌铜原电池,锌作负极,铜作正极②金属和非金属。如锌锰干电池,锌作负极,石墨棒作正极③金属和化合物。如铅蓄电池,铅块作负极,PbO2作正极④惰性电极。如氢氧燃料电池中,两根电极均可用Pt
(2)电池的电极材料必须能导电
(1)电解质溶液一般要能够与负极发生反应。但若是两个半反应分别在两个烧杯中进行,则左右两个烧杯中的电解质溶液应 与电极材料具有相同的阳离子。
1.根据上述原理,为获得较长时间的稳定电流,如何将必修2中由“Zn-稀H2SO4-Cu”组成的原电池(如左下图)进行简单改装?
课堂练习(上述原理的应用)
练习: 利用Fe + Cu2+=Fe2+ +Cu设计一个原电池,画出示意图,写出电极反应。
负极:Fe – 2e- =Fe2+
正极:Cu2+ +2e- =Cu
请根据氧化还原反应 :Cu +2 Fe3+ = Cu2+ + 2Fe2+设计成原电池。你有哪些可行方案?
Cu Cu – 2e- = Cu2+
比Cu不活泼的金属或石墨2Fe3+ + 2e- = 2Fe2+
Fe2(SO4 )3、FeCl3等
负极:正极:电解质溶液:
若是采用烧杯和盐桥装置图,采用的电解质溶液又是什么?
2. 依据氧化还原反应: 2Ag+(aq) + Cu(s) == Cu2+(aq) + 2Ag(s) 设计的原电池如图所示,请回答下列问题:
(1)电极X的材是 ; 电解质溶液Y是 ;(2)银电极为电池的 极, 发生的电极反应为 ;
X电极上发生的电极反应为 ;(3)外电路中的电子是从 电极 流向 电极。
3.控制适合的条件,将反应2Fe3++2I- ⇌ 2Fe2++I2 设计成如右图所示的原电池。下列判断不正确的是 A. 反应开始时,乙中石墨电极上发生氧化反应 B. 反应开始时,甲中石墨电极上Fe3+被还原 C. 电流计读数为零时,反应达到化学平衡状态 D. 电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极
7、原电池的表示方法: (-) Zn|Zn2+ (C1) ‖ Cu2+ (C2)|Cu (+) “|”表示液-固相有一界面;“‖”表示盐桥。 在有气体参加的电池中还要表明气体的压力,溶液要表明浓度。
(1)比较金属活动性强弱。
例1 下列叙述中,可以说明金属甲比乙活泼性强的是( )A.甲和乙用导线连接插入稀盐酸溶液中,乙溶 解,甲上有H2气放出;B.在氧化–还原反应中,甲比乙失去的电子多;C.将甲乙作电极组成原电池时甲是负极;D.同价态的阳离子,甲比乙的氧化性强;
(2)比较反应速率快慢
例2 :下列制氢气的反应速率最快的是( )A.纯锌和1ml/L 硫酸;B.纯锌和18 ml/L 硫酸;C.粗锌和 1ml/L 盐酸;D.粗锌和1ml/L 硫酸的反应中加入几滴CuSO4溶液。
(3)比较金属腐蚀的快慢
下列各情况,在其中Fe片腐蚀由快到慢的顺序是
下列装置中四块相同的Zn片,放置一段时间后腐蚀速率由慢到快的顺序是
(4)判断溶液pH值变化
在Cu-Zn原电池中,200mLH2SO4 溶液的浓度为0.125ml/L , 若工作一段时间后,从装置中共收集到 0.168L升气体,则流过导线的电子为———— ml,溶液的pH值为_________?(溶液体积变化忽略不计)
y =0.015 (ml)
x =0.015 (ml)
=3.75× 10﹣ 4(ml/L )
∴pH =-lg3.75 ×10-4
=4 -lg3.75
Zn-2e-=Zn2+
2H++2e- =H2↑
2 2 22.4
x y 0.168
0.2×0.125×2
2H+ —— 2e——H2↑
(5)原电池原理的综合应用
例6:市场上出售的“热敷袋”的主要成分为铁屑、炭粉、木屑、少量氯化钠和水等。 “热敷袋”启用之前用塑料袋使其与空气隔绝,启用时,打开塑料袋轻轻揉搓就会放出热量。使用完后,会发现有大量铁锈存在。“热敷袋”是利用 放出热量。2)炭粉的主要作用是 。3)加入氯化钠的主要作用是 。4)木屑的作用是 。
与铁屑、氯化钠溶液构成原电池,加速铁屑的氧化.
氯化钠溶于水,形成电解质溶液.
摩擦生热,产生启动反应的热量,使用“热敷袋”时受热均匀.
高中化学人教版 (新课标)选修4 化学反应原理第一节 原电池集体备课课件ppt: 这是一份高中化学人教版 (新课标)选修4 化学反应原理第一节 原电池集体备课课件ppt,共28页。PPT课件主要包含了第一节原电池,探究一,探究二,探究三等内容,欢迎下载使用。
人教版 (新课标)选修4 化学反应原理第一节 原电池教课ppt课件: 这是一份人教版 (新课标)选修4 化学反应原理第一节 原电池教课ppt课件,共41页。PPT课件主要包含了原电池原理,电极反应式,总反应式,锌铜原电池工作原理,实验探索,不可以,电极方程式的书写,练一练,解释某些化学现象,原电池原理应用等内容,欢迎下载使用。
人教版 (新课标)选修4 化学反应原理第一节 原电池教课课件ppt: 这是一份人教版 (新课标)选修4 化学反应原理第一节 原电池教课课件ppt,共27页。PPT课件主要包含了Zn2+,阳离子,阴离子,SO42-,原电池工作原理,外部条件,组成原电池的条件等内容,欢迎下载使用。













