




高中化学第二节 元素周期律图片课件ppt
展开周期性:每隔一定数目或时间重复出现的某种变化,这种重复不是简单机械的重复,而是在变化中重复,在重复中变化。
起床、早读、上课、中午饭、午睡、上课、晚饭、晚自习、睡觉……
讨论:我们所知道的周期
第1课时 原子核外电子排布
化学元素也具体周期性规律
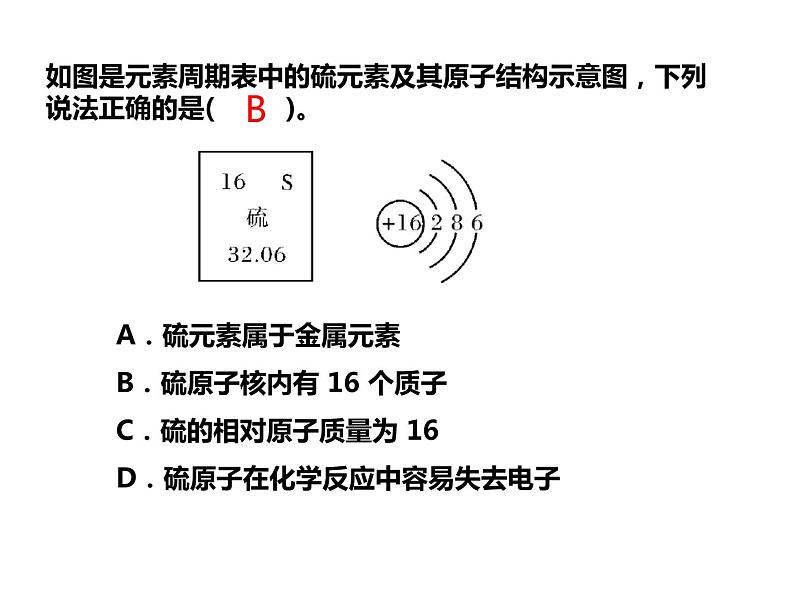
如图是元素周期表中的硫元素及其原子结构示意图,下列说法正确的是( )。
A.硫元素属于金属元素B.硫原子核内有 16 个质子C.硫的相对原子质量为 16D.硫原子在化学反应中容易失去电子
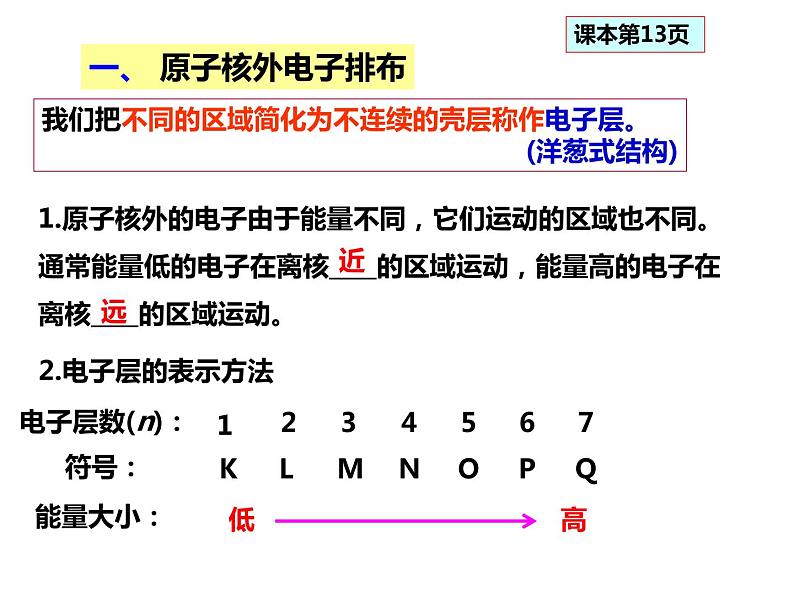
一、 原子核外电子排布
1.原子核外的电子由于能量不同,它们运动的区域也不同。通常能量低的电子在离核____的区域运动,能量高的电子在离核____的区域运动。
我们把不同的区域简化为不连续的壳层称作电子层。 (洋葱式结构)
3.核外电子的排布规律
(1)按能量由低到高,即由内到外,分层排布。
(4)次外层电子数不超过____个;倒数第三层不超过___个。
(2)各电子层最多容纳的电子数是 2n2(n 表示电子层)
(3)最外层电子数不超过_____个(K 层是最外层时,最多不超过____个)。
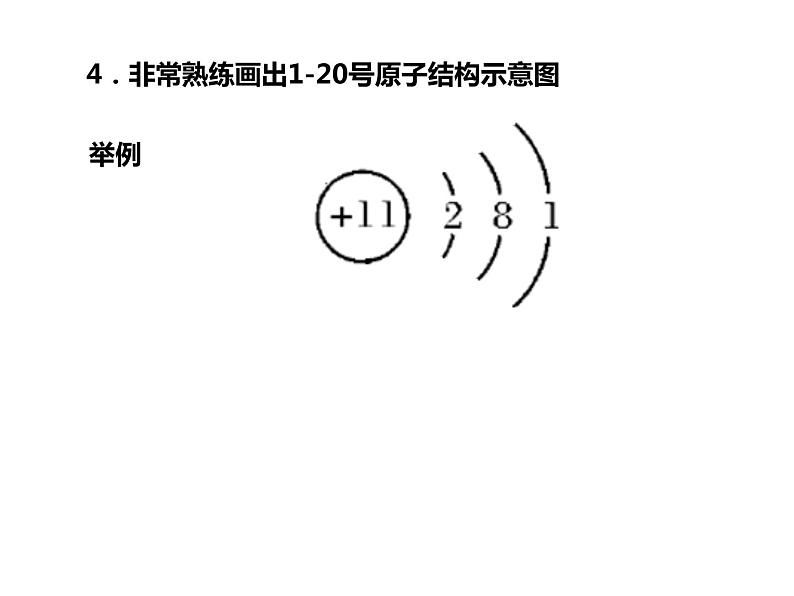
4.非常熟练画出1-20号原子结构示意图
写出下面的原子或离子结构示意图
氮原子结构示意图为_______________氯离子结构示意图_______________镁离子结构示意图为_______________
(1)下图横坐标为原子,纵坐标为原子的最外层电子数,找出各原子的最外层电子数,连线起来,观察有什么规律吗?
(1)下图横坐标为原子,纵坐标为原子的最外层电子数,找出各原子的最外层电子数,描点,观察有什么规律吗?
1.随着原子序数的递增,元素的原子核外层电子排布呈现周期性变化。
(2)下图横坐标为1到18号原子,纵坐标为主要化合价,找出各元素主要化合价,找点,观察有什么规律?
2.随着原子序数的递增,元素的化合价呈现周期性变化 。
主族元素的最高正价=
元素的化合价呈现周期性变化之外,观察课本第15页第一个表格,还有以下规律:
│最高正价│+│负价│=
0.152nm 0.071nm
0.186nm 0.099nm
3.随着原子序数的递增,元素的原子半径呈现周期性变化 。
同周期从左到右,原子半径逐渐 ;
同族从上到下,原子半径逐渐 ;
通过上述探究,我们发现随着原子序数的递增,元素的______________________ 、__________________和__________________都呈现周期性变化。
化学第1节 原子结构与元素性质优质课件ppt: 这是一份化学第1节 原子结构与元素性质优质课件ppt,共12页。PPT课件主要包含了质子数,原子核,核外电子,原子是电中性的,质量数,AZ个,知识回顾,核外电子排布规律,原子结构示意图等内容,欢迎下载使用。
人教版 (2019)选择性必修2第一节 原子结构评课课件ppt: 这是一份人教版 (2019)选择性必修2第一节 原子结构评课课件ppt,共60页。PPT课件主要包含了课前·新知导学,概率密度,哑铃状,空间运动状态,微思考,单独分占,原子轨道,课堂·素养初培,情境导入,深化理解等内容,欢迎下载使用。
高中化学人教版 (新课标)必修2第二节 元素周期律备课课件ppt: 这是一份高中化学人教版 (新课标)必修2第二节 元素周期律备课课件ppt,共33页。PPT课件主要包含了元素周期律,元素位置,2非金属元素中,元素的原子半径递变,金属性依次增强,元素的性质递变小结,元素相对位置,是解题的关键,KOH,HClO4等内容,欢迎下载使用。













