

高中人教版 (2019)第二节 离子反应第1课时学案及答案
展开第1课时 电解质的电离
目标与素养:1.了解电解质的概念。(宏观辨识)2.了解酸、碱、盐在水溶液中的电离及导电条件。(宏观辨识与微观探析) 3.会书写电解质的电离方程式。(宏观辨识与微观探析)
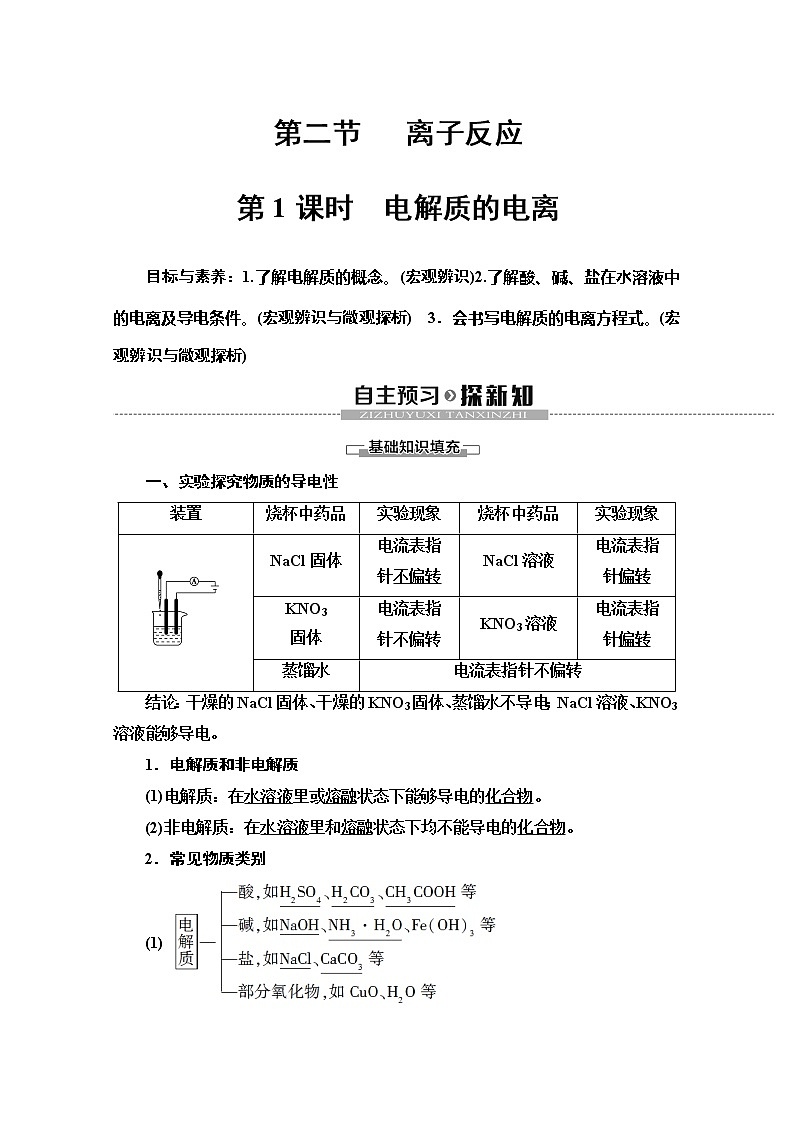
一、实验探究物质的导电性
结论:干燥的NaCl固体、干燥的KNO3固体、蒸馏水不导电;NaCl溶液、KNO3溶液能够导电。
1.电解质和非电解质
(1)电解质:在水溶液里或熔融状态下能够导电的化合物。
(2)非电解质:在水溶液里和熔融状态下均不能导电的化合物。
2.常见物质类别
(1)
(2)
微点拨:氨气、二氧化硫、二氧化碳的水溶液能导电,是因为它们与水反应生成电解质NH3·H2O、H2SO3、H2CO3,而氨气、二氧化硫、二氧化碳都是非电解质。氨水是混合物不是电解质。
3.电解质导电的原因
二、酸、碱、盐在水溶液中的电离
1.电离:电解质溶于水或受热熔化时,形成自由移动的离子的过程。
2.电离方程式
(1)定义:电离方程式是用化学式和离子符号表示电解质电离过程的式子。
(2)举例
①硫酸(H2SO4):H2SO4===2H++SOeq \\al(2-,4)。
②氢氧化钠(NaOH):NaOH===Na++OH-。
③硫酸钠(Na2SO4):Na2SO4===2Na++SOeq \\al(2-,4)。
3.认识酸、碱、盐的本质
(1)酸:电解质电离出的阳离子全部是H+,如H2SO4、HNO3等。
(2)碱:电解质电离出的阴离子全部是OH-,如NaOH、Ba(OH)2等。
(3)盐:电解质电离出的阴离子是酸根离子;阳离子是金属离子或铵根离子,如Na2SO4、NH4NO3等。
1.判断正误(正确的打“√”,错误的打“×”)
(1)在水中能导电的化合物一定是电解质( )
(2)氯化氢是电解质,但液态氯化氢不导电( )
(3)溶于水能电离产生H+的电解质一定属于酸 ( )
(4)氯化钠晶体不能导电,是由于其中不含离子( )
[答案] (1)× (2)√ (3)× (4)×
2.下列关于电解质的叙述中错误的是( )
A.电解质是自身可电离出离子的化合物
B.电解质、非电解质都是化合物,不可能是单质
C.在水中能导电的化合物一定是电解质
D.纯水的导电性很差,但水也是电解质
C [在水溶液中或熔融状态下能导电的化合物叫电解质(能电离产生离子),在水溶液中和熔融状态下均不导电的化合物叫非电解质(不能电离产生离子),A、B正确;在水中导电的化合物不一定是电解质,如二氧化碳,C错误;水是电解质,D正确。]
3.现有下列物质:
①氢氧化钠固体 ②铜丝 ③氯化氢气体 ④稀硫酸 ⑤二氧化碳气体 ⑥氨水 ⑦碳酸钠粉末 ⑧蔗糖晶体 ⑨熔融氯化钠 ⑩胆矾晶体
请用序号填空:
(1)上述状态下可导电的物质是________。
(2)属于电解质的是________。
(3)属于非电解质的是________。
(4)上述状态下的电解质不能导电的是________。
[解析] 化合物酸(如氯化氢)、碱(如氢氧化钠)、盐(如碳酸钠、胆矾)都是电解质;化合物非金属氧化物(如二氧化碳)、有机物(如蔗糖)都是非电解质;单质(如铜)和混合物(如氨水)既不是电解质,也不是非电解质。能导电的物质有金属(如铜)、熔融电解质(如熔融氯化钠)、电解质溶液(如稀硫酸、氨水)。
[答案] (1)②④⑥⑨ (2)①③⑦⑨⑩ (3)⑤⑧ (4)①③⑦⑩
1.电离方程式的书写
(1)强酸、强碱、大部分盐的电离方程式在书写时用“===”连接,如H2SO4===2H++SOeq \\al(2-,4)、NaOH===Na++OH-、NaCl===Na++Cl-。
(2)酸式盐的电离方程式
①强酸的酸式盐在水溶液中完全电离,如NaHSO4===Na++H++SOeq \\al(2-,4)。熔融状态下NaHSO4的电离方程式为NaHSO4===Na++HSOeq \\al(-,4)。
②弱酸的酸式盐在溶液中电离产生酸式酸根离子和阳离子,如NaHCO3===Na++HCOeq \\al(-,3)。熔融状态下的电离与水溶液中的电离方程式相同。
2.电离方程式书写注意事项
(1)符合客观事实,不能随意书写离子符号,要注意正确标注离子所带的电荷种类及其数目。
(2)质量守恒,即电离方程式左右两侧元素的种类、原子或原子团的个数相等。
(3)电荷守恒,即电离方程式右侧的正负电荷数相等,溶液呈电中性。
3.影响电解质溶液导电能力强弱的因素
电解质溶液的导电能力与溶液中离子浓度及离子所带电荷多少有关,离子浓度越大,离子所带电荷越多,溶液导电能力越强。
【典例】 导电性实验可以作为研究电解质电离本质及反应机理的有效方法。
(1)在如下图所示的装置里,若灯泡亮,广口瓶内的物质A可以是________(填序号)。
①干燥的氯化钠晶体 ②干燥的氢氧化钠晶体 ③蔗糖晶体 ④酒精 ⑤氯化钠溶液 ⑥氢氧化钠溶液 ⑦稀盐酸 ⑧硫酸铜溶液
(2)在电解质溶液的导电性装置(如下图所示)中,若向某一电解质溶液中逐滴加入另一溶液时,则灯泡由亮变暗,至熄灭后又逐渐变亮的是________(填字母)。
A.盐酸中逐滴加入食盐溶液
B.硫酸中逐滴加入氢氧化钠溶液
C.石灰乳中滴加稀盐酸
D.硫酸中逐滴加入氢氧化钡溶液
【思路点拨】
[解析] (1)氯化钠、氢氧化钠晶体虽由离子构成,但离子不能自由移动,所以不导电。两者溶于水后,在水分子的作用下,离解成自由移动的阴、阳离子(实为水合离子),所以二者的水溶液能导电;蔗糖由分子构成,不能导电,其水溶液也不导电。
(2)溶液能否导电,取决于溶液中是否有自由移动的离子存在;导电性强弱则由离子浓度大小及所带电荷数多少等因素决定。D选项中,发生反应H2SO4+Ba(OH)2===BaSO4↓+2H2O,溶液中离子浓度减小,恰好完全反应时,溶液中几乎没有离子,继续滴加Ba(OH)2溶液,Ba(OH)2过量,溶液中Ba2+、OH-数目增多;石灰乳中Ca(OH)2溶解度小,加稀盐酸生成了可溶性的CaCl2,导电能力增强。
[答案] (1)⑤⑥⑦⑧ (2)D
(1) 比较溶液导电性时要先分类,再比较。分清电解质和非电解质,前者溶于水或熔融状态下能导电,后者则不导电。
(2)涉及反应前后溶液导电性的分析,应首先明确反应前溶液中离子浓度,再分析发生的化学反应,看反应后溶液中的离子浓度,最后做出判断。
1.某化学兴趣小组进行化学实验,按照图Ⅰ连接好线路发现灯泡不亮,按照图Ⅱ连接好线路发现灯泡亮,由此得出的结论正确的是( )
图Ⅰ 图Ⅱ
A.MgCl2是非电解质
B.MgCl2溶液是电解质
C.MgCl2在水溶液中电离出了可以自由移动的离子
D.MgCl2只有在溶液中才能导电
C [MgCl2固体中离子不能自由移动,不导电;MgCl2在溶液中电离生成能够自由移动的Mg2+和Cl-,MgCl2溶液导电;MgCl2在熔融状态也能导电,D错。]
2.在如图所示的串联装置中,发现灯泡不亮,但若向其中一个烧杯中加水,则灯泡会亮起来:
A B C
则:(1)加水的烧杯为________(填序号)。
(2)向烧杯C中加适量A中的溶液后,溶液的导电性会________(填“增强”“减弱”或“不变”)。
(3)写出C烧杯中电解质的电离方程式: __________________
_____________________________________________________。
[解析] 三个烧杯中只有B中没有发生电解质电离,没有自由移动的离子,当加水时,KCl发生电离而导电;稀硫酸溶液与Ba(OH)2溶液混合后,溶液中的SOeq \\al(2-,4)与Ba2+生成BaSO4沉淀,H+与OH-生成H2O,从而使溶液中离子浓度减小,导电能力减弱。
[答案] (1)B (2)减弱 (3)Ba(OH)2===Ba2++2OH-
1.下列说法正确的是( )
A.液态氯化氢不导电,所以氯化氢是非电解质
B.二氧化碳的水溶液导电,所以二氧化碳是电解质
C.铜丝、石墨都能导电,所以它们都是电解质
D.蔗糖在水溶液中和熔融状态时都不导电,所以蔗糖是非电解质
D [酸(如氯化氢等)、碱、盐都是电解质,非金属氧化物(如二氧化碳等)、有机物(如蔗糖等)都是非电解质,单质既不是电解质也不是非电解质。]
2.现有一种固体化合物X不导电,但熔融状态或溶于水导电,下列关于X的说法中,正确的是( )
A.X一定为电解质 B.X可能为非电解质
C.X只能是盐类 D.X只能是碱类
A [因为该化合物在熔融状态或溶于水能导电,该化合物一定是电解质,可以是盐类(如氯化钠),也可以是碱类(如氢氧化钠)等。]
3.下列电离方程式正确的是( )
A.NaHSO4===Na++H++SOeq \\al(2-,4)
B.Cu(NO3)2===Cu2++2(NO3)2-
C.Ca(OH)2===Ca2++OH2-
D.K2SO4===K++SOeq \\al(2-,4)
A [电离方程式要符合质量守恒、电荷守恒。A中NaHSO4为强酸酸式盐,NaHSO4电离生成Na+、H+和SOeq \\al(2-,4),B中应为Cu(NO3)2===Cu2++2NOeq \\al(-,3),C中应为Ca(OH)2===Ca2++2OH-,D中应为K2SO4===2K++SOeq \\al(2-,4),故A正确。]
4.下列说法正确的是( )
A.电离时能生成H+的化合物是酸
B.水溶液显碱性的物质是碱
C.碱类电解质电离时产生的阴离子全部是OH-
D.能与碱发生反应生成水的化合物是酸
C [能与碱发生反应生成水的化合物可能是酸,也可能是酸性氧化物。]
5.现有中学化学中常见的八种物质:
①固体氢氧化钡 ②石墨碳棒 ③纯醋酸 ④液态氯化氢 ⑤硫酸氢钾固体 ⑥熔融氯化钠 ⑦蔗糖 ⑧碳酸钠粉末
请用序号填空:
(1)上述状态下可导电的是________,属于非电解质的是________。
(2)属于酸的是________,属于碱的是________,属于盐的是________。
(3)写出①④⑤⑧在水溶液中的电离方程式:
①__________________________________________________;
④_________________________________________________;
⑤__________________________________________________;
⑧__________________________________________________。
[答案] (1)②⑥ ⑦ (2)③④ ① ⑤⑥⑧
(3)①Ba(OH)2===Ba2++2OH- ④HCl=== H++Cl- ⑤KHSO4===K++H++SOeq \\al(2-,4) ⑧Na2CO3===2Na++COeq \\al(2-,3)
装置
烧杯中药品
实验现象
烧杯中药品
实验现象
NaCl固体
电流表指
针不偏转
NaCl溶液
电流表指
针偏转
KNO3
固体
电流表指
针不偏转
KNO3溶液
电流表指
针偏转
蒸馏水
电流表指针不偏转
电解质电离方程式的书写及导电影响因素
高中化学人教版 (2019)必修 第一册第一节 原子结构与元素周期表第1课时学案设计: 这是一份高中化学人教版 (2019)必修 第一册第一节 原子结构与元素周期表第1课时学案设计,共8页。学案主要包含了原子的构成,核外电子排布等内容,欢迎下载使用。
人教版 (2019)必修 第一册第三章 铁 金属材料第二节 金属材料第1课时学案设计: 这是一份人教版 (2019)必修 第一册第三章 铁 金属材料第二节 金属材料第1课时学案设计,共7页。学案主要包含了合金,铁合金,铝和铝合金,新型合金等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第二节 氯及其化合物第1课时导学案及答案: 这是一份高中化学人教版 (2019)必修 第一册第二章 海水中的重要元素——钠和氯第二节 氯及其化合物第1课时导学案及答案,共9页。学案主要包含了氯气的物理性质,氯气的化学性质等内容,欢迎下载使用。













