


九年级上册课题4 化学式与化合价教课课件ppt
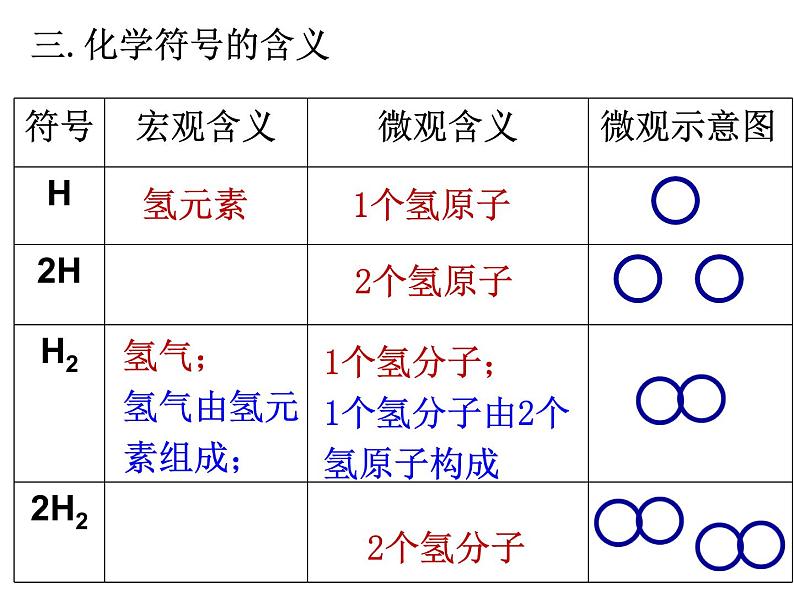
展开H、2H、2H2、O2-
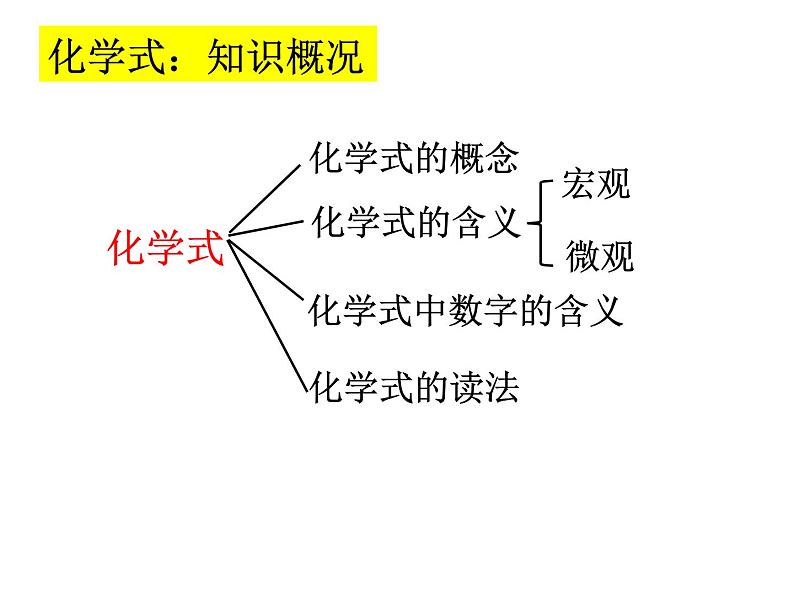
用元素符号和数字的组合表示物质组成的式子。
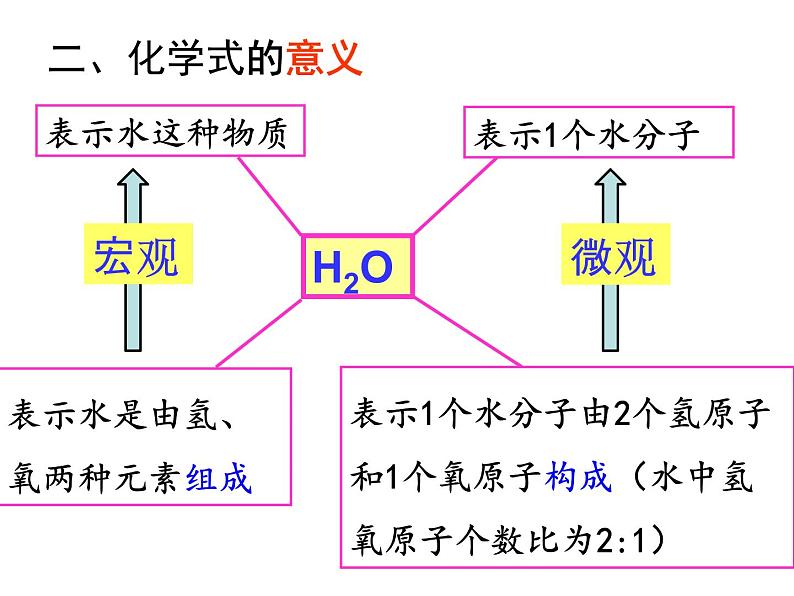
表示水是由氢、氧两种元素组成
表示1个水分子由2个氢原子和1个氧原子构成(水中氢氧原子个数比为2:1)
1个氢分子;1个氢分子由2个氢原子构成
氢气;氢气由氢元素组成;
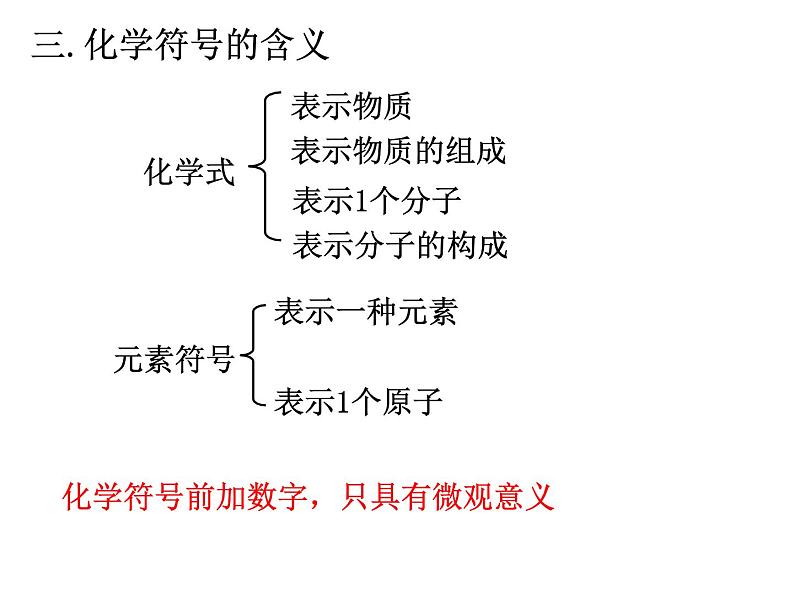
表示物质 表示物质的组成
表示1个分子 表示分子的构成
化学符号前加数字,只具有微观意义
1.请你说说“CO2”的含义
① 二氧化碳② 二氧化碳是由碳元素和氧元素组成③ 1个二氧化碳分子④ 1个二氧化碳分子是由1个碳原子和2个氧原子构成
2. 请你说说“2CO2”的含义
1个氢分子中含有2个氢原子
1个二氧化碳分子中含有2个氧原子
1个氧离子带2个单位负电荷
1个分子中所含原子的个数
1个钙离子带2个单位正电荷
直接读元素名称,如Fe(铁),Al(铝)
气体在元素符号名称后加“气”字,如O2(氧气),Cl2(氯气)
两种元素组成的化合物,从右往左读作某化某(有时读出原子个数)如NaCl(氯化钠),SO2(二氧化硫)
有原子团的,通常读作某酸某,如Na2CO3(碳酸钠)
物质 物质的组成
气体在元素符号名称后加“气”字,如O2(氧气)
两种元素组成的化合物,从右往左读作某化某(有时读出原子个数)如NaCl(氯化钠),SO2(二氧化硫)
课题4 化学式和化合价(第2课时)
化合物有固定的组成,即形成化合物的元素有固定的原子个数比。
十九世纪中叶,科学家提出了化合价的概念,规定氢原子化合价为+1价。
二十世纪初期,科学家提出核外电子排布理论,将化合价的数目与原子结构建立了联系。
NaCl中, 钠元素显+1价 氯元素显-1价
思考: 结合例子,请你说说化合价与原子结构的关系?
在化学反应中,通常用“化合价”来反映原子得失电子的情况,原子的最外层电子数与元素化合价有密切关系。
1、原子结构与元素化合价的关系
请推测下列元素可能的化合价?
O F Mg
请推测镁元素和氯元素形成的化合物中,两种粒子的个数比?
Mg Cl
化学上用“化合价”来表示原子之间相互化合的数目。
请你观察课本P85表4-2,找出常见元素的化合价规律。
某些元素有不同的化合价
氢元素+1价氧元素-2价
化合物中,正负化合价的代数和为零。 单质中,元素化合价为零。
你知道H2中氢元素的化合价是怎样的吗?
有一些物质,如CaCO3、Ca(OH)2等,它们中的一些带电的原子团,如OH-和CO32-常作为一个整体参加反应,这样的“原子团” 又叫做“根”,根也有化合价,如OH-为-1价,CO32-为-2价。
3.化合价的表示方法:
O Na SO42-
标在元素符号或原子团的正上方(“1”不能省略)
☺注意与离子符号的区别
O Na
O2- Na+
练习:写出下列数字2的意义
在氧化镁中,氧元素显-2价
在氧化镁中,镁元素显+2价
Na K Ag H
铜 镁 锌 钡 钙
Cu Mg Zn Ba Ca
氢氧根:硝酸根: 碳酸根: 硫酸根: 铵 根:
一、化合价发展史二、化合价
1.用“化合价”来表示原子之间相互化合的数目。
①有正价也有负价②化合物里,氢通常显+1价,氧通常显-2价。③金属元素通常显正价,非金属元素通常显负价。④化合物里,正负化合价的代数和为零。⑤单质里,元素的化合价为零。⑥某些元素有不同的化合价。如:FeO(氧化亚铁)Fe2O3(氧化铁)
1.化合物都有固定的组成,即固定的原子个数比
化学上用“化合价”来反映原子得、失电子的情况,原子的最外层电子数与化合价有密切的关系。例如:
镁元素的化合价是+2价
在氧化镁中氧元素的化合价为-2价
3.化合价的写法和意义
在氧化镁中镁元素的化合价为+2价
正上方的数字: (在什么中),某元素的化合价为多少价
标在元素符号的正上方,正负号在前,数字在后
2.在化合物里,正负化合价的代数和为零
元素的化合价有正、有负化合物中,H为+1价,O为-2价,Cl为-1价
如何知道不同元素以什么样的原子个数比结合呢?
比较:离子符号和化合价
离子:数字在前,正负号在后;写在右上角化合价:正负号在前,数字在后;写在正上方
钙元素的化合价是+2价
每个钙离子带2个单位正电荷
①金属元素与非金属元素化合时,金属元素显正价,非金属元素显负价②一些元素在不同的物质中可显不同的化合价③元素的化合价是元素的原子在形成化合物时表现出来的一种性质,因此,在单质里,元素的化合价为0
第3课 原子团、根据化学式求化合价
Na K Ag H
Cu Mg Zn Ba Ca
+1 +1 +1 +1
+2 +2 +2 +2 +2
3.金属元素与非金属元素化合时,金属元素显正价,非金属元素显负价;一些元素在不同的物质中可显不同的化合价;在单质里,元素的化合价为0 。
1.化合价标在元素符号的正上方 正负号在前,数字在后
Ca(OH)2 NaNO3 CaCO3 BaSO4 NH4Cl
作为一个整体参加反应,又叫做根
氢氧根:OH- 硝酸根:NO3-碳酸根:CO32- 硫酸根:SO42- 铵 根:NH4+
7.根据化学式求化合价
原则:化合物中元素正负化合价的代数和为零
在NaCl中,氯元素为-1价,请求出钠元素的化合价
在Na2S中,钠元素为+1价,请求出钠元素的化合价
(+1)×2 +X=0
练一练:算出下列划横线元素的化合价
(+1)×2 +X=0
X×2 +(-2)×3 =0
(+1)+X +(-2)×3 =0
作业本 做课本P89.3.4
练习:说出下列数字3的含义
每个什么离子带多少个单位的什么电荷
每个什么分子有多少个什么原子
(在什么中),某元素的化合价为多少价
①②前面: 右上角:③正上方: 右下角:
三个铝原子 三个铝离子 每个铝离子带三个单位正电荷 在氧化铝中,铝元素的化合价是+3价 一个氧化铝分子中有三个氧原子
1.化合价的定义:化合物都有固定的组成, 即形成化合物的元素有固定的原子个数比
2.在化合物里,正负化合价的代数和为 .
元素的化合价 ;化合物中,H为 价,O为 价,Cl为 价
3.化合价标在元素符号的正上方,
常见元素化合价口诀P85
亚铁 铜 镁 锌 钡 钙
Fe Cu Mg Zn Ba Ca
6.根据化合价求化学式P86
课本P89,5,6
化合物中元素化合价的代数和为零
检查:+4+(-2)×2=0
例 已知某种碳的氧化物中磷为+4,氧为-2,写出这种碳的氧化物的化学式
6.根据化合价求化学式———含原子团
例 已知钙元素的化合价为+2价,碳酸根的化合价为-2,写出其化学式
思考:已知钙元素的化合价为+2价,氢氧根的化合价为-1,写出其化学式
氧化物读作:几氧化几某
两种元素组成读作:某化某
①Na和Cl②Ba和NO3③Ca和CO3 ④Na和SO4 ⑤Ca和OH⑥NH4和Cl⑦NH4和SO4
NaClBa(NO3)2CaCO3 Na2SO4 Ca(OH)2NH4Cl(NH4)2SO4
练习1:写出下列元素组成的化学式和名称
作业本 书P86-87 练一练
练习2:写出下列物质的化学式
①氧化钾②氧化钙③氧化铁
氢氧化钾氢氧化钙氢氧化铁
(1)指出下列各物质中氯元素的化合价: KCl、Ca(ClO)2、KClO3、HClO4、Cl2
-1 +1 +5 +7 0
(2)确定下列物质中原子团的化合价: Mg(NO3)2、BaSO4、Ca(OH)2、NH4NO3
(3)某化学式为Hn+1RO2n+1,则R的化合价为
- 1 - 2 - 1 -1
练习3:根据化学式求化合价
化学式中各原子的相对原子质量的总和:Mr
已知:C:12 O:16 N:14 H:1 Ca:40
练习:计算下列相对分子质量 ①CO2 ②Ca(OH)2 ③NH4NO3 ④(NH4)2CO3
第6课时 有关相对分子质量的计算
2.计算元素质量比、原子个数比
计算H2O各元素质量比和原子个数比
= (1×2) :16
练习:计算下列各元素质量比和原子个数比 ①CO2 ②Ca(OH)2 ③NH4NO3 ④(NH4)2CO3
3.计算元素的质量分数
例题:求出H2O中氢元素的质量分数
练习:计算下列划线元素的质量分数 ①CO2 ②Ca(OH)2 ③NH4NO3 ④(NH4)2CO3
(1)N(NO2)3的相对分子质量
(2)N(NO2)3中,元素质量比N:O=
(3)N(NO2)3中,N%=
=14+(14+16×2)×3
=(14×4):(16×6)
(6)维生素C,C6H8O6
①C6H8O6的相对分子质量
=12×6+8+16×6
②C6H8O6中,元素质量比C:H:O=
=(12×6):8:(16×6)
③C6H8O6中,氢元素质量分数
在C6H8O6中,H%=
已知尿素的化学式是CO(NH2)2,完成下列计算:
在CO(NH2)2 中,N%=
(1)尿素的相对分子质量
(2)碳元素和氮元素的质量比
CO(NH2)2的相对分子质量
=12+16+(14+2)×2
CO(NH2)2中,元素质量比C:N
(3)氮元素的质量分数
(4)现有一包75kg尿素,内含氮元素的质量是多少?
公式:X元素质量=化合物的质量×X%
(5)现有一包尿素,内含氮元素的质量是70kg,请问这包尿素的质量是多少?
“瘦肉精”(化学式为C12H19Cl3N2O) (1)“瘦肉精” 由___种元素组成,每个“瘦肉精”分子中共有___个原子。(2)“瘦肉精”其分子中氢、氧原子个数比为________; (3) “瘦肉精”中碳、氮元素的质量比为____;(4) “瘦肉精”的相对分子质量为________; (5) “瘦肉精”中____元素的质量分数最大(填名称);(6) 313.5g “瘦肉精”中含有氯元素___克。
练习:求出 CO(NH2)2 和NH4NO3的氮元素质量分数
在NH4NO3 中N%=
相对原子质量×原子个数
1.化学式H2O的意义
(2)表示水是由氢、氧两种元素组成
(4)表示一个水分子由2个氢原子和1个氧原子构成
2.数字的意义①右上角的数字: 每个什么离子带多少个单位的什么电荷②前面的数字:多少个粒子③右下角的数字: 每个什么分子有多少个什么原子④正上方的数字: (在化合物中),某元素的化合价为多少价
3. 化学式的写法和读法
:元素符号右下角加数字
(3)金属在左边,非金属在右边
注意:一般“气”字头的单质都读作“某气”
含NO3读作硝酸某含CO3读作碳酸某含SO4读作硫酸某含OH读作氢氧化某NH4读作铵
1.元素的化合价有正价和负价;其中,在化合物中,H为+1价,O为-2价,Cl为-1价
3.化合价:写在正上方,正负号在前,数字在后
4.原子团:作为一个整体参加反应,又叫做根
5.根据化合价写化学式: 正左负右→约分交叉→检查
2.元素质量比、原子个数比
硫酸铵的质量=132kg
在CO(NH2)2中:
在(NH4)2SO4中:
练习:现有1000kg的NH4NO3,含有氮元素多少千克
化合物的质量×某元素的质量分数
新闻:9月11日晚间,新华社发布通稿:中国卫生部指出,近期甘肃等地报告多例婴幼儿泌尿系统结石病例,调查发现患儿多有食用三鹿牌婴幼儿配方奶粉的历史,经相关部门调查,高度怀疑石家庄三鹿集团股份有限公司生产的三鹿牌婴幼儿配方奶粉受到污染。至今全国各地已经有多名婴儿因喂养受污染的奶粉而导致结石。题目:生鲜牛奶的蛋白质含氮率约16%,一般都能达到国家标准,除非往原奶中兑水。要提防有人拿水卖出奶的价钱,就有必要在收购生鲜牛奶时检测蛋白质的氮含量。有一个不法商人在牛奶中兑水了,为了通过检测,他需要在兑水牛奶中加入了一种物质以增加氮的含量,
已知尿素CO(NH2)2和三聚氰胺C3N3(NH2)3都能增加氮的含量(1)请算出相对分子质量和N% (2)请说明这个不法商人的选择。已知:尿素溶解在水中会发出刺鼻的氨味 三聚氰胺溶于水后不会散发出任何气味解(1)在尿素中: 相对分子质量=12×1+16×1+14×2+1×4=60 N%≈46.7% 在三聚氰胺中: 相对分子质量=12×3+14×6+1×6=126 N%≈66.7%(2)该不法商人会选择三聚氰胺,因为三聚氰胺的含氮量比尿素高,而且溶于水后不会散发出任何气味,不容易被察觉;尿素溶解在水中会发出刺鼻的氨味容易被察觉
(1)定义:化学式中各原子的相对原子质量(Ar)的总和, 用符号Mr表示,一般不写单位
(2)根据第4点意义:如一个H2O分子是由两个H原子和一个O原子构成的
H2O的相对分子质量=1×2+16×1 =18
(已知:相对原子质量 H:1 O:16 S:32 )
练习:课本P87第7题(1)(2)
O2的相对分子质量=16×2=32
(3)含有原子团的化学式的相对分子质量的计算
例题:计算 (NH4)2S的相对分子质量
练习:1、课本P87.7(3)
已知: N:14 H:1 Cl:35.5 S:32 Ca:40
练习:计算NH4NO3的相对分子质量
NH4NO3的相对分子质量=14×2+1×4+16×3 =80
练习:课本P87第8题
2.计算物质组成元素的质量比
例1求CO2中碳元素和氧元素的质量比(已知C:13 ,O:16)
解:质量比C:O=12:(16×2)=3:8
例2求硫酸铵(NH4)2SO4中各元素的质量比。(N:14 H:1 S:32 O:16)
解 :质量比N:H:S:O=(14×2):(1×8) :(32×1):(16×4)=28:8:32:64=7:2:8:16
现有80g NH4NO3,经称量得到其中的氮元素的质量为28g,请计算氮元素的质量分数。
3.计算物质中某元素的质量分数(宏观)
3.计算物质中某元素的质量分数
某元素的质量分数= (X%)
例:⑴计算NH4NO3中氮元素的质量分数 ⑵计算80g NH4NO3中含氮元素的质量
⑴NH4NO3的相对分子质量 =14×2+1×4+16×3=80
⑵氮元素的质量=80g×35%=28g
练习:课本P87第9,10题
(已知C:12 O:16 N:14 H:1)
请算出H2SiO3中,硅元素的质量分数
请计算阿奇霉素片中碳元素的质量分素
相对分子质量=12×38+1 ×72+14 ×2+16×12 =748
求相对分子质量: H2 CO2 KMnO4 HCl Ca(OH)2 CuO
39+55+16×4=158
1+35.5=36.5
40+(16+1)×2=74
求相对分子质量总和:
2H2 2H2O 3O2 2KClO3 10NaCl
2×(1×2+16)=36
3×(16×2)=96
2×(39+35.5+16×3)=245
10×(23+35.5)=585
求各元素的质量比:H2O CO2 CH4 H2SO4 Cu(OH)2
在H2O中,H:O=1×2:16 =1:8
在CO2中, C:H=12:16×2=3:8
在CH4中, C:H=12:1×4=3:1
在H2SO4中, H:S:O=1×2:32:16×4=1:16:32
在Cu(OH)2中, Cu:O:H=64:16×2:1×2=32:16:1
硫酸铵的化学式为(NH4)2SO4,求: (NH4)2SO4的相对分子质量; (2) (NH4)2SO4中各元素的质量比; (3) (NH4)2SO4中氮元素的质量分数。(4) 264kg (NH4)2SO4中含氮元素多少千克?(5) 多少kg(NH4)2SO4中含氮元素质量84kg?
练习3:已知元素M的氧化物化学式为M2On,则M的氯化物的化学式为____。
练习2:判断下列化学式是否正确,错则更正。 MgO2、NaO、Ba2O2、K(OH)2、 NaCO3、 CaCl、 AgCl2
1.氧化钾 氧化钡 氧化铝 氧化亚铁 氧化铁 氧化铵
2.氯化钾 氯化钡 氯化铝 氯化亚铁 氯化铁 氯化铵
7.氢氧化钾 氢氧化钙 氢氧化钡 氢氧化亚铁 氢氧化铁
5.硫酸钾 硫酸钡 硫酸铝 硫酸亚铁 硫酸铁 硫酸铵
4.碳酸钾 碳酸钡 碳酸铝 碳酸亚铁 碳酸铁 碳酸铵
K2CO3 BaCO3 Al2(CO3)3 FeCO3 Fe2(CO3)3 (NH4)2CO3
3.硝酸钾 硝酸钡 硝酸铝 硝酸亚铁 硝酸铁 硝酸铵
KNO3 Ba(NO3)2 Al(NO3)3 Fe(NO3)2 Fe(NO3)3 NH4NO3
6.硫化钾 硫化钡 硫化铝 硫化亚铁 硫化铁 硫化铵
(1)KMnO4表示:
①高锰酸钾②高锰酸钾是由钾元素、锰元素和氧元素组成③一个高锰酸钾分子④一个高锰酸钾分子是由一个钾原子、一个锰原子和四个氧原子构成
①二氧化碳②二氧化碳是由碳元素和氧元素组成③一个二氧化碳分子④一个二氧化碳分子是由一个碳原子和两个氧原子构成
化学九年级上册课题4 化学式与化合价授课ppt课件: 这是一份化学九年级上册课题4 化学式与化合价授课ppt课件,共60页。PPT课件主要包含了宏观意义,微观意义,动动脑,知识巩固,7Fe,化合价的运用,化合价的应用,相对原子质量的总和等内容,欢迎下载使用。
初中化学课题4 化学式与化合价说课ppt课件: 这是一份初中化学课题4 化学式与化合价说课ppt课件,共60页。PPT课件主要包含了其他意义,一个偏二甲肼分子,AlCl3,SiO2,N2O3,KClO3,二氧化硫,四氧化三铁,FeCl3,Al2SO43等内容,欢迎下载使用。
化学九年级上册第四单元 自然界的水课题4 化学式与化合价课堂教学课件ppt: 这是一份化学九年级上册第四单元 自然界的水课题4 化学式与化合价课堂教学课件ppt,共19页。PPT课件主要包含了教材分析,教材的地位和作用,教材内容的地位和作用,利用化合价推求化学式,教学重点,教学难点,学情分析,教学方法,教法学法,敢思会思等内容,欢迎下载使用。













