





所属成套资源:2026届高三化学二轮复习 课件 微主题和破难点
微主题1 物质的结构、性质 元素周期律 课件 2026届高三化学二轮复习
展开 这是一份微主题1 物质的结构、性质 元素周期律 课件 2026届高三化学二轮复习,共19页。PPT课件主要包含了基础回归,3d5,XY或YX,HCl,sp2,SO3SO2,体系建构,名卷优选,s22s1,s24p2等内容,欢迎下载使用。
1 分别写出基态Mn、Cu、Zn2+的简化电子排布式:_______________________________;写出基态As、Fe3+的价电子排布式:______________;写出基态C的轨道表示式:_________________;写出基态Cu的价电子轨道表示式:_____________________。2 基态S原子的电子运动状态有________种,电子空间运动状态有______种,有______种能量不同的电子。【解析】 题中依次考查的是电子数、轨道数、能级数。
[Ar]3d54s2、[Ar]3d104s1、[Ar]3d10
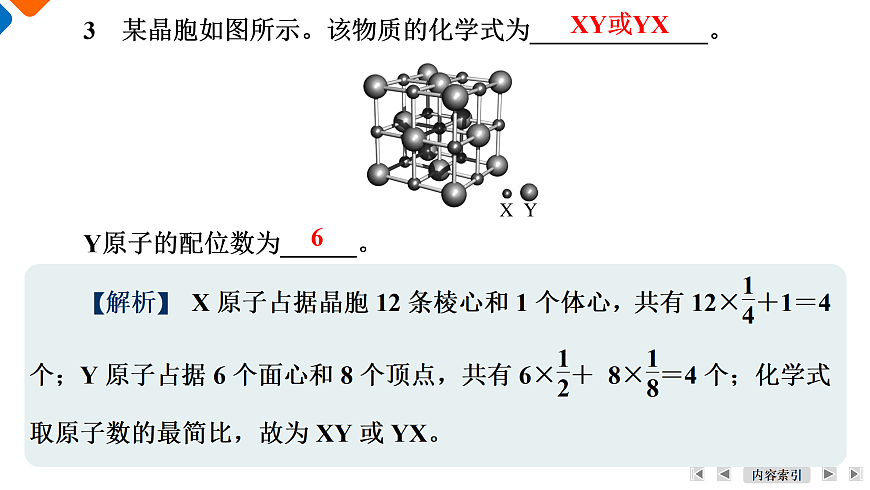
3 某晶胞如图所示。该物质的化学式为______________。Y原子的配位数为______。
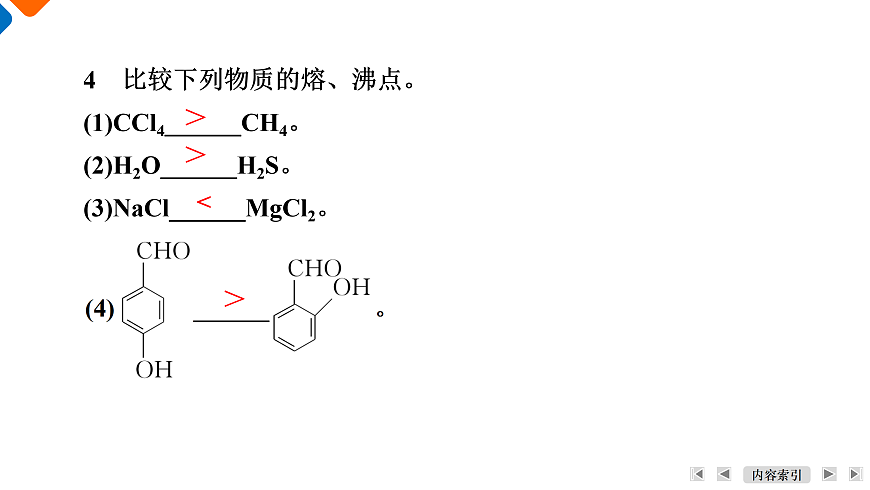
4 比较下列物质的熔、沸点。(1)CCl4______CH4。(2)H2O______H2S。(3)NaCl______MgCl2。
【解析】 (1)(2)(4)中的物质为分子晶体。(1) CCl4的相对分子质量大,范德华力强,熔、沸点高。(2) 水形成分子间氢键,熔、沸点高。(3) NaCl、MgCl2为离子晶体,镁离子半径小,所带电荷多,晶格能大,熔、沸点高。(4) 前者可形成分子间氢键,后者形成分子内氢键,故后者熔、沸点低。
5 根据电负性判断ICl水解产物:__________________。6 SO2与SO3中硫原子杂化方式分别为______________;VSEPR模型分别为__________________________;键角大小为_____________。
平面三角形、平面三角形
【解析】 电负性Cl>I,ICl中Cl带负电性,I带正电性;水中氢原子带正电性,氧带负电性,故相异电荷吸引结合得到HCl和HIO。
【解析】 SO2与SO3的中心原子S均为sp2杂化,VSEPR模型均为平面三角形。SO2中硫原子有一个孤电子对,SO3中硫原子电子全部参与成键,孤电子对斥力大于成键电子对,故SO3键角大于SO2。
考向1 原子结构与元素性质 元素周期律(2)[2022江苏卷改编]基态锗原子(32Ge)的价电子排布式为_________。(3)[2021江苏第二次适应性考试]基态Mn2+的电子排布式为_______________________________。
1s22s22p63s23p63d5或[Ar]3d5
2 (1)[2025江苏卷]电负性:χ(F)______χ(Cl);离子半径:r(F-)___r(Na+)。(2)[2023江苏卷改编]C、Si、Ge位于元素周期表中ⅣA族。原子半径:_____________;第一电离能:____________。(3)[2023江苏卷]电负性:χ(F) ______χ(O)。
3 [2021江苏卷]前4周期主族元素X、Y、Z、W的原子序数依次增大,X是空气中含量最多的元素,Y的周期序数与族序数相等,基态时Z原子3p原子轨道上有5个电子,W与Z处于同一主族。下列说法正确的是( )A. 原子半径:r(X)I1(Al)。(4) 同周期主族元素从左到右,电负性依次增大,同主族元素从上到下,电负性依次变小,则电负性χ(P)>χ(Mg)>χ(Ca);同周期主族元素从左到右,第一电离能总体呈增大趋势,则第一电离能I1(P)>I1(Mg)>I1(Na)。
考向2 分子结构与性质2 关于共价键类型和数目判断,分子空间结构判断,分子性质对溶解性、熔沸点影响的考查。
(5)[2025南京二模]NF3的空间结构为____________。
(9)[2025南通如皋适应性二]NH3中所含键角________(填“大于”“小于”或“等于”)H2O中所含键角。(11)[2024南京调研]室温下,A在水中的溶解度比B______(填“大”“小”或“无差别”)。
(12)[2025南京、盐城一模]HOCH2CH2NH2(乙醇胺)也能捕集CO2。乙醇胺的沸点高于氨的原因是__________________________________________________________________________________。
乙醇胺分子间形成氢键的能力更强;乙
醇胺相对分子质量比氨大,范德华力更强
3 溶剂极性、超分子对溶质溶解度的影响。(1)[2025南京、盐城一模]向[Cu(NH3)4]SO4溶液中加入乙醇,增大溶剂极性,析出深蓝色晶体。该说法是否正确,并说明理由:_______________________________________________________________________________________________________________________________________。
错误。乙醇的极性小于水,加入乙醇会减小溶剂的极性,而[Cu(NH3)4]SO4是离子化合物,在极性小的溶剂中溶解度小,以晶体形式析出
(2)[2025南京、盐城一模] 已知C难溶于水,而18-冠-6(结构如图所示)可溶于水和甲苯,且分子空腔直径与K+相当。C→D的过程中使用18-冠-6 可提升K3[Fe(CN)6]水溶液氧化C的效率,其原因为______________________________________________________________________________________________。
18-冠-6易与K+相互作用,增大K3[Fe(CN)6]在甲苯中的溶解度,提高氧化C的速率
【解析】 (2) 冠醚常被用作相转移催化剂,冠醚与试剂中正离子络合,使该正离子可溶在有机溶剂中,而与它相对应的负离子因为静电作用也随同进入有机溶剂内,冠醚不与负离子络合,使游离或裸露的负离子反应活性很高,能迅速反应。
4 分子中基团的位阻对物质性质的影响。(1)[2025常州期末]对硝基苯的合成如下:未直接使用“A→D”合成,而使用“A→B→C→D”三步的原因是________________________________________________________________________________________。
保护氨基,防止硝化时被氧化,(同时酰胺基因空间位阻增大,有利于硝基在其对位发生取代)
甲基的体积比氢原子大,空间位阻大,Nu-主要与不连甲基的碳原子作用
考向3 晶体结构与性质5 关于晶胞中原子数目、配位数及位置判断。(1)[2025苏锡常镇二调]CeO2晶体晶胞如图所示。晶胞中与每个Ce4+距离最近的Ce4+的个数为________。
(2)[2024苏锡常镇二模]净化时生成的CaF2沉淀晶胞结构如图所示。在CaF2晶胞中F-周围距离最近的Ca2+形成的空隙结构为___________。
(3)[2024苏北八市三模]充电时,Li+脱嵌形成Li1-xFePO4(0甲胺(CH3NH2)>三甲胺[(CH3)3N],理论上甲基的推电子效应使得甲胺、二甲胺、三甲胺的碱性依次增强,但实际上三甲胺碱性最弱,显然此时是空间位阻的作用对其碱性的影响大于增多的甲基的推电子效应的影响。它是调控化学反应的“隐形之手”,通过设计分子中基团的大小和位置,可控制反应是否发生、生成何种产物。在药物合成中,利用位阻优化分子结构,能提高目标产物纯度,减少副反应。理解空间位阻,能更精准地预测和设计有机反应。
6 极性分子与非极性分子
(1)H2O2结构中氧原子为sp3杂化,形成如图所示结构。H2O2为________(填“极性”或“非极性”,下同)分子。(2)O3分子中的共价键是________键,结构类似SO2,中心氧原子为sp2杂化,与另外2个氧原子形成V形分子,为________分子。(3)白磷(P4)为正四面体结构,为__________分子。
(4) 甲烷为正四面体结构,为__________分子;CH3Cl为四面体结构,为________分子。
7★ 溶剂的极性(1)溶剂的极性对物质溶解性的影响,可通过“相似相溶”原理来理解。部分物质虽为极性分子,但若含较大非极性基团(如高级醇),在水中溶解性会下降(因非极性部分占比高)。混合极性溶剂与非极性溶剂,可调节整体极性,溶解兼具极性结构与非极性结构的物质(如某些有机物)。
(2)离子化合物的溶解度与溶剂极性的关系,本质上由离子化合物的解离特性和溶剂的极性相互作用决定。①极性溶剂对离子化合物的溶解有促进作用;②非极性溶剂中离子化合物的溶解度极低。典型案例:食盐(NaCl)在水中易溶,而在非极性溶剂(如苯)中几乎不溶,因水的强极性能有效“包围”Na+和Cl-,而苯无法提供足够的相互作用。指出1、2、3分别对应的微粒:______________________。
H2O、Na+、Cl-
例3 (1)氧化浸取辉铜矿(Cu2S)时,控制温度为80 ℃,空气流速一定,加入Fe2(SO4)3与NaCl协同浸取。其他条件相同时,铜浸出率与c(NaCl)的关系如图所示。Cl-破坏硫覆盖层,但c(NaCl)>1.0 ml/L时,铜浸出率下降,原因可能是_____________________________________________________。
溶液中离子浓度增大,溶液极性增强,O2的溶解度降低
(2)[C(NH3)6]Cl3晶体制备。[C(NH3)6]Cl3晶体易溶于热水和稀盐酸中,在冰水、浓盐酸、无水乙醇中溶解度较小。请补充完整实验方案:在通风橱中将制得的[C(NH3)6]Cl2溶液加热至55 ℃左右,边搅拌边加入适量NH4Cl,再加入__________________________________________________________________________________________________________________________________________________,低温烘干,得到[C(NH3)6]Cl3晶体。(实验中须使用:4% H2O2溶液、红色石蕊试纸、冰水、浓盐酸、无水乙醇)
4% H2O2溶液至产生的气体不能使湿润的红色石蕊试纸变蓝,冰水浴冷却,再加入浓盐酸(无水乙醇)至有大量晶体析出,过滤,用无水乙醇洗涤2~3次
核心3 晶体类型和性质 1 常见典型晶体的晶胞结构图及其主要性质
分子间作用力(或范德华力)
2 晶胞中微粒数目的计算方法——均摊法石墨晶胞每一层内碳原子排成六边形,其顶点(1个碳原子)被三个六边形共有,每个六边形占______个碳原子。
3 分子晶体熔、沸点的比较(1)组成和结构相似的分子晶体,分子间作用力越大,物质的熔、沸点越高。具有分子间氢键的分子晶体,熔、沸点反常地高。如H2O、H2S、H2Se、H2Te熔、沸点高低顺序为___________________________;C2H5OH、CH3OCH3熔、沸点高低顺序为___________________________;烃、卤代烃、醇、醛、羧酸等有机物一般随着分子里碳原子数增加,熔、沸点________。
H2O>H2Te>H2Se>H2S
C2H5OH>CH3OCH3
(2)组成和结构不相似的物质(相对分子质量相近),分子极性_____,其熔、沸点就________。如熔、沸点:CO______N2。(3)同分异构体:链烃及其衍生物的同分异构体随着支链________,熔、沸点________。如CH3(CH2)3 CH3(正戊烷)______CH3CH2CH(CH3)2(异戊烷)______(CH3)4C(新戊烷)。
核心4★ 配合物与超分子1 配离子对反应速率的影响已知:沉淀的生成速率越快,颗粒越小,呈凝乳状胶体,不易过滤。在制备超细粉末时,通常以配离子为反应物控制反应速率。(1)通过形成配离子减慢反应速率如AgNO3溶液转化成配离子[Ag(NH3)2]+,降低溶液中Ag+的浓度,且[Ag(NH3)2]+的氧化性弱于Ag+,使生成单质Ag的反应速率减慢。
(2)通过形成配离子加快反应速率如AgCl沉淀转化成配离子[Ag(NH3)2]+,与还原剂N2H4充分接触,使生成单质Ag的反应速率加快,同时避免生成的Ag单质中混有AgCl,Ag的回收率和纯度下降。(3)通过形成配离子影响金属离子得失电子能力如易被氧化的Fe2+与CN-形成[Fe(CN)6]4-后,稳定性增强,更难被氧化;C2+的还原性相对较弱,但[C(NH3)6]2+易被氧化为[C(NH3)6]3+。
2 超分子与相转移相转移是指物质在不同相(如液相-液相、液相-固相、液相-气相等)之间发生的转移过程,常见于化学合成、分离提纯等领域。其核心是解决不同相态中物质难以接触反应或分离的问题。通过加入相转移催化剂,如冠醚,冠醚与试剂中阳离子络合,使该阳离子进入有机溶剂中,通过静电作用将阴离子也带入有机溶剂中,从而可帮助离子型物质从水相转移到有机相,或让有机物质进入水相,使反应物在同一相中接触并反应,从而加速反应进行。
例4 冠醚是由多个二元醇分子之间失水形成的环状化合物,它们能与碱金属离子作用并随着环的大小不同而与不同金属离子作用。由于烯烃难溶于水,故KMnO4水溶液氧化烯烃的效果较差。若在烯烃中溶入某冠醚,与KMnO4发生如图所示的变化后,氧化效果明显提升。加入该冠醚后,烯烃的氧化效果明显提升的原因是______________________________________________________________________________________________________________________________________。
该冠醚可溶于烯烃,冠醚加
增大了反应物的接触面积,提高了氧化效果
【解析】 Al3+和O2-的电子层结构相同,Al的核电荷数比O大,Al对核外电子的吸引能力大,故半径r(Al3+)<r(O2-),A错误;非金属性F>O,F的得电子能力强于O,故电负性χ(O)r(O2-)B. 电负性:χ(O)>χ(F)C. 第一电离能:I1(Al)>I1(Mg)D. 碱性:Ca(OH)2>Mg(OH)2
2 [2025南通、泰州等八市二调]下列说法正确的是( )A. 基态Ge核外电子排布式:[Ar]4s24p2B. H2S中心原子的杂化方式为sp3C. Si3N4是一种高强度耐高温材料,Si3N4为分子晶体D. 1 ml SiO2(晶胞如图)含2 ml σ键
3 [2025泰州中学调研]下列说法正确的是( )A. 如图所示是Cu2S晶胞中S2-位置,则1个晶胞中含有8个Cu+B. 基态Cu+转化为基态Cu原子,得到的电子填充在3d轨道上C. H2S和SO2的中心S原子都采取sp3杂化D. SO2的键角比SO3的键角大
A. 该反应的ΔS>0B. 步骤Ⅰ中CO2带正电荷的C与催化剂中的N之间作用C. 步骤Ⅲ中存在非极性键的断裂和形成D. 反应中每消耗1 ml CO2,转移电子数约为4×6.02×1023
相关课件
这是一份微主题1 物质的结构、性质 元素周期律 课件 2026届高三化学二轮复习,共19页。PPT课件主要包含了基础回归,3d5,XY或YX,HCl,sp2,SO3SO2,体系建构,名卷优选,s22s1,s24p2等内容,欢迎下载使用。
这是一份微主题1 物质的结构、性质 元素周期律 课件 2025届高考化学二轮复习,共60页。PPT课件主要包含了内容索引,基础回归,XY或YX,HCl,sp2,平面三角形,SO3SO2,体系建构,名卷优选,s24p2等内容,欢迎下载使用。
这是一份新高考化学二轮复习导学案课件 微主题3 物质的结构与性质 元素周期律(含解析),共60页。PPT课件主要包含了命题规律,高考回眸,sp2,sp3,Ca2+,Cl参与形成的,CsCl,电解质,s24p4,BDE等内容,欢迎下载使用。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)




