





所属成套资源:2026届高三化学二轮复习 课件 微主题和破难点
微主题4 反应热 电化学 课件 2026届高三化学二轮复习
展开 这是一份微主题4 反应热 电化学 课件 2026届高三化学二轮复习,共19页。PPT课件主要包含了基础回归,反应ΔH0,-1362,分离氯气和氢气,允许Na+迁移获得,NaOH溶液,体系建构,名卷优选,+824,-824等内容,欢迎下载使用。
1 SiHCl3(g)+H2(g)===Si(s)+3HCl(g) ΔH从反应前后总能量变化角度:ΔH=_________________________________________________________;从键能的角度(E表示键能):ΔH=_________________________________________________________。2 CO2(g)+3H2(g)===CH3OH(g)+H2O(g)能在一定条件下自发进行的原因是________________。
Si(s)和HCl(g)的总能量-
SiHCl3(g)和H2(g)的总能量
3E(Si—Cl)+E(Si—H)+E(H—H)-2E(Si—Si) -3E(H—Cl)
3 已知:①2NO2(g)+H2O(l)===HNO3(aq)+HNO2(aq) ΔH1=-116.1 kJ/ml②3HNO2(aq)===HNO3(aq)+2NO(g)+H2O(l) ΔH2=+75.9 kJ/ml反应3NO2(g)+H2O(l)===2HNO3(aq)+NO(g)的ΔH=_____________kJ/ml。
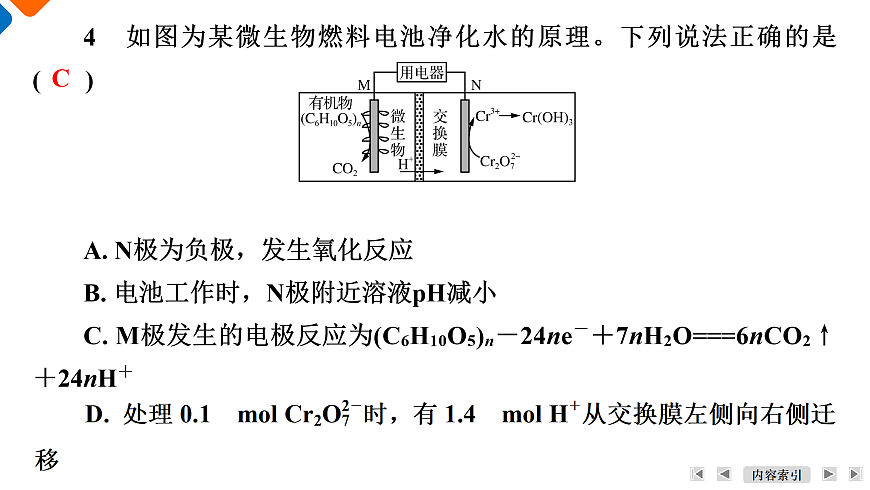
4 如图为某微生物燃料电池净化水的原理。下列说法正确的是( )A. N极为负极,发生氧化反应B. 电池工作时,N极附近溶液pH减小C. M极发生的电极反应为(C6H10O5)n-24ne-+7nH2O===6nCO2↑+24nH+
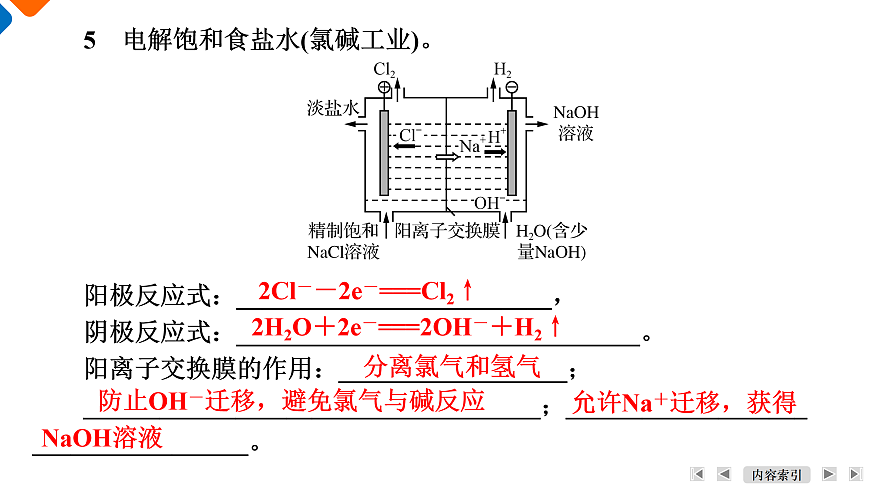
5 电解饱和食盐水(氯碱工业)。阳极反应式:_________________________,阴极反应式:________________________________。阳离子交换膜的作用:__________________;____________________________________;____________________________________。
2Cl--2e-===Cl2↑
2H2O+2e-===2OH-+H2↑
防止OH-迁移,避免氯气与碱反应
考向1 化学反应与能量小综合1 下列说法正确的是______(填序号)。 ①[2023江苏卷改编]金属硫化物(MxSy)催化反应CH4(g)+2H2S(g)===CS2(g)+4H2(g),该反应的ΔS0②[2025苏州期初]肼(N2H4)常温下为液态,燃烧热为642 kJ/ml,肼的燃烧:N2H4(l)+O2(g)===N2(g)+2H2O(g) ΔH=-642 kJ/ml
2 [2024盐城、南京期末] 氨的饱和食盐水捕获CO2是CO2利用的方法之一,反应原理如下:NaCl(aq)+NH3(g)+CO2(g)+H2O(l)===NaHCO3(s)+NH4Cl(aq)。该反应常温下能自发进行的原因是________________。
考向2 ΔH计算及盖斯定律的应用3 (1)[2025南京二模]CH4-H2O(g)重整制氢过程中的主要反应(忽略其他副反应)如下:①CH4(g)+H2O(g)===CO(g)+3H2(g)ΔH=+206 kJ/ml②CO(g)+H2O(g)===CO2(g)+H2(g)ΔH=-41 kJ/ml反应CH4(g)+2H2O(g)===CO2(g)+4H2(g)的ΔH=__________kJ/ml
(2)[2024南京学情调研]“碳达峰、碳中和”是我国社会发展重大战略之一。CH4与CO2经催化重整可制得CO和H2,相关反应如下:主反应:CH4(g)+CO2(g)===2CO(g)+2H2(g) ΔH副反应:Ⅰ. H2(g)+CO2(g)===H2O(g)+CO(g) ΔH1Ⅱ. 2CO(g)===CO2(g)+C(s) ΔH2Ⅲ. CH4(g)===C(s)+2H2(g) ΔH3Ⅳ. CO(g)+H2(g)===C(s)+H2O(g) ΔH4其中,副反应Ⅱ、Ⅲ、Ⅳ形成的积碳易导致催化剂活性降低。主反应的ΔH=____________________________________。
ΔH3-ΔH2或ΔH1+ΔH3-ΔH4
【解析】 (1)根据盖斯定律,①+②可得目标热化学方程式,则ΔH=ΔH1+ΔH2=[+206+(-41)]kJ/ml=+165 kJ/ml。
考向3 原电池的工作原理及应用4 [2025苏州期初]普通锌锰干电池的构造如图所示。关于该电池及其工作原理,下列说法正确的是( )A. 石墨作电池的负极材料C. 电池工作时,MnO2发生氧化反应D. 环境温度过低,不利于电池放电
【解析】 Zn失去电子,作负极,A错误;原电池中,阳离子移向正极,B错误;MnO2作氧化剂,发生还原反应,C错误;温度较低时,反应速率较慢,不利于电池的放电,D正确。
【解析】 用“铁粉还原法”处理废水中的Cr(Ⅵ)时,加入Cu2+后,Fe将Cu2+还原生成Cu,Fe、Cu可构成原电池,随着Cu2+浓度由0升高至15 mg/L,废水中形成很多微小的原电池,加快了Fe2+的生成速率,使Cr(Ⅵ)的去除率增大。
5 [2024南京二模]绿矾(FeSO4·7H2O)还原法和铁粉还原法均可用于处理废水中的Cr(Ⅵ)。为探究铜离子浓度对Cr(Ⅵ)去除率的影响,向1 000 mL某浓度酸性废水中加入2.0 g铁粉,随着Cu2+浓度由0升高至15 mg/L,测得废水中Cr(Ⅵ)的去除率增大,其可能原因为___________________________________________________________________________。
形成Fe-Cu原电池,增大了c(Fe2+),Cr(Ⅵ)去除率增大
考向4 电解池的工作原理及应用6 [2025苏州期末]冶金废水(主要含CaCl2)通过“电解-碳化”制备CaCO3的装置如图所示。下列说法不正确的是( )A. M极上产生黄绿色气体B. 电解前后,N极区溶液的pH基本不变D. 1 ml Ca2+通过阳离子交换膜时,理论上共产生44.8 L的气体
7 (1)[2024南通、泰州等八市三模]钴酸锂电池放电时示意图如图所示。放电时,Li+从LixC6中脱嵌。请写出放电至完全时Li1-xCO2电极的电极反应式:______________________________________________。
Li1-xCO2+xe-+xLi+===LiCO2
当电流强度大于4A时,随着电流强度的增大,Cl-放电生成了更高价态的酸根(或OH-参加放电),溶液中ClO-浓度减小,NO的去除率降低
【解析】 (3)由图可知,NO去除率降低时,ClO-浓度也降低,ClO-浓度降低的原因可能是电流强度过大发生其他副反应,如Cl-、ClO-都可以在阳极放电,氯元素被氧化为更高价态的酸根,OH-也在阳极竞争放电。溶液中ClO-浓度减小,NO去除率降低。
核心1 反应热 热化学方程式1 焓变ΔH的计算
生成物总能量-反应物总能量
反应物总键能-生成物总键能
ΔH1+ΔH2+ΔH3
ΔH1+3ΔH2-ΔH3
说明 1 ml常见物质中含有的σ键的物质的量。晶体硅:Si—Si_________SiO2:Si—O_________石墨:C—C__________金刚石:C—C________白磷(P4 ):P—P__________
2 比较焓变的大小C(s)+O2(g)===CO2(g) ΔH1则ΔH1______ΔH2。S(s)+O2(g)===SO2(g) ΔH3S(g)+O2(g)===SO2(g) ΔH4则ΔH3______ΔH4。2H2(g)+O2(g)===2H2O(g) ΔH52H2(g)+O2(g)===2H2O(l) ΔH6则ΔH5______ΔH6。
3 根据盖斯定律计算ΔH的步骤和方法
4★ 键能与反应化学反应的本质是______________________________。反应物键能越高,断键时需要________的能量越多,反应的活化能可能随之升高,导致反应更难发生。但反应中并不是所有化学键均断裂,这样会使反应变得容易。如N2在部分加成反应或配位反应中,N≡N可能仅发生部分断裂[在特定催化剂作用下,N2可能先断裂一个键(形成N===N),逐步加氢生成中间产物(形成N—N),最终才完全断裂],甚至保持三键但通过配位作用参与反应(如某些固氮酶中的N2-金属配合物)。__________(填“反应物”或“产物”,下同)键能高通常使反应更难启动,________键能高则促进反应进行。实际中需结合活化能、反应条件等因素,不能仅凭键能单一指标判断反应难易。
旧化学键断裂与新化学键形成
例1 (1)从共价键类型及键能角度分析,H2C===CH—CH===CH2 分子为什么易发生加成反应:______________________________________________________。
碳碳双键中σ键键能大,不易断裂;π键键能小,易断裂
例2 (1)CO与N2分子中电子总数相等,结构与物理性质相似。结合事实判断CO和N2中化学性质更活泼的是________,试用下表中的键能数据解释其相对更活泼的原因:______________________________________________________________________________________________________________________________________________________________。
断开CO分子中第一个π键所需要的能量(1 072 kJ/ml-745 kJ/ml=327 kJ/ml)比断开N2分子中第一个π键所需要的能量(946 kJ/ml-418 kJ/ml=528 kJ/ml)小
(2)CO2氧化C2H6脱氢制C2H4的热化学方程式为C2H6(g)+CO2(g)===C2H4(g)+CO(g)+H2O(g) ΔH。几种化学键的键能数据如下,结合键能数据分析该技术的难点:________________________________________________________________________________________________________________________________________________。
CO2中C===O的键能较高,断裂需要较高能量;乙烷分子中C—H的键能大于C—C的键能,难点是选择合适的催化剂在C—H断裂的同时C—C不断裂
核心2 原电池原理与应用1 原电池工作原理
2 燃料电池电极反应式的书写(以CH3OH燃料电池为例,体会不同介质对电极反应的影响)
CH3OH-6e-+H2O===CO2↑+6H+
O2+4e-+4H+===2H2O
O2+4e-+2H2O===4OH-
CH3OH-6e-+3O2-===CO2↑+
O2+4e-===2O2-
3 锂离子电池充、放电分析正极材料:LiMO2(M:C、Ni、Mn等)、LiM2O4(M:C、Ni、Mn等)、LiMPO4(M:Fe等)负极材料:石墨(能吸附锂原子)负极反应式:_______________________________正极反应式:____________________________________
LixCn-xe-===xLi++nC
Li1-xMO2+xLi++xe-===LiMO2
4 新型化学电源电极反应式的书写
核心3 电解原理与应用1 电解池模型——以惰性电极电解CuCl2溶液为例
2 电解池电极反应式的书写(1)提取“信息”书写电极反应式
2Al-6e-+3H2O===Al2O3+6H+
2H++2e-===H2↑
2H2O+2e-===H2↑+2OH-
(2)根据“交换膜”利用“信息”书写电极反应式
2I--2e-===I2
②可用氨水作为吸收液吸收工业废气中的SO2,当吸收液失去吸收能力时,可通过电解法使吸收液再生而循环利用(电极均为石墨电极),并生成化工原料硫酸。其工作示意图如下:
3 电解原理的应用(1)电解饱和食盐水(氯碱工业)阳极反应式:____________________________阴极反应式:______________________________________总化学方程式:________________________________________
(2)电解精炼铜电极材料:粗铜作________;纯铜作________。电解质溶液:______________________。阳极反应式:Zn-2e-===Zn2+、Fe-2e-===Fe2+、Ni-2e-===Ni2+、Cu-2e-===Cu2+阴极反应式:______________________阳极泥的形成:在电解过程中,活动性位于铜之后的银、金等杂质,难以在阳极失去电子变成阳离子而溶解,它们以金属单质的形式沉积在电解槽底部,形成阳极泥。
Cu2++2e-===Cu
(3)电镀如图为金属表面镀银的工作示意图。镀件作________,镀层金属银作________。电解质溶液是__________________。阳极反应式:______________________阴极反应式:______________________特点:阳极溶解,阴极沉积,电镀液的浓度________(填“变大”“变小”或“不变”)。
Ag-e-===Ag+
Ag++e-===Ag
4★ 电极竞争放电电极竞争放电是指在电解池或原电池中,多个可能发生的电极反应(氧化或还原反应)同时存在时,因反应难易程度不同而出现的优先放电现象。竞争放电的本质是不同反应争夺电子的过程。(1)常见放电顺序(以水溶液电解为例)阴极(还原反应,阳离子得电子):金属活动性顺序逆序(部分):Ag+>Hg2+>Fe3+>Cu2+>H+(酸中)>Pb2+>Fe2+>Zn2+>H+(水中)>Al3+>Mg2+>Na+等。如电解含Cu2+和H+的溶液时,阴极产物为________。
(2)竞争放电的顺序受离子浓度等因素影响(电极上产生的气体会阻碍离子吸附)电解食盐水时,Cl-浓度高时(常温下饱和溶液氯化钠溶液浓度为26.4%)在阳极失电子生成Cl2;当Cl-浓度低于15%时,OH-竞争放电产生O2,而且Cl-浓度越低,O2产量越高,Cl2产量降低。
例3 (1)电解含FeSO4、H2SO4的溶液可获得铁。为提高阴极的电解效率,可加入少量具有还原性的弱酸盐柠檬酸钠,其作用是_______________________________________________________________________。
根离子与H+结合,减少H+在阴极放电;防止Fe2+被氧化为Fe3+
pH从5变化到3时,溶液中H+浓
图1 图2
5 金属的电化学防护牺牲阳极法(原电池原理):被保护的金属作________,比被保护的金属活泼的金属作________。外加电流法(电解池原理):被保护的金属作________,惰性电极作________。
核心4 离子交换膜1 离子交换膜的作用(1)可平衡左、右两侧电荷,得到稳定电流。(2)能将两极区隔离,阻止两极区产生的物质接触,防止发生化学反应。
阳离子交换膜只允许Na+通过,阻止阴离子(Cl-)和气体(Cl2)通过。这样既防止了两极产生的H2和Cl2混合爆炸,又避免了Cl2和阴极产生的____________反应生成NaClO而影响烧碱的质量。
(3)制备某些特定产品。用NaOH溶液吸收烟气中的SO2,将所得的Na2SO3溶液进行电解,可循环再生NaOH,同时得到H2SO4,其原理如图所示。①A为__________________;C为____________________。②a为__________(填“阴离子”或“阳离子”,下同)交换膜;b为__________交换膜。
2 多膜电解池中电极反应式的书写及分析双膜三室电解技术处理吸收液(用NaOH溶液吸收烟气中的SO2)
C. 反应的ΔH=4E(C—H)+4E(O—H)-2E(C===O)-4E(H—H)(E表示键能)D. 反应在高温、高压和催化剂条件下进行可提高H2的平衡转化率
【解析】 该反应为气体物质的量减小的反应,故ΔS<0,A错误;平衡常数为生成物浓度的系数幂与反应物浓度的系数幂之比,B正确;热效应ΔH=反应物总键能—生成物总键能=[2E(C===O)+4E(H—H)]-[4E(C—H)+4E(O—H)],C错误;由ΔH-TΔS
相关课件
这是一份微主题4 反应热 电化学 课件 2026届高三化学二轮复习,共19页。PPT课件主要包含了基础回归,反应ΔH0,-1362,分离氯气和氢气,允许Na+迁移获得,NaOH溶液,体系建构,名卷优选,+824,-824等内容,欢迎下载使用。
这是一份微主题4 反应热 电化学 课件 2025届高考化学二轮复习,共60页。PPT课件主要包含了基础回归,反应ΔH0,-1362,分离氯气和氢气,防止OH-迁移避,免氯气与碱反应,体系建构,名卷优选,+824,-824等内容,欢迎下载使用。
这是一份新高考化学二轮复习导学案课件 微主题5 反应热 电化学(含解析),共60页。PPT课件主要包含了命题规律,高考回眸,+908,C石墨s+,-223,+170,模考前沿,核心突破,能力提升,kJmol等内容,欢迎下载使用。
相关课件 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





.png)




