

2024-2025学年福建省南平市高一(上)期末化学试卷-自定义类型
展开 这是一份2024-2025学年福建省南平市高一(上)期末化学试卷-自定义类型,共8页。试卷主要包含了单选题,流程题,实验题,简答题等内容,欢迎下载使用。
1.中科院发现宋代建盏中含罕见的“永磁”新生物质(ε—Fe2O3),可使茶水变得绵软清甜。这种“永磁”新生物质属于( )
A. 金属单质B. 氧化物C. 氢氧化物D. 合金
2.“84消毒液”是以次氯酸钠为有效成分的液体消毒剂。下列说法错误的是( )
A. 加入食醋可增强消毒效果
B. 不能与洁厕剂(含盐酸)混合使用
C. 可用于皮肤、丝、毛、地板等物品消毒
D. 次氯酸钠的电离方程式为NaClO=Na++ClO-
3.“天宫课堂”中王亚平将泡腾片(含有碳酸氢钠和固体酸)放进注有蓝色试剂的水球内,粥产生气泡形成“太空欢乐球”。下列说法正确的是( )
A. 水球内的蓝色试剂可能是酚酞试液
B. 气泡为二氧化碳,二氧化碳属于电解质
C. 若再往水球中注入浓氢氧化钠溶液,水球会变大
D. 空间站里气泡感受不到浮力会“安逸”地待在水球里
4.下列各组离子在水溶液中能大量共存的是( )
A. Ca2+、、S2-、OH-B. K+、Ag+、Cl-、
C. Na+、Mg2+、、D. Fe2+H+、、
5.氢化钠(氢元素为-1价)作为生氢剂的原理为NaH+H2O=NaOH+H2↑。设NA为阿伏加德罗常数的值。下列说法正确的是( )
A. 18gH2O中含有的质子数为10NA
B. 消耗1mlNaH转移的电子数为2NA
C. 生成的11.2LH2中含氢原子数为NA
D. 0.1ml•L-1NaOH溶液中含有Na+的数目为NA
6.下列离子反应方程式正确的是( )
A. 用氢氧化钠溶液吸收氯气:
B. 过氧化钠与水反应:
C. 向稀硝酸中加入过量的铁粉:
D. 向小苏打溶液中滴入氢氧化钾溶液:
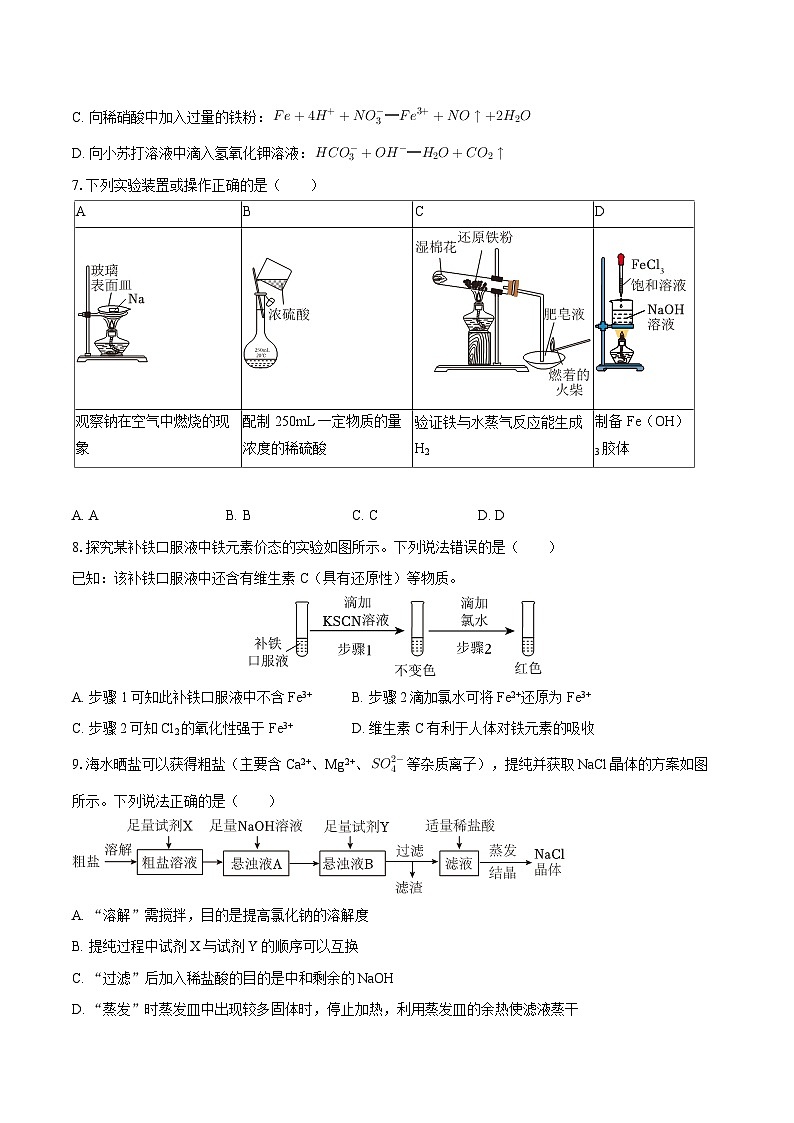
7.下列实验装置或操作正确的是( )
A. AB. BC. CD. D
8.探究某补铁口服液中铁元素价态的实验如图所示。下列说法错误的是( )
已知:该补铁口服液中还含有维生素C(具有还原性)等物质。
A. 步骤1可知此补铁口服液中不含Fe3+B. 步骤2滴加氯水可将Fe2+还原为Fe3+
C. 步骤2可知Cl2的氧化性强于Fe3+D. 维生素C有利于人体对铁元素的吸收
9.海水晒盐可以获得粗盐(主要含Ca2+、Mg2+、等杂质离子),提纯并获取NaCl晶体的方案如图所示。下列说法正确的是( )
A. “溶解”需搅拌,目的是提高氯化钠的溶解度
B. 提纯过程中试剂X与试剂Y的顺序可以互换
C. “过滤”后加入稀盐酸的目的是中和剩余的NaOH
D. “蒸发”时蒸发皿中出现较多固体时,停止加热,利用蒸发皿的余热使滤液蒸干
10.向盛有20mL0.03ml•L-1NaHSO4溶液的烧杯中,匀速逐滴加入0.03ml•L-1Ba(OH)2溶液,测得电导率与滴入Ba(OH)2溶液的体积变化关系如图所示。(已知:电导率表示溶液传导电流的能力,离子浓度越大,电导率越强)。下列说法错误的是( )
A. a点溶液中
B. b点溶液中
C. c点溶液中
D. d点溶液中c(Na+)=c(OH-)=0.015ml•L-1
二、流程题:本大题共1小题,共15分。
11.实验室探索一种某工业废水(主要含大量Mn2+、H+。Cl-以及Fe2+、Fe3+、Cu2+)回收二氯化锰晶体工艺流程如图:
已知:MnS难溶于水,“除铜”可生成更难溶于水的CuS。
Ⅰ.工业废水中Fe2+的检验
(1)有同学设计用KMnO4溶液检测该工业废水中是否含有Fe2+,该方案不合理的原因为 ______ 。
Ⅱ.废水的净化与利用
(2)“氧化”滴入H2O2时被氧化的微粒为 ______ (填离子符号),该离子既有氧化性又有还原性,判断的依据为 ______ 。
(3)“除铁”观察到的现象为 ______ ,化学方程式为 ______ 。
(4)“除铜”分离出沉淀的操作名称为 ______ ,所用的玻璃仪器除玻璃棒外还有 ______ 、______ 。
(5)“多步操作”中将MnCl2和NH4Cl分离所选择的最佳温度为 ______ ℃(溶解度曲线如图所示)。分离后的产物NH4Cl的用途为 ______ (写出一种即可)。
三、实验题:本大题共1小题,共15分。
12.三氯化氮(NCl3)可用于漂白和消毒。实验室用氯气和氨气为原料制取少量NCl3并探究其与水反应的产物。
【资料】
ⅰ.NCl3是黄色油状液体,有刺激性气味,熔点为-40℃,沸点为71℃,95℃以上易爆炸;
ⅱ.制备NCl3原理为4NH3+3Cl2=NCl3+3NH4Cl;
ⅲ.NH4Cl会部分溶解在NCl3中,NH4Cl的分解温度为300℃左右。
Ⅰ.NCl3制备
实验装置如图所示。
回答下列问题:
(1)装置A制取氯气,试剂X能选用的是 ______ (填标号)。
a.KMnO4
b.KCl
c.CaCO3
d.MnO2
(2)除去氯气中HCl气体的装置是 ______ (填装置标号);
装置E的名称为 ______ ,其作用为 ______ 。
(3)装置F中发生反应的化学方程式为 ______ 。
(4)①三颈烧瓶中的现象除产生大量白烟外,还可观察到 ______ ;
②欲从a口导出NCl3气体再冷凝得到少量NCl3,需控制水浴的温度范围为 ______ 。
Ⅱ.NCl3与水反应产物的探究
取收集到的NCl3滴入一定量40℃左右的水中,有无色无味的气体生成。静置后得溶液A,进行如下实验:
(查相关资料可知:NCl3与水反应产生的气体为N2)
[实验1]
[实验2]
(5)根据实验1的现象判断:溶液A具有酸性和 ______ 性。
(6)实验2中“红色不褪去”的原因为 ______ 。
(7)综上所述,NCl3与水反应的化学方程式为 ______ 。
四、简答题:本大题共2小题,共30分。
13.某研究团队对氮肥厂产生的废水和尾气进行处理并制备NaNO3晶体。
Ⅰ.废水中的转化与处理
(1)利用微生物的作用实现转化,在碱性条件下,被O2氧化成转移电子的物质的量为 ______ ml。在一定条件下向溶液中加入甲醇(CH3OH),实现HNO3→N2转化,体现甲醇的 ______ 性。
(2)钠离子交换树脂(用NaR表示)是不溶性的高分子化合物。利用钠离子交换树脂将废水中的与Na+进行交换而去除,离子方程式为 ______ 。
Ⅱ.尾气的处理及NaNO3晶体的制备
部分工艺流程如图:
(3)若工业尾气中NO与NO2的体积比为1:1,用NaOH溶液吸收的化学方程式为 ______ 。
(4)“一系列操作”中可加入的物质为 ______ (填标号)。
a.热空气
b.Na2S
c.H2O2
d.BaCl2
(5)现配制500mL1ml•L-1的NaNO3溶液。
①计算:需要NaNO3固体的质量为 ______ g;
②图1所示的步骤应在 ______ (填标号);
A.ab间
B.bc间
C.cd间
D.d后
③溶液配制时会导致NaNO3溶液浓度偏小的情况是 ______ (填标号)。
A.称量时将NaNO3固体置于托盘天平右盘
B.容量瓶在使用前未干燥
C.定容时俯视刻度线
D.定容摇匀后,发现液面下降,继续加水至刻度线
14.物质类别和核心元素的化合价是研究物质的重要角度。根据图示回答下列问题:
(1)b为 ______ (填化学式)。
(2)实现①和③的转化需加入 ______ (填“氧化剂”或“还原剂”)。
(3)H2S与SO2混合反应,生成含硫元素物质的颜色为 ______ ,氧化产物与还原产物的质量之比为 ______ 。
(4)H2S在充足的空气中点燃实现②的转化,化学方程式为 ______ 。
(5)通过复分解反应实现⑤的转化,离子方程式为 ______ 。
(6)酿造葡萄酒过程产生的杂菌会影响葡萄酒的酿造和保存,另外葡萄酒中所含的还原性物质易被氧化影响口感。使用SO2食品添加剂可解决这两大问题。
ⅰ.SO2食品添加剂的作用为 ______ 、______ 。
ⅱ.实验室常用碘一淀粉法实现④的转化来测定葡萄酒中SO2的含量,化学方程式为SO2+I2+2H2O=2HI+H2SO4。取某葡萄酒100mL,经测定消耗2.5×10-4ml的I2,该葡萄酒中SO2的含量 ______ (填“合格”或“不合格”)。(国家规定葡萄酒中SO2的含量小于0.25g•L-1)。
1.【答案】B
2.【答案】C
3.【答案】D
4.【答案】C
5.【答案】A
6.【答案】A
7.【答案】C
8.【答案】B
9.【答案】D
10.【答案】B
11.【答案】Cl-也能使酸性高锰酸钾溶液褪色,会干扰Fe2+的检验 Fe2+;化合价处于中间价态,既可以升高到+3价,体现还原性,也可以降低到0价,体现氧化性 生成红褐色沉淀;FeCl3+3NH3•H2O=Fe(OH)3↓+3NH4Cl 过滤;烧杯;漏斗 30;作化肥或化工原料
12.【答案】a B;(球形)干燥管;除去氨气中的水蒸气或干燥氨气 2NH4Cl+Ca(OH)22NH3↑+CaCl2+2H2O 有黄色油状液体生成;71℃~95℃ 漂白 光照较长时间,溶液中次氯酸分解,无漂白性,故红色不褪去 2NCl3+3H2O=N2↑+3HClO+3HCl
13.【答案】8;还原 NO+NO2+2NaOH=2NaNO2+H2O ac 42.5;C;AD
14.【答案】H2SO3 还原剂 淡黄色;2:1 2H2S+3O2=2SO2+2H2O +2H+=SO2↑+H2O 防腐;抗氧化;合格 A
B
C
D
观察钠在空气中燃烧的现象
配制250mL一定物质的量浓度的稀硫酸
验证铁与水蒸气反应能生成H2
制备Fe(OH)3胶体
相关试卷
这是一份2024-2025学年福建省南平市高一(上)期末化学试卷-自定义类型,共8页。试卷主要包含了单选题,流程题,实验题,简答题等内容,欢迎下载使用。
这是一份2024-2025学年福建省南平市高二(上)期末化学试卷-自定义类型,共8页。试卷主要包含了单选题,流程题,实验题,简答题等内容,欢迎下载使用。
这是一份2024-2025学年福建省漳州市高一(上)期末化学试卷-自定义类型,共8页。试卷主要包含了单选题,填空题,流程题,实验题,计算题等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 









