

山东省滨州市惠民县(五四制)2024-2025学年九年级上学期期末化学试卷(学生版)
展开 这是一份山东省滨州市惠民县(五四制)2024-2025学年九年级上学期期末化学试卷(学生版),共8页。试卷主要包含了答卷前,考生务必用0,第Ⅱ卷必须用0,0g等内容,欢迎下载使用。
1.本试卷分第Ⅰ卷和第Ⅱ卷两部分,共7页。满分100分。考试用时60分钟。考试结束后,将试题卷和答题卡一并交回。
2.答卷前,考生务必用0.5毫米黑色签字笔将自己的姓名、准考证号、座号填写在试题卷和答题卡规定的位置上。
3.第Ⅰ卷每小题选出答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑;如需改动,用橡皮擦干净后,再选涂其他答案标号。答案不能答在试题卷上。
4.第Ⅱ卷必须用0.5毫米黑色签字笔作答,答案必须写在答题卡各题目指定区域内相应的位置,不能写在试题卷上;如需改动,先划掉原来的答案,然后再写上新的答案;不准使用涂改液、胶带纸、修正带。不按以上要求作答的答案无效。
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Na 23 Cl 35.5 Fe 56 Cu 64 Ag 108
第Ⅰ卷(选择题 共48分)
一、选择题(本大题包括16小题,每小题3分,共48分。每小题只有一个选项符合题意。)
1.下列物质的使用过程中发生了化学变化的是
A.干冰降雨B.活性炭净水
C.醋酸除水垢D.酒精清洗碘渍
2.正确的实验操作是完成好化学实验的基本要求。小明同学在完成“二氧化碳的实验室制取与性质”实验时,进行了下列操作,其中正确的是
A.点燃酒精灯B.倾倒液体
C.滴加液体D.闻气体气味
3.豆腐是我们日常食品,它能提供多种氨基酸,含量最多是亮氨酸(C6H13NO2)。下列关于亮氨酸的说法错误的是
A.一个亮氨酸分子中含有22个原子B.亮氨酸由4种元素组成
C.亮氨酸中碳元素与氢元素质量比是6:13D.亮氨酸中碳元素的质量分数最高
4.模型是学习化学的重要方法,下列有关模型正确的是
A.原子结构模型B.地壳元素含量模型
C.物质分类模型D.空气组成模型
5.下列对实验结果分析正确的是
A.测定空气里氧气含量时,若装置漏气,会导致测定结果偏高
B.验证质量守恒定律时,若不采用密闭装置,一定会导致反应前后质量总和不相等
C.除去粗盐中难溶性杂质的过程中,若蒸发时液体溅出,会导致产率偏低
D.配制一定溶质质量分数的溶液,若装瓶时洒出一部分,会导致溶质质量分数变小
6.2021年3月,三星堆遗址出土了黄金面具残片,结合如图,下列说法正确的是
A.金元素符号是AUB.金原子的质子数是79
C.金原子的核外电子数是118D.金的相对原子质量是197.0g
7.下列各种“水”中属于混合物的是
A.矿泉水B.纯净水
C.冰水混合物D.蒸馏水
8.下列物质的转化在给定条件下均能实现的是
A.
B.溶液
C.溶液NaCl溶液NaOH溶液
D.溶液
9.下列物质间转化均能通过一步反应实现的是
A.Cu→Cu(NO3)2→KNO3B.Fe→Fe2O3→FeCl2
C.Na2SO4→NaNO3→NaClD.KOH→Ba(OH)2→NaOH
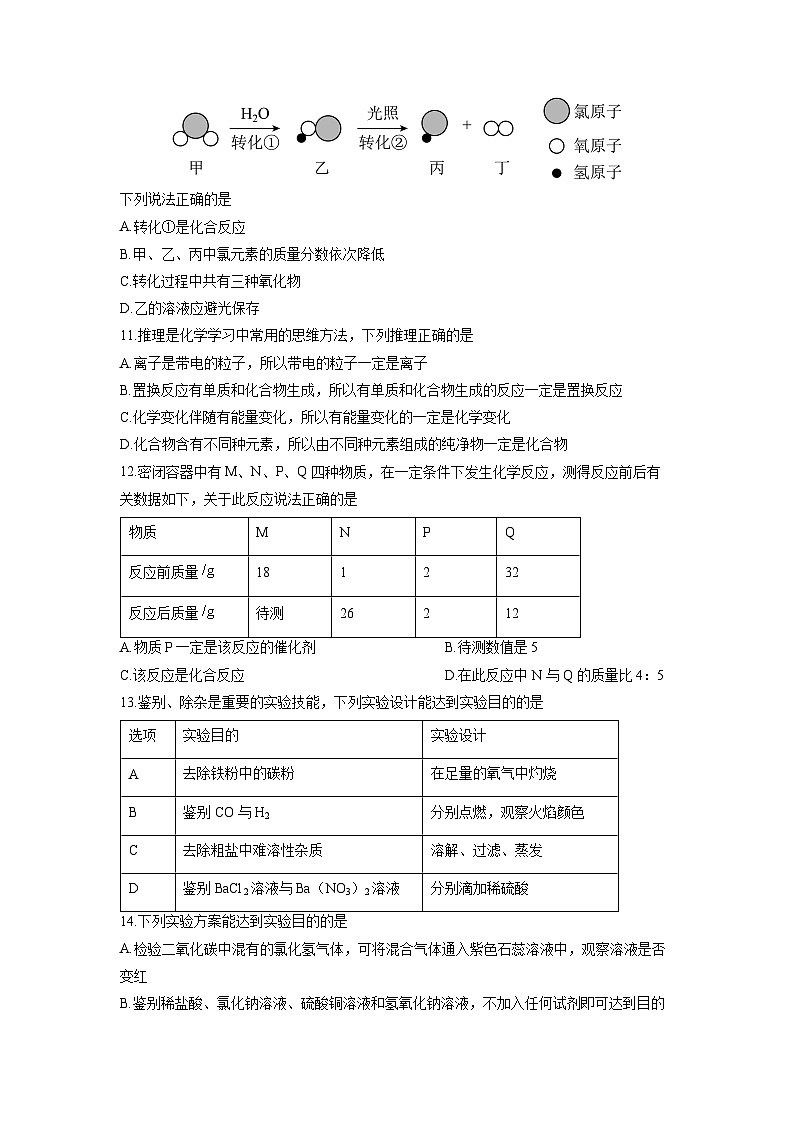
10.物质甲、乙均可灭杀新型冠状病毒(2019﹣nCV),灭杀过程中有如图转化。
下列说法正确的是
A.转化①是化合反应
B.甲、乙、丙中氯元素的质量分数依次降低
C.转化过程中共有三种氧化物
D.乙的溶液应避光保存
11.推理是化学学习中常用的思维方法,下列推理正确的是
A.离子是带电的粒子,所以带电的粒子一定是离子
B.置换反应有单质和化合物生成,所以有单质和化合物生成的反应一定是置换反应
C.化学变化伴随有能量变化,所以有能量变化的一定是化学变化
D.化合物含有不同种元素,所以由不同种元素组成的纯净物一定是化合物
12.密闭容器中有M、N、P、Q四种物质,在一定条件下发生化学反应,测得反应前后有关数据如下,关于此反应说法正确的是
A.物质P一定是该反应的催化剂B.待测数值是5
C.该反应是化合反应D.在此反应中N与Q的质量比4:5
13.鉴别、除杂是重要的实验技能,下列实验设计能达到实验目的的是
14.下列实验方案能达到实验目的的是
A.检验二氧化碳中混有的氯化氢气体,可将混合气体通入紫色石蕊溶液中,观察溶液是否变红
B.鉴别稀盐酸、氯化钠溶液、硫酸铜溶液和氢氧化钠溶液,不加入任何试剂即可达到目的
C.除去氯化铜溶液中的硫酸铜,可向其中加入过量的氯化钡溶液,过滤
D.除去铁粉中的氧化铁,可向其中加入足量的稀盐酸,过滤
15.甲、乙两个排污口共排放了H2SO4、KNO3、MgCl2和NaOH四种物质,每个排污口各排放其中的两种不同物质。下列关于污水成分的分析合理的是( )
A.H2SO4和KNO3一定来自同一排污口
B.H2SO4和MgCl2一定来自同一排污口
C.H2SO4和NaOH一定来自同一排污口
D.将两处污水混合后,溶液一定呈中性
16.向装有一定量硝酸铜和硝酸银混合溶液的试管中,缓慢加入细铁粉,充分反应。下列关于试管中物质的变化关系图错误的是
A.B.
C.D.
第Ⅱ卷(非选择题 共52分)
二、填空题(本大题包括6小题,共30分。)
17.用化学用语填空。
(1)酸具有相似的化学性质,其原因是酸溶液中都含有______。
(2)标出工业用盐中氮元素的化合价______。
(3)焙制糕点所用的发酵粉主要成分之一是小苏打,它的化学式是______。
(4)保持氩气化学性质的微粒______。
18.生命的孕育和维系需要水。
(1)如图1是探究水组成的实验装置。反应开始后,试管a收集到的气体是______,该实验说明水是由______组成。
(2)图2是氧原子的结构示意图,x的值为______。
(3)图3是水分子分解示意图。请将B框补充完整。
(4)生活中经常使用活性炭净化水,主要利用活性炭的______性。高铁酸钠是一种新型水处理剂,高铁酸钠中铁元素的化合价为______价。
19.请根据图中甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
(1)在________℃时,甲、丙两种物质的溶解度相等。
(2)在t2℃时,向盛有25g甲物质的烧杯中加入50g水,充分溶解后,所得溶液的质量为________g。
(3)若乙物质中混有少量甲物质,最好采用________(填“降温结晶”或“蒸发结晶”)的方法提纯乙。
(4)t2℃时,甲、乙、丙三种物质的饱和溶液同时降温至t1℃,所得溶液中溶质质量分数由大到小的顺序为________。
20.小明到超市购买了一批物品,请根据相关信息回答下列问题。
(1)牛奶可以为人体补充钙元素,钙元素属于人体含有的______(填“常量”或“微量”)元素;
(2)小明买了一个便携式净水器,该净水器适合长期野外工作人群使用,其内部结构示意图如图所示,请结合示意图思考,MIR高聚碘杀菌树脂杀菌过程属于______变化(填“物理”或“化学”)。此种“生命吸管”虽广泛使用,但海上应急却不能使用,原因是______。
(3)为了保障家人健康,小明决定使用84消毒液对房屋进行消毒。某84消毒液部分说明如图:
使用时将84消毒液稀释的步骤是:计算、______、混匀;根据注意事项,平时不用84消毒液时应______保存。
21.我国力争2060年前实现“碳中和”,二氧化碳的捕获、储存、利用和转化等是实现目标的重要途径。某小组设计的二氧化碳捕获过程如图所示(反应条件已略去),A—G是初中化学中常见的物质,其中C是一种常见的溶剂。请回答下列问题:
(1)固态的F俗称为______。
(2)反应①的化学方程式为______。
(3)反应③的化学方程式为______。
(4)D的一种用途是______。
22.实验室有一瓶除去难溶性杂质的粗盐样品,其中还含有少量氯化镁和氯化钙。为了得到较纯净的食盐晶体,同学们设计如下实验方案,请你参与他们的实验探究。
(1)实验过程中,向粗盐水中先加入过量氢氧化钙溶液,再加入过量碳酸钠溶液,依次加入的目的是______,写出两种盐之间发生反应的化学方程式______。
(2)实验过程中,用到的操作有______,得到食盐晶体时应在______(填仪器名称)中加热得到。
三、实验题(本大题包括2小题,共12分。)
23.如图为实验室制取并收集气体的装置图,回答下列问题。
(1)a仪器的名称是__。
(2)实验室用高锰酸钾制取并收集干燥的氧气应选用的装置组合是___(填序号)。
(3)若用F装置收集并测量氧气的体积,应在__(填“d”或“e”)端连接量筒。
(4)实验室制取二氧化碳的化学方程式是___,用B装置制取二氧化碳的优点是_____,制取时应将大理石放在___(填“b”或“c”)处。
24.中和反应是一类重要的化学反应。某同学利用图1装置研究稀盐酸与氢氧化钠液反应的过程,并用pH和温度传感器测量反应过程中相关物理量的变化情况,得到图2和图3
(1)烧杯中发生反应的化学方程式为____________________;
(2)仪器A中溶液的溶质是_________________(填化学式);
(3)图3中V的数值最接近_______(填“6”、“12”或“16”);
(4)下列说法错误的是____________。
A 图2中b点所示溶液中的溶质是NaCl和NaOH;
B 取图2中d点所示溶液加热蒸干所得固体为纯净物
C 图2中c→d所示溶液中NaCl的质量不断增加;
D 图3中e→f变化趋势可说明该反应是放热反应。
四、计算题(本大题包括1小题,共10分。)
25.洁厕灵的有效成分为HCl,李强同学测定某品牌洁厕灵中HCl的质量分数。他将100.0g洁厕灵倒入锥形瓶中,逐次加入等质量相同质量分数的Na2CO3溶液,测出每次完全反应后溶液的总质量,实验数据记录如下表。
请根据实验数据分析解答下列问题:
(1)表格中M数值为 。
(2)恰好完全反应时消耗Na2CO3的质量是多少
(3)该洁厕灵中HCl的质量分数是多少?
物质
M
N
P
Q
反应前质量
18
1
2
32
反应后质量
待测
26
2
12
选项
实验目的
实验设计
A
去除铁粉中的碳粉
在足量的氧气中灼烧
B
鉴别CO与H2
分别点燃,观察火焰颜色
C
去除粗盐中难溶性杂质
溶解、过滤、蒸发
D
鉴别BaCl2溶液与Ba(NO3)2溶液
分别滴加稀硫酸
84消毒液
有效成分:主要成分为次氯酸钠(NaClO)
主要用途:消毒杀菌,灭活病毒
使用配比:按原液与水体积比稀释
注意事项:
①外用消毒剂,需稀释后使用
②受热或见光易分解
第一次
第二次
第三次
第四次
第五次
加入Na2CO3溶液的质量/g
20.0
200
20.0
20.0
20.0
反应后溶液的总质量/g
118.9
1378
M
175.6
195.6
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 





