
四川省成都市成华区2025-2026学年高二上学期10月考试化学试卷
展开 这是一份四川省成都市成华区2025-2026学年高二上学期10月考试化学试卷,共10页。试卷主要包含了单项选择题,填空题等内容,欢迎下载使用。
可能用到的相对原子质量:S-32H-1O-16
一、单项选择题(本题共 15 小题,每小题 3 分,共 45 分)
社会的发展、科技的进步离不开化学。下列说法中不正确的是
“玉兔号”月球车上的太阳能电池可将太阳能转化为电能
除去工业废水中的 Cu2+、Hg2+可用 Na2S 溶液作沉淀剂
二氧化硅的半导体性能在芯片中提升了 AI 技术的表现
用 TiCl4 制备 TiO2 时,需加入大量的水同时加热
下列表示或说法不正确的是
图标 的含义是:防止锋利物品扎伤或割伤
依据相同温度下可逆反应的 Q 与 K 大小的比较,可推断反应进行的方向
用电子式表示 KCl 的形成过程:
H2O2 的电子式:
实验是探究化学的基础。下列有关装置、实验操作与目的均正确的是
硫及其化合物部分转化关系如图。设 NA 为阿伏加德罗常数的值,下列说法正确的是
装置
操作与目的
A.用 KMnO4 标准液滴定 Na2SO3 溶液
B.配制一定物质的量浓度的 KCl 溶液
装置
操作与目的
C. pH 试纸测定溶液 pH
D.喷泉实验
标准状况下,11.2L SO2 中原子总数为 0.5NA
3
100 mL 0.1 ml·L-1 Na2SO3 溶液中,SO 2-数目为 0.01NA
反应①每消耗 3.4 g H2S,生成物中硫原子数目为 0.1NA
反应②每生成 1ml 还原产物,转移电子数目为 2NA
下列叙述正确的是
A.用 CH3COOH 溶液做导电性实验,灯泡很暗,能证明 CH3COOH 是弱电解质 B.两种醋酸溶液的物质的量浓度分别 c1 和 c2,pH 分别为 a 和 a+1,则 c1 = 10 c2 C.常温下,pH=11 的 NaOH 溶液与 pH=3 的醋酸溶液等体积混合,滴入石蕊溶液呈红色 D.常温下,pH 均为 8 的氢氧化钠溶液和 CH3COONa 溶液中,由水电离出的 c(OH-)之比为 1:1
X、Y、Z、W、Q 为短周期元素,原子序数依次增大,最外层电子数之和为 18。X 元素的原子失去一个电子后成为一个裸露的质子,Z 和 Q 同族,Z 的原子序数是 Q 的一半,W 元素焰色试验呈黄色。下列说法错误的是
A. X、Y 组成的最简单的化合物有可燃性B. X、Q 组成的化合物有还原性
C. Z、W 组成的化合物含有离子键D. W、Q 组成的化合物溶于水呈酸性
下列选项中的物质能按图示路径在自然界中转化,且甲和水可以直接生成乙的是
选项
甲
乙
丙
A
Cl2
NaClO
NaCl
B
SO2
H2SO4
CaSO4
C
Fe2O3
Fe(OH)3
FeCl3
D
CO2
H2CO3
Ca(HCO3)
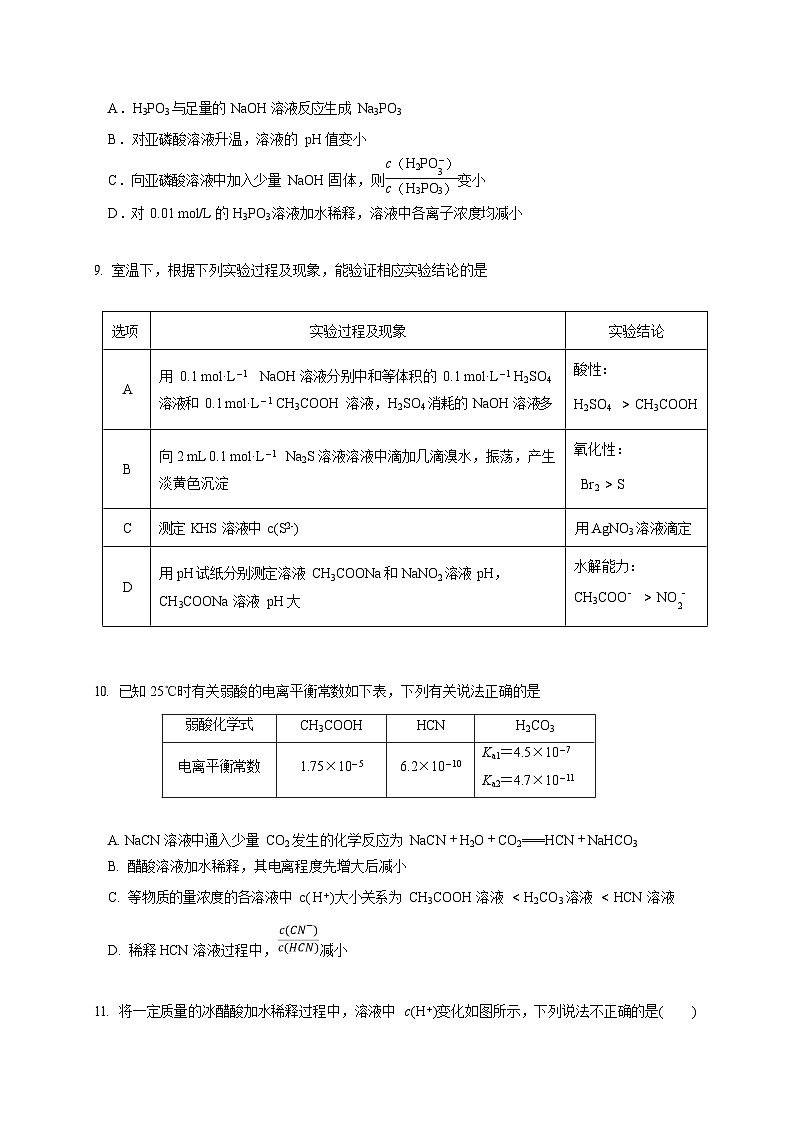
亚磷酸(H3PO3)是二元弱酸,常温下电离常数 Ka1=1.0×10-2,Ka2=2.6×10-7。下列说法正确的是
A.H3PO3 与足量的 NaOH 溶液反应生成 Na3PO3 B.对亚磷酸溶液升温,溶液的 pH 值变小
3
c(H2PO-)
C.向亚磷酸溶液中加入少量 NaOH 固体,则c(H3PO3) 变小
D.对 0.01 ml/L 的 H3PO3 溶液加水稀释,溶液中各离子浓度均减小
室温下,根据下列实验过程及现象,能验证相应实验结论的是
已知 25℃时有关弱酸的电离平衡常数如下表,下列有关说法正确的是
NaCN 溶液中通入少量 CO2 发生的化学反应为 NaCN+H2O+CO2===HCN+NaHCO3
醋酸溶液加水稀释,其电离程度先增大后减小
等物质的量浓度的各溶液中 c( H+)大小关系为 CH3COOH 溶液 < H2CO3 溶液 < HCN 溶液
稀释 HCN 溶液过程中,减小
将一定质量的冰醋酸加水稀释过程中,溶液中 c(H+)变化如图所示,下列说法不正确的是()
选项
实验过程及现象
实验结论
A
用 0.1 ml·L-1 NaOH 溶液分别中和等体积的 0.1 ml·L-1 H2SO4
溶液和 0.1 ml·L-1 CH3COOH 溶液,H2SO4 消耗的 NaOH 溶液多
酸性:
H2SO4 > CH3COOH
B
向 2 mL 0.1 ml·L-1 Na2S 溶液溶液中滴加几滴溴水,振荡,产生淡黄色沉淀
氧化性:
Br2 > S
C
测定 KHS 溶液中 c(S2-)
用 AgNO3 溶液滴定
D
用 pH 试纸分别测定溶液 CH3COONa 和 NaNO2 溶液 pH, CH3COONa 溶液 pH 大
水解能力:
CH3COO- > NO -
2
弱酸化学式
CH3COOH
HCN
H2CO3
电离平衡常数
1.75×10-5
6.2×10-10
Ka1=4.5×10-7
Ka2=4.7×10-11
若使 b 点对应的溶液中 c(CH3COO-)增大、c(H+)减小,可采用加入 NaOH 固体的方法
a、b、c 三点对应溶液的导电能力:cK2
在不同温度下的水溶液中离子浓度曲线如图所示,下列说法正确的是
在水中加少量酸,可实现 c 点向 d 点移动
纯水 T℃的电离度是 25℃时的 10 倍
4
b 点对应的溶液中大量存在:K+、Na+、MnO -、I-
T℃时,将 pH=4 的硫酸与 pH=10 的 KOH 等体积混合后,溶液呈中性
25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是
A.0.1 ml·L-1 (NH4)2Fe(SO4)2 溶液中:c(SO42-)>c(Fe2+)>c(NH4+)>c(H+)
B.pH=11 的氨水和 pH=3 的盐酸溶液等体积混合,所得溶液中:c(Cl-)>c(NH4+)>c(OH-)>c(H+)
C.在 0.1 ml·L-1 Na2CO3 溶液中:2c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3)
D.20 mL 醋酸钠溶液与等浓度盐酸10 mL 混合后溶液显酸性:c(CH3COO-)>c(Cl-)>c(CH3COOH)
常温下,向 1 L pH=10 的 NaOH 溶液中持续通入 CO2。通
入的 CO2 的体积(V)与溶液中水电离出的 OH-浓度(c)的关系如图所示。下列叙述不正确的是()
A. b 点溶液中:c(OH-)=1×10-7 ml·L-1
B.a 点溶液中:水电离出的 c(H+)=1×10-10 ml·L-1
C.c 点溶液中:c(Na+)>c(CO2-)>c(HCO-)
33
D.d 点溶液中:溶液是 NaHCO3 和 H2CO3 的混合液
二、填空题(本题共 4 题,每空 2 分,共 55 分)
16.( 14 分)过氧化氢是重要的氧化剂,也可作还原剂,它的水溶液称为双氧水,常用于消毒剂、杀菌、漂白等。某化学研究性学习小组取一定量的市售过氧化氢溶液, 测定其中 H2O2 的质量分数。
量取10.00 mL 密度为ρ g/mL 的市售过氧化氢溶液,应选用的滴定管是(填“酸式”或“碱式”)滴定管。
将上述溶液配制成 250.00 mL,配制的过程需要用到的玻璃仪器是烧杯、玻璃棒、
(填名称), 移取配置后的过氧化氢溶液 25.00 mL 至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释。用高锰酸钾标准溶液来滴定该过氧化氢溶液, 滴定到达终点的现象是:当滴入最后半.滴.高锰酸
钾,。
若滴定开始和结束时,滴定管中的液面如图所示,则终点读数为mL。
①完成滴定过程中反应的离子方程式。
②重复滴定三次,平均耗用 cml/L KMnO4 标准溶液 VmL,则原过氧化氢溶液中过氧化氢的
质.量.分数为 。(用字母表示)
③下列操作会导致测定结果偏高的是(填序号)。
滴定前滴定管未用 KMnO4 溶液润洗
移取 25.00 mL 过氧化氢待测液注入有少量蒸馏水的锥形瓶中
滴定开始时,装 KMnO4 溶液的滴定管有气泡未排出,滴定结束气泡消失
将 H2O2 溶液配制成 250.00 mL 溶液时,仰视刻度线定容
17.(12 分)磷酸铁锂电池是我国新能源汽车产业发展初期的主流电池,具有安全性能好、循环寿命
长、成本低等突出优点。一种以废磷酸铁锂正极渣(主要含有 LiFePO4、炭黑、铝粉、有机黏结剂)为原料,回收制备电池级磷酸铁锂的流程如图所示:
已知 1:常温下,Fe(OH)3 沉淀在 pH ≥ 2.8 可稳定存在。
a1a2a3
已知 2:常温下,H3PO4 的电离常数K 7.1103 、K 6.2 108 、K 4.51013 。回答下列问题:
(1)浸出前,需将结块的废磷酸铁锂正极渣粉碎成粉,目的是。 (2)常温下,NaH2PO4 溶液呈(填“酸性”“碱性”或“中性”)。
加入 H2O2 的离子反应方程式:;
在实际操作中H2O2 的用量约为理论量的 1.2 倍,其原因可能是。
沉淀过程中,控制 pH 不大于 2 的原因是。
写出浸出过程中 LiFePO4 发生反应生成 Fe(H2PO4)2 的化学方程式:。
18.( 15 分)MgCl2 在金属冶炼、食品添加等行业应用广泛,熔点为 714℃,易水解和形成结晶水合物。学习小组在实验室对 MgCl2 的制备进行探究。
由 MgO、C 和 Cl2 制备 MgCl2 并验证生成气体产物中有 CO 和 CO2
制备氯气
①m 的名称为。
②氯气的发生装置可选择图中的(填大写字母),反应的化学方程式为。
③欲收集一瓶纯净的氯气,按气流从左到右的方向,上述装置的合理连接顺序为:a→
(用小写字母表示,部分装置可重.复.使用)。
制备 MgCl2 并验证生成气体产物中有 CO 和 CO2。将上述制得的 Cl2 持续充入如图所示装置中进行实验。 ( 已知:PdCl2 + CO + H2O===Pd↓(黑色)+ 2HCl + CO2 )
①H 的作用为。
②试剂 X 可选用。
③ 若生成 CO 和 CO2 的物质的量之比为 10:1 , 则 G 的反应管中发生的化学反应方程式为。
(3)MgCl2 溶液经过蒸发浓缩、冷却结晶,可得 MgCl2·xH2O。取 MgCl2·xH2O 样品,在不断通入
HCl 的条件下充分加热失去结晶水,通 HCl 的原因为。
19.( 14 分)H2 在冶金、电力等领域应用广泛。请回答下列问题:
H2 还原 NO 的反应为 2H 2 (g) + 2 NO (g) N2(g) + 2H2O(1),其反应速率的表达式为 v=k·cm(NO)·cn(H2)(k 是速率常数,只与温度有关)。某温度下,反应速率与反应物浓度的变化关系如下:
由表中数据可知,m=,n=。
合成氨反应 N2(g) + 3H2(g) 2NH3(g) 在常温下能自发进行,其原因是。用 H2 催化还原法可降低水中 NO3- 的浓度,得到的产物能参与大气循环,则反应后溶液的
编号
c(H2) / (ml/L)
c(NO) / (ml/L)
V / (ml/Lmin)
1
0.10
0.10
0.414k
2
0.10
0.20
1.656k
3
0.50
0.10
2.070k
pH(填“升高”、“降低”或“不变”)。
向密闭容器中充入 1 ml CO 和 2.2mlH2,在恒温恒压条件下发生反应 CO(g)+2H2(g) CH3OH(g),平衡时,CO 的转化率 α(CO) 随温度、压强的变化情况如下左图。
① M 点时,H2 的转化率为(计算结果精确到 0.1%),该反应的分压平衡常数 Kp= (用 p 的代数式表示)。
② 不同温度下,该反应的平衡常数的对数值(lgK)如上右图,其中 A 点为 506K 时平衡常数的对数值,则 B、C、D、E 四点中能正确表示该反应的 lgK 与温度(T)的关系的点是。
2025-2026 学年度(上)阶段性考试(一)
高二化学答案
一、单项选择题(本题共 15 小题,每小题 3 分,共 45 分)
二、填空题(本题共 4 题,每空 2 分,共 55 分)
16.( 14 分)
酸式 (2 分)
250mL 容量瓶、胶头滴管 (2 分,各 1 分)
溶液由无色变为浅红色(或溶液变为浅红色),且 30 秒内不褪色(2 分)
(3)26.10( 2 分)
42 222
(4)①2 MnO -+5 H O +6 H+= 2Mn2+ + 5O ↑ + 8 H O(2 分)
17CV
②2ρ % (2 分)
③ A、C(2 分)
17.( 12 分,每空 2 分)
增大反应物接触面积,提高浸出速率,使反应充分进行
酸性
2 22
H O 2Fe2 2H 2Fe3 2H O
H2O2 在Fe3+ 催化下容易分解,故实际加入的H2O2 的量要高于理论量
pH 过高,会生成 Fe(OH)3 沉淀
LiFePO4+2H3PO4=Fe(H2PO4)2+LiH2PO4
1
2
3
4
5
6
7
8
9
10
11
12
13
14
15
C
D
D
D
C
D
D
B
B
A
C
B
B
D
A
18.( 15 分)
①长颈漏(2 分)
② B2KMnO4 +16HC1(浓)===2KCl+2MnCl2+5Cl2↑ +8H2O
=====
[ 或 CMnO2+4HCl(浓)△MnCl2+Cl2↑ +2H2O ]
(答出 B 或 C 得 1 分,答出对应方程式得 2 分,共 3 分,其他合理答案也给分)
③ d e d e c b f (2 分)
①防止Ⅰ中的水蒸气进入 G 的反应管中影响实验(2 分,其他合理答案也给分)
②澄清石灰水(2 分,其他合理答案也给分)
高温
③ 12 MgO + 11 C + 12 Cl2 =====
12 MgCl2 + 10 CO + CO2(2 分)
抑制 MgCl2 水解同时可带走水分 (2 分,各 1 分)
19.( 14 分,每空 2 分)
(1) 21
(2) 常温下自发进行,△G = △H - T△S< 0;该反应△S
相关试卷
这是一份四川省成都市成华区2025-2026学年高二上学期10月考试化学试卷,共10页。试卷主要包含了单项选择题,填空题等内容,欢迎下载使用。
这是一份四川省成都市成华区2025-2026学年高一上学期10月考试化学试卷,共9页。试卷主要包含了选择题等内容,欢迎下载使用。
这是一份四川省成都市成华区某校2024-2025学年高二上学期10月测试化学试卷(解析版),共19页。试卷主要包含了选择题,完成下列各题等内容,欢迎下载使用。
相关试卷 更多
- 1.电子资料成功下载后不支持退换,如发现资料有内容错误问题请联系客服,如若属实,我们会补偿您的损失
- 2.压缩包下载后请先用软件解压,再使用对应软件打开;软件版本较低时请及时更新
- 3.资料下载成功后可在60天以内免费重复下载
 免费领取教师福利
免费领取教师福利 









