




2025届高中化学全程复习构想课件全套53反应进程中溶液粒子浓度变化曲线
展开1. 能正确识别图像,能从图像中找到曲线指代、趋势、关键点。2.利用溶液中的平衡关系,学会分析不同类型图像中各粒子浓度之间的关系。
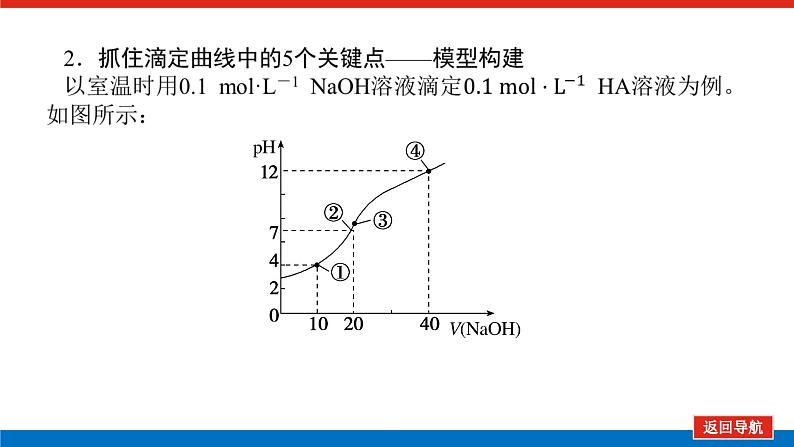
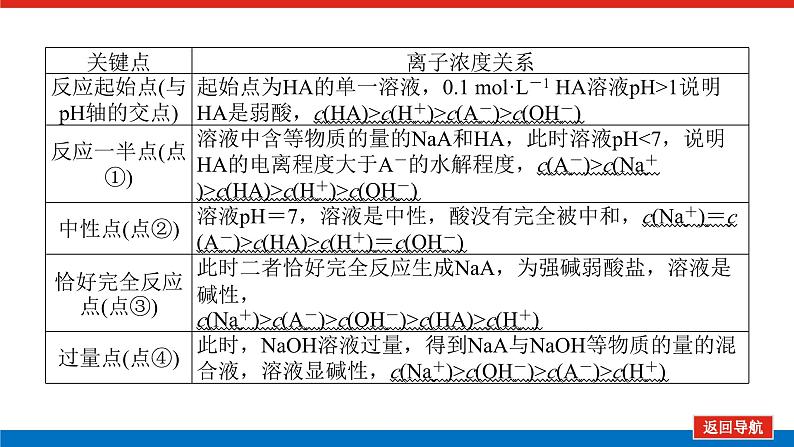
类型一 滴定曲线 1.巧抓“5点”,突破滴定曲线中粒子浓度关系(1)抓反应的“起始”点:判断酸、碱的相对强弱。(2)抓反应“一半”点,判断是什么溶质的等量混合。(3)抓“恰好”反应点,生成的溶质是什么,判断溶液的酸碱性。(4)抓溶液的“中性”点,生成什么溶质,哪种物质过量或不足。(5)抓反应的“过量”点,溶液中的溶质是什么,判断哪种物质过量。
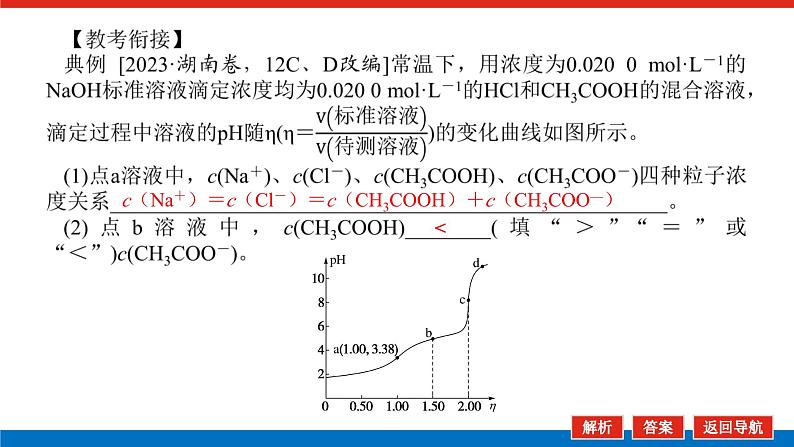
c(Na+)=c(Cl-)=c(CH3COOH)+c(CH3COO—)
解析:(1)a点溶液为等浓度的NaCl和CH3COOH混合溶液,存在物料守恒关系c(Na+)=c(Cl-)=c(CH3COOH)+c(CH3COO-)。(2)点b溶液中含有NaCl及等浓度的CH3COOH和 CH3COONa,由于pH<7溶液显酸性,说明CH3COOH的电离程度大于CH3COO-的水解程度,c(CH3COOH)
【对点演练】1.室温下,将1.00 ml·L-1盐酸滴入20.00 mL 1.00 ml·L-1的氨水中,溶液pH和温度随加入盐酸体积的变化曲线如图所示。
类型二 分布系数曲线1.透析分布曲线,锁定思维方向
2.明确解题要领,快速准确作答(1) 读“曲线”——每条曲线所代表的粒子及变化趋势;(2)“读浓度”——通过横坐标的垂线,可读出某pH时的粒子浓度;(3)“用交点”——交点是某两种粒子浓度相等的点,可计算电离常数K;(4)“可替换”——根据溶液中的元素质量守恒进行替换,分析得出结论。
下列说法正确的是( )A.当pH=1时,体系中c(H2L)>c([FeL]+)>c(OH-)>c(HL-)B.pH在9.5~10.5之间,含L的物种主要为L2-C.L2-+[FeL]+⇌[FeL2]-的平衡常数的lg K约为14D.当pH=10时,参与配位的c(L2-)≈1.0×10-3 ml·L-1
【师说·延伸】 本题主要涉及如下平衡体系:H2L⇌H++HL-、HL-⇌H++L2-、Fe3++L2-⇌[FeL]+、Fe3++2L2-⇌[FeL2]-、Fe3++3L2-⇌[FeL3]3-、Fe3++2L2-+OH-⇌[FeL2(OH)]2-。
2.常温下,向二元弱酸H2Y溶液中滴加NaOH溶液,所得混合溶液的pH与离子浓度变化的关系如图所示:
H2Y+OH-===H2O+HY-、HY-+OH-===H2O+Y2-
新高考化学一轮复习精品课件 第9章 第56讲 反应过程中溶液粒子浓度变化的图像分析 (含解析): 这是一份新高考化学一轮复习精品课件 第9章 第56讲 反应过程中溶液粒子浓度变化的图像分析 (含解析),共60页。PPT课件主要包含了内容索引,滴定过程pH变化曲线,必备知识,CH3COOH,CH3COONa,cNa+,NaOH,关键能力,分布系数曲线,真题演练明确考向等内容,欢迎下载使用。
2024年高考化学一轮复习课件(鲁科版)第8章 第50讲 反应过程中溶液粒子浓度变化的图像分析: 这是一份2024年高考化学一轮复习课件(鲁科版)第8章 第50讲 反应过程中溶液粒子浓度变化的图像分析,文件包含第8章第50讲反应过程中溶液粒子浓度变化的图像分析pptx、第8章第50练反应过程中溶液粒子浓度变化的图像分析docx、第8章第50讲反应过程中溶液粒子浓度变化的图像分析docx等3份课件配套教学资源,其中PPT共60页, 欢迎下载使用。
2024年高考化学一轮复习(新高考版) 第9章 第56讲 反应过程中溶液粒子浓度变化的图像分析: 这是一份2024年高考化学一轮复习(新高考版) 第9章 第56讲 反应过程中溶液粒子浓度变化的图像分析,文件包含2024年高考化学一轮复习新高考版第9章第56讲反应过程中溶液粒子浓度变化的图像分析pptx、2024年高考化学一轮复习新高考版第9章第56讲反应过程中溶液粒子浓度变化的图像分析docx、第9章第56讲反应过程中溶液粒子浓度变化的图像分析docx、第9章第56练反应过程中溶液粒子浓度变化的图像分析docx等4份课件配套教学资源,其中PPT共60页, 欢迎下载使用。












