



人教版 (2019)选择性必修3第二节 研究有机化合物的一般方法导学案
展开有机物的分离提纯
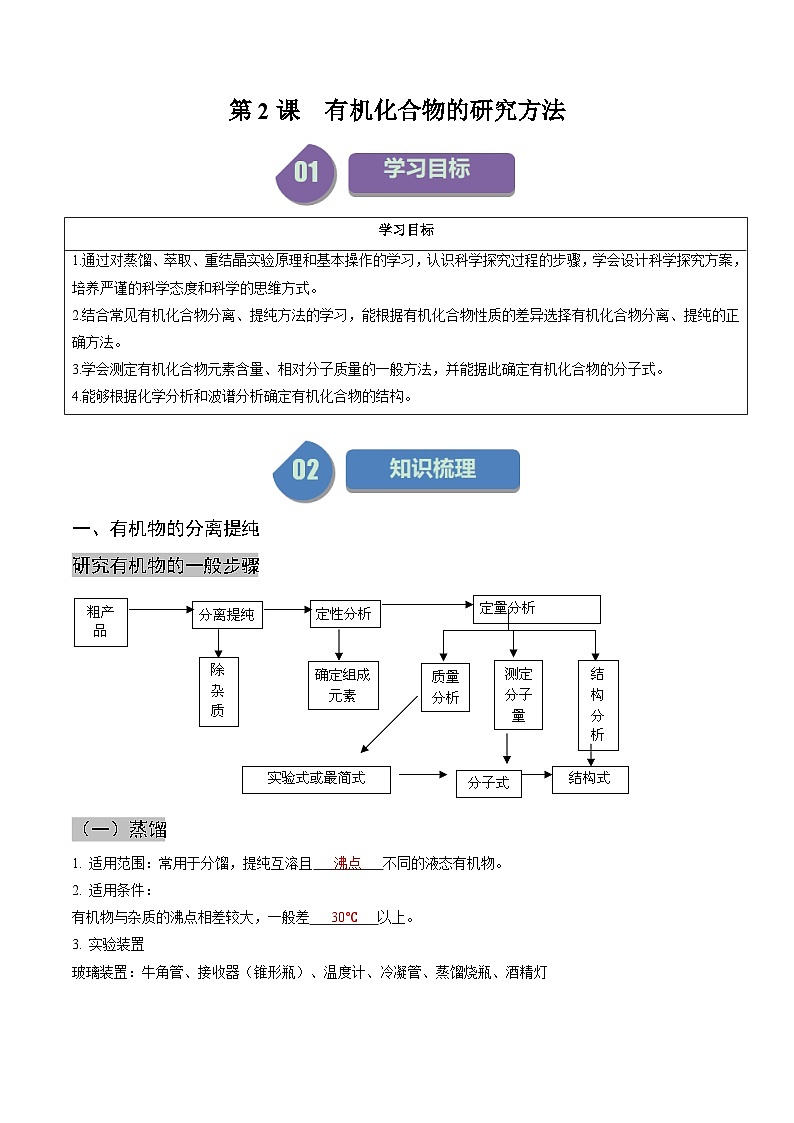
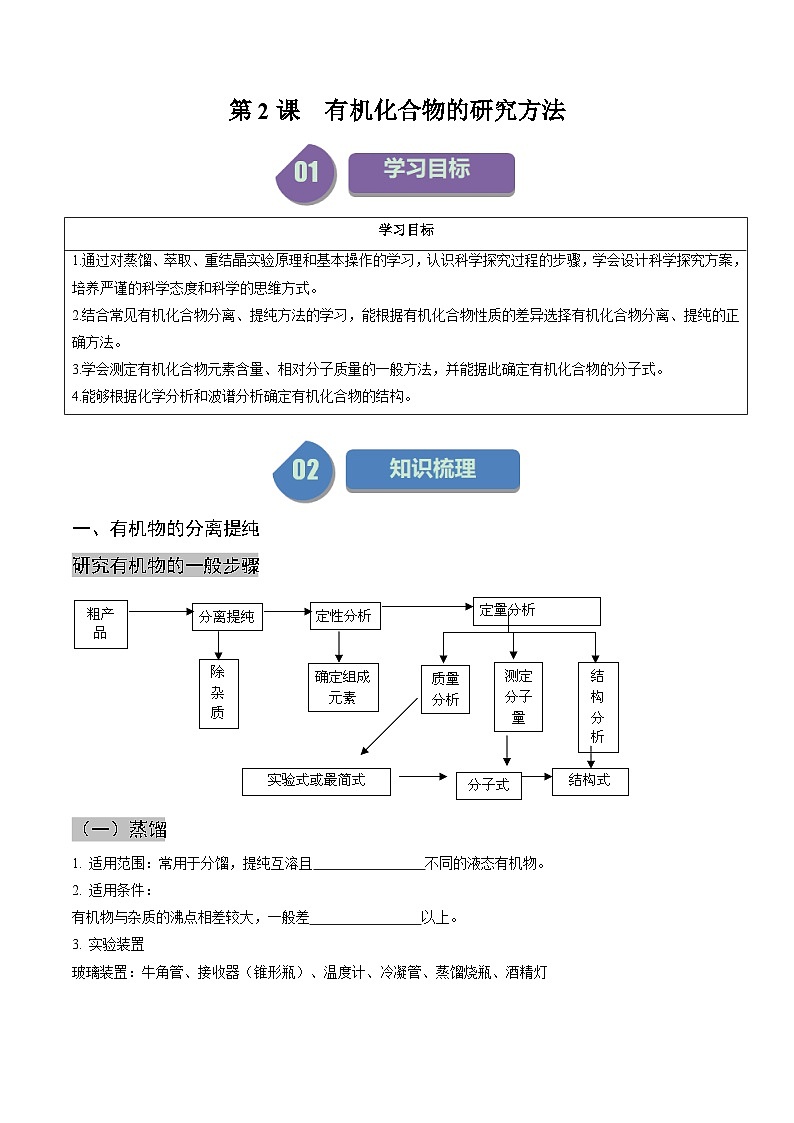
研究有机物的一般步骤
(一)蒸馏
1. 适用范围:常用于分馏,提纯互溶且 不同的液态有机物。
2. 适用条件:
有机物与杂质的沸点相差较大,一般差 以上。
实验装置
玻璃装置:牛角管、接收器(锥形瓶)、温度计、冷凝管、蒸馏烧瓶、酒精灯
注意事项
在蒸馏烧瓶中放少量碎瓷片或沸石,防止 。
温度计水银求的位置应与 相平。
冷凝管中冷却水从 进 , 出。
提问1:乙醇中混有水通过直接蒸馏的方式能否进行分离?
补充知识:
共沸是指两组分或多组分的液体混合物以特定比例组成时,在恒定压力下沸腾,其蒸气组成比例与溶液相同的现象。这实际是表明,此时沸腾产生的蒸气与液体本身有着完全相同的组成。
提问2:若想得到无水乙醇,应使用什么方法呢?
(二)分液与萃取
1. 分液
(1)适用范围:分离两种 的液体的操作方法。
(2)实验装置:分液使用的仪器是 ,另外还需要烧杯与铁架台进行辅助。
(3)注意事项:
①分液漏斗使用前要 ;
②分液时,先把下层液体从 放出,再把上层液体从 倒出。
常见有机物的密度特点
①CCl4、含溴的液态有机物、硝基苯密度一般大于水,在水的下层;
②液态的烃和酯的密度一般小于水,在水的上层。
萃取
萃取原理
液-液萃取是利用溶质在两种互不相容的溶剂里溶解能力的不同,用一种溶剂(萃取剂)将其从原溶剂中提取出来的方法。
萃取剂的要求
①萃取剂与原溶剂 ;
②溶质在萃取剂中的溶解度 在原溶剂中的溶解度;
③萃取剂与原溶液中的成分不反应。
常用萃取剂: 、 、 等。
萃取的过程:
如:从溴水中提取单质溴,需要先用CCl4萃取溴水中的溴,然后分液。
向100ml碘的饱和溶液中加入5ml 的苯,充分混合后静置,实验现象为
重结晶
实验原理:重结晶是提纯固体有机物常用的方法,是利用被提纯物质与杂质在同一溶剂中的溶解度不同而将杂质除去的方法。
溶剂的选择
①选用合适的溶剂,使得杂质在所选溶剂中溶解度 ,易于除去;
②被提纯的有机化合物在所选溶剂中的溶解度受温度的影响 ,能够进行 。
实验探究
重结晶法提纯苯甲酸,除去样品中少量的氯化钠和泥沙。
【操作】
【问题讨论】
①重结晶法提纯苯甲酸的原理是什么?有哪些主要操作步骤?
提示
②溶解粗苯甲酸时加热的作用是什么?趁热过滤的目的是什么?
提示
③实验操作中多次用到了玻璃棒,分别起到了哪些作用?
提示
④如何检验提纯后的苯甲酸中氯化钠已被除净?
提示
有机物分子组成确定
确定实验式
定性分析——确定有什么元素。
将某有机物在O2中充分燃烧后,各元素对应的燃烧产物
C - ; H -
定量分析——最简整数比
判断是否含有 。
碳元素的质量与氢元素质量之和等于有机物的质量则该物质中无氧元素。碳元素的质量与氢元素质量之和不等于有机物的质量则该物质中无氧元素。
方法:
①根据CO2的质量和H2O的质量分别求出C元素和氢元素的质量;剩下的即为氧的质量。
②求C与H的个数比,或C、H与O的个数比,确定最简式。
确定分子式
已知最简比,测分子相对质量即可得分子式
质谱法测相对质量
质谱仪——可以精确测定相对分子质量。
原理:用高能电子流轰击样品,使分子失去电子变成带正电荷得分子离子和碎片离子,在磁场得作用下,由于他们得相对质量不同而使其到达检测器的时间先后不同,其结果被记录为质谱图。
质谱图:以 为横坐标,以 为纵坐标,根据记录结果所建立的坐标图。
补充:
①质荷比:是指离子的相对质量与其电荷的比值。
②质谱图中,质荷比的最大值表示样品分子的相对分子质量。
有机物分子结构确定
红外光谱
利用红外光谱可以鉴别分子式相同,结构不同的有机物。
或者 在光谱图中显示出的吸收频率不同,因此在红外光谱图中可获得分子的化学键信息,进而推出官能团信息。
如分子式为C2H6O的有机物A有如下两种可能的结构: 或 ,利用红外光谱来测定,分子中有O—H(或—OH)可确定A的结构简式为 。
核磁共振氢谱
在有机物分子中, 。
补充:
①同C上的H为等效氢
②同C上相同基团上的H为等效氢
③对称位置上的H为等效氢
(1)原理
处于不同 中的氢原子因产生共振时吸收电磁波的频率不同,相应的信号在谱图中出现的位置不同,具有不同的 ,而且吸收峰的面积与 成正比,吸收峰的数目等于 。
(2)核磁共振氢谱图
如分子式为C2H6O的有机物A的核磁共振氢谱如图,可知A中有 种不同化学环境的氢原子且个数比为 ,可推知该有机物的结构简式应为 。
在核磁共振氢谱中:
等效氢的种类数=吸收峰数目
等效氢的个数比=吸收峰面积比
►问题一 物质分离提纯方法选择
【典例1】(2023上·江苏盐城·高二盐城市大丰区新丰中学校联考期中)为提纯下列物质(括号内的物质为杂质),所用除杂试剂和分离方法都正确的是
【变式1-1】(2023上·江苏无锡·高二无锡市市北高级中学校考期中)除去下列物质中所含少量杂质(括号内为杂质),所选用的试剂和分离方法正确的是
【变式1-2】(2023下·辽宁大连·高二大连八中校考阶段练习)为提纯下列物质(括号内的物质是杂质),所选用的除杂试剂和分离方法都正确的是
►问题二 分子组成确定
【典例2】(2023下·山西朔州·高二怀仁市第一中学校校联考期末·节选)根据以下有关信息确定有机物的组成:测定实验式:某含C、H、O三种元素的有机物,经燃烧实验测得其碳的质量分数为64.86%,氢的质量分数为13.51%,则其实验式是 。
【变式2-1】(2023下·上海青浦·高二上海市青浦高级中学校考期末·决选)常温常压下,某气态烃7.2克在足量氧气中完全燃烧,生成折合成状态下为,试回答下列问题:
根据上述数据,该气态烃的最简式(实验式)为 。
【变式2-2】(2023下·山西·高二忻州一中校联考阶段练习)根据要求,回答下列问题:
为了测定某有机物A的结构,进行如下实验:
a.将2.3g该有机物完全燃烧,生成和2.7g水;
b.用质谱仪测定其相对分子质量,得到如图所示的质谱图。
①有机物A的相对分子质量是 。
②有机物A的实验式是 。
►问题三 分子结构确定
【典例3】(2023下·广西桂林·高二统考期末)谱图是研究物质结构的重要手段之一,下列对各谱图的解析正确的是
【变式3-1】(2023下·河北保定·高二河北省唐县第一中学校考阶段练习)核磁共振(NMR)氢谱图上不是有3个吸收峰的是
A.2,5-二甲基-3-己烯B.1,4-二甲基环己烷
C.D.
【变式3-2】 (2023上·广东江门·高二江门市第一中学校考阶段练习)如图是一种分子式为C4H8O2的有机化合物的红外光谱图,则该有机化合物的结构简式
A.CH3CH2CH2COOHB.CH3COOCH2CH3
C.CH3CH(CH3)COOHD.HCOOCH(CH3)2
1.(2023上·宁夏石嘴山·高二平罗中学校考阶段练习)下列各组混合物分离或鉴别方法正确的是
A.用质谱仪鉴别乙酸和丙醇B.蒸馏法分离和水
C.用溴水鉴别苯和己烯D.分液法分离乙醇和水
2.(2023上·广西柳州·高二柳铁一中校考开学考试)科学家可以借助某些实验手段或仪器来测定化学物质的组成和空间结构,下列有关说法错误的是
A.质谱仪可以快速精确地测定有机物的相对分子质量
B.红外光谱仪可以用来测定分子的化学键和官能团
C.通过测定物质的熔点和沸点可以确定物质是否含有配位键
D.区别晶体和非晶体最可靠的科学方法是对固体进行X-射线衍射实验
3.(2023上·浙江·高三校联考阶段练习)下列说法不正确的是
A.苯甲酸重结晶过程中,加热、玻璃棒搅拌均能提高苯甲酸的溶解度
B.利用质谱仪可区分乙醇和二甲醚
C.研究有机物的一般步骤:分离、提纯→确定实验式→确定化学式→确定结构式
D.用苯萃取溴水时有机层应从上口倒出
4.(2023下·贵州黔西·高二统考期末)化学分析的手段通常有定性分析、定量分析、仪器分析等,现代化学中仪器分析是研究物质结构的基本方法和实验手段。下列仪器分析手段的运用科学可行的是
A.元素分析仪用于测定分子的空间结构
B.通过红外光谱分析、核磁共振氢谱分析均可以区分丙醇和乙酸
C.质谱仪是通过分析最小的碎片离子测出分子的相对质量
D.的核磁共振氢谱中有四组峰,峰面积之比为
5.(2023下·高二单元测试)将与样品分别送入以下仪器进行分析,能得到相同结果的是
①元素分析仪②质谱仪③红外光谱仪④核磁共振仪
A.①B.①②C.①②③D.①②③④
6.(2023上·甘肃兰州·高三兰州市第五十五中学校考开学考试)某有机物A用质谱仪测定如图1,核磁共振氢谱示意图如图2,则A的结构简式可能为
A.CH3CH2OHB.CH3CHOC.HCOOHD.CH3CH2CH2COOH
7.(2023下·广东湛江·高二湛江二十一中校考期中)2002年诺贝尔化学奖获得者的贡献之一是发明了对有机物分子进行结构分析的质谱法。其方法是让极少量的(10-9g)化合物通过质谱仪的离子化室使样品分子大量离子化,少量分子碎裂成更小的离子。如C2H6离子化后可得到C2H6+、C2H5+、C2H4+……,然后测定其质荷比。某有机物样品的质荷比如下图所示(假设离子均带一个单位正电荷,信号强度与该离子的多少有关),则该有机物可能是( )
A.甲醇B.丙烷C.甲烷D.乙烯
8.(2023上·云南红河·高二蒙自一中校考期中)为了提纯下表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是
9.(2023下·河北邯郸·高二武安市第三中学校考阶段练习)青蒿素为无色针状晶体,熔点为156~157℃,易溶于丙酮、氯仿和苯,在水中几乎不溶。
Ⅰ.实验室用乙醚提取青蒿素的工艺流程如图所示。
(1)在操作i前要对青蒿进行粉碎,其目的是 。
(2)操作ii的名称是 。
(3)操作iii涉及重结晶,则操作iii的步骤为加热溶解、 、过滤、洗涤、干燥。
Ⅱ.已知青蒿素是一种烃的含氧衍生物,某同学为确定其化学式,进行如图实验:
实验步骤:
①按图所示连接装置,检查装置的气密性;
②称量装置E、F中仪器及试剂的质量;
③取14.10g青蒿素放入硬质玻璃管C中,点燃装置C、D处的酒精灯;
④实验结束后冷却至室温,称量装置E、F中仪器及试剂的质量。
(4)装置E、F应装入的试剂分别为 、 。
(5)实验测得数据如表:
通过质谱仪测得青蒿素的相对分子质量为282,结合上述数据,得出青蒿素的分子式为 。
(6)某同学认为使用上述方法会产生较大实验误差,你的改进方法是 。
【点睛】利用空气提供O2或排尽装置内的气体时,需防止空气中某些成分对实验结果产生影响。
10.(2023上·云南红河·高二开远市第一中学校校考开学考试)Ⅰ.为测定某有机化合物A的结构,进行如下实验:
第一步,分子式的确定。
(1)将有机物A置于氧气流中充分燃烧,实验测得:生成5.4 g H2O和8.8 g CO2,消耗氧气6.72 L(标准状况下),则该有机物的实验式是 。
(2)用质谱仪测定该有机化合物的相对分子质量,得到如图①所示质谱图,则其相对分子质量为 ,该物质的分子式是 。
第二步,结构简式的确定。
(3)根据价键理论,预测A的可能结构并写出结构简式: (写出一种)。
(4)经测定,有机物A的核磁共振氢谱如图②所示,则A的结构简式为
Ⅱ.现有某烃W的键线式为。
(5)W的分子式为 。
(6)W的一氯代物有 种。
(7)写出W的芳香族同分异构体(能发生聚合反应)的结构简式: ,写出该聚合反应的化学方程式: 。
1.(2023下·山东·高二校联考阶段练习)下列研究有机物的方法错误的是
A.分离提纯有机物的常用方法是燃烧法
B.2,2,6,6—四甲基庚烷的核磁共振碳谱中出现了3个峰
C.图为某有机物的质谱图,可推知该有机物的相对分子质量为90
D.利用X射线衍射技术可以区分有机物的对映异构体
2.(2023下·云南楚雄·高二统考期末)下列有关有机化合物的研究方法、结构特点及性质的说法正确的是
A.利用红外光谱可以确定有机物的相对分子质量
B.向蛋白质溶液中加入硫酸铵溶液,蛋白质的性质和生理功能会发生改变
C.研究有机物的基本步骤:分离、提纯→确定实验式→确定分子式→确定分子结构
D.实验室通常利用电石和水制备乙炔,并用氯化钠溶液除去乙炔中混有的等杂质气体
3.(2024·全国·高二假期作业)下列关于物质的分离、提纯实验中的一些操作或做法,正确的是
A.在组装蒸馏装置时,温度计的水银球应伸入液面下
B.用96%的工业酒精制取无水乙醇,可采用直接蒸馏的方法
C.在苯甲酸重结晶实验中,粗苯甲酸加热溶解后还要加少量蒸馏水
D.在苯甲酸重结晶实验中,待粗苯甲酸完全溶解后,要冷却到常温才过滤
4.(2024·全国·高二假期作业)下列有关图所示实验的叙述正确的是
A.用装置①来分离苯和溴苯的混合物
B.用装置②蒸馏工业乙醇可得到无水乙醇
C.重结晶提纯苯甲酸过程中要用到装置③进行分离操作
D.装置④为蒸发结晶装置,实验者用玻璃棒不断搅拌溶液,以促进液体挥发,烧杯底部垫上石棉网,能让容器受热更加均匀
5.(河北邢台·高二期中)除去下列物质中所含的少量杂质(括号内为杂质),所选用的试剂和分离方法能达到实验目的的是( )
6.(甘肃天水·高二统考期中)下列各组物质除杂和分离方法正确的是
7.(2024·全国·高二假期作业)选择下列实验方法分离提纯物质,将分离提纯方法的字母序号填在横线上。
A.萃取分液 B.升华 C.重结晶 D.分液 E.蒸馏 F.过滤 G.洗气
(1) 分离氯化钾与固体碘的混合物。
(2) 提纯含有泥沙的苯甲酸固体。
(3) 分离水和CCl4的混合物。
(4) 分离石油中的各组分。
(5) 除去混在甲烷中的乙烯。
(6) 提取溴水中的溴。
8.(2024·全国·高二假期作业)苯甲醇与苯甲酸都是常见化工原料,在化工生产中有广泛应用。工业上常在碱性条件下由苯甲醛来制备。某实验室模拟其生产过程,实验原理、实验方法及步骤如下:
实验原理:
有关资料:
苯甲醛在空气中极易被氧化,生成白色苯甲酸。
实验步骤及方法如下:
I.向盛有足量溶液的反应器中分批加入新蒸过的苯甲醛,持续搅拌至反应混合物变成白色蜡糊状A,转移至锥形瓶中静置24小时以上。
反应装置如图1:
II.步骤I所得产物后续处理如图2:
(1)仪器a的名称为 。
(2)步骤I中苯甲醛需要分批加入且适时冷却,其原因是 。
(3)为获取产品1,将乙醚萃取液依次用饱和亚硫酸氢钠溶液、10%碳酸钠溶液和水进行洗涤并分液。乙醚萃取液的密度小于水,取分液后 (填“上”或“下”)层液体加入无水,其作用为 ,操作①含多步操作,其中最后一步分离操作是对乙醚和产品1进行分离,其名称为 。
(4)水层中加入浓盐酸发生反应的离子方程式为 。
(5)操作②包含溶解、蒸发浓缩、结晶、晾干,下列仪器中在该操作中不需要用到的有____(填序号)。
A.分液漏斗B.蒸发皿C.研钵D.玻璃棒
(6)①若产品2产率比预期值稍高,可能原因是 。
A.操作②未彻底晾干 B.产品中混有其他杂质
C.过滤时滤液浑浊 D.部分苯甲醛被直接氧化为苯甲酸
②产品2经干燥后称量,质量为6.1g,计算其产率为 (保留3位有效数字,写出计算过程)。
9.(2023下·福建龙岩·高二福建省龙岩第一中学校联考阶段练习)化学上研究有机化合物一般先进行分离提纯,再测定有机物的组成和结构。
Ⅰ.按以下实验方案可从海洋动物柄海鞘中提取具有抗肿瘤活性的天然产物。
(1)操作(1)(2)(3)(4)对应仪器分别是 。
Ⅱ.有机物M具有特殊香味。某化学兴趣小组从粗品中分离提纯有机物M,然后借助李比希法、现代科学仪器测定有机物M的分子组成和结构,具体实验过程如下:
步骤一:将粗品用蒸馏法进行纯化。
(2)如图1所示,图中虚线框内仪器应选用 (填“仪器x”或“仪器y”),仪器a的名称是 。
步骤二:确定M的实验式和分子式。
(3)利用元素分析仪测得有机物M中碳的质量分数为54.5%,氢的质量分数为9.1%。
①M实验式为 。
②已知M的密度是同温同压下密度的2倍,则M的分子式为 。
步骤三:确定M的结构简式。
(4)用核磁共振仪测出M的核磁共振氢谱如图2所示,图中峰面积之比为1:3:1:3;利用红外光谱仪测得M的红外光谱如图3所示。
①M的结构简式为 。
②M的所有同分异构体在下列一种表征仪器中显示的信号(或数据)完全相同,该仪器是 (填标号)
a.质谱仪 b.红外光谱仪 c.元素分析仪 d.X射线衍射仪
10.(北京海淀·高二北大附中校考期中)茶叶中含有丰富的有机物,通过不同提取方法可以获得不同的有机物成分。
I.从茶叶中提取咖啡因的主要流程如下:
资料:咖啡因能溶于乙醇等溶剂,120℃升华显著,熔点为238℃
(1)第①步使用乙醇提取咖啡因的原因是 。
(2)步骤②使用的装置是 (填序号)。
(3)上述步骤中主要利用化学变化进行物质分离的是 (填数字序号)。
(4)由液相色谱法从茶叶中可以分离得到B,为确定B的结构,进行如下实验:
综上所述,B的结构简式是 。
学习目标
1.通过对蒸馏、萃取、重结晶实验原理和基本操作的学习,认识科学探究过程的步骤,学会设计科学探究方案,培养严谨的科学态度和科学的思维方式。
2.结合常见有机化合物分离、提纯方法的学习,能根据有机化合物性质的差异选择有机化合物分离、提纯的正确方法。
3.学会测定有机化合物元素含量、相对分子质量的一般方法,并能据此确定有机化合物的分子式。
4.能够根据化学分析和波谱分析确定有机化合物的结构。
A
B
C
D
物质
乙醇(水)
苯(甲苯)
乙烷(乙烯)
溴苯(液溴)
除杂试剂
生石灰
酸性溶液
酸性溶液
苯
分离方法
蒸馏
分液
洗气
分液
混合物
试剂
分离方法
A
乙酸乙酯(乙酸)
NaOH溶液
分液
B
乙烷(乙烯)
氢气
加热
C
乙醇(水)
生石灰
蒸馏
D
苯(甲苯)
蒸馏水
分液
选项
被提纯的物质
除杂试剂及分离方法
A
乙酸乙酯(乙酸)
饱和碳酸钠溶液,蒸馏
B
苯(苯酚)
浓溴水,过滤
C
乙醇(乙酸)
CaO,蒸馏
D
苯(甲苯)
KMnO4溶液,分液
A.可能是原子核外电子从基态跃迁至激发态时的光谱图
B.可能是的质谱图
C.可能是的红外光谱图
D.可能是的核磁共振氢谱图
选项
被提纯的物质
除杂试剂
分离方法
A
己烷(己烯)
溴水
分液
B
溴苯(苯)
水
分液
C
苯(苯酚)
NaOH溶液
分液
D
甲烷(乙烯)
酸性溶液
洗气
装置
实验前
实验后
E
24.00g
33.90g
F
100.00g
133.00g
选项
混合物
试剂
分离方法
A
溴苯(溴)
溶液
分液
B
乙醇(水)
过滤
C
甲烷(乙烯)
酸性高锰酸钾溶液
洗气
D
乙酸乙酯(乙酸)
溶液
分液
被提纯物质
除杂试剂
分离方法
A
苯(苯甲酸)
生石灰
蒸馏
B
乙酸乙酯(乙酸)
氢氧化钠溶液
分液
C
乙烷(乙烯)
酸性高锰酸钾溶液
洗气
D
苯(苯酚)
浓溴水
过滤
名称
相对分子质量
熔点(℃)
沸点(℃)
溶解性
水
醇
醚
苯甲醛
106
179.62
微溶
易溶
易溶
苯甲酸
122
122.13
249
微溶
易溶
易溶
苯甲醇
108
205.7
微溶
易溶
易溶
乙醚
74
34.6
微溶
易溶
——
实验步骤
解释或实验结论
①取适量B用质谱仪确定相对分子质量
B的相对分子质量212
②将此2.12gB在足量纯O2中充分燃烧,使其产物依次缓缓通过浓硫酸,碱石灰,计算发现生成0.06ml H2O和0.10mlCO2
B的分子式为
③B能使FeCl3溶液变紫色,另取2.12gB与足量NaOH溶液反应,最多消耗0.04mlNaOH,且产物之一是1-丙醇
B中含有的官能团有: 、
④B的核磁共振氢谱有6组信号峰且峰面积比为1:2:2:2:2:3,且环上有3个相同的取代基位于相邻位置。
B中含 种氢原子
人教版 (2019)第一节 合成高分子的基本方法优秀学案: 这是一份人教版 (2019)<a href="/hx/tb_c4002483_t4/?tag_id=42" target="_blank">第一节 合成高分子的基本方法优秀学案</a>,文件包含第25讲合成高分子的基本方法教师版-2024年高中化学同步精品讲义选择性必修三docx、第25讲合成高分子的基本方法学生版-2024年高中化学同步精品讲义选择性必修三docx等2份学案配套教学资源,其中学案共27页, 欢迎下载使用。
高中化学人教版 (2019)选择性必修3第三节 核酸优质学案: 这是一份高中化学人教版 (2019)选择性必修3<a href="/hx/tb_c4002479_t4/?tag_id=42" target="_blank">第三节 核酸优质学案</a>,文件包含第23讲核酸教师版-2024年高中化学同步精品讲义选择性必修三docx、第23讲核酸学生版-2024年高中化学同步精品讲义选择性必修三docx等2份学案配套教学资源,其中学案共21页, 欢迎下载使用。
选择性必修3第二节 蛋白质精品导学案: 这是一份选择性必修3<a href="/hx/tb_c4002478_t4/?tag_id=42" target="_blank">第二节 蛋白质精品导学案</a>,文件包含第22讲蛋白质教师版-2024年高中化学同步精品讲义选择性必修三docx、第22讲蛋白质学生版-2024年高中化学同步精品讲义选择性必修三docx等2份学案配套教学资源,其中学案共31页, 欢迎下载使用。













