

黑龙江省哈尔滨市第九中学校2023-2024学年高一下学期4月学业阶段性评价考试化学试题(无答案)
展开可能用到的相对原子质量:
第I卷(共45分)
一、选择题(共15小题,每小题3分,每小题只有一个选项符合题意)
1.下列有关说法正确的是
A.水泥、玻璃、水晶饰物都是硅酸盐制品B.石灰石是制造玻璃和水泥的主要原料之一
C.闻名世界的秦兵马俑是陶制品,由黏土经高温烧结而成,烧制的过程为物理变化
D.晶体硅的导电性介于导体和绝缘体之间,常用于制造光导纤维
2.下列说法正确的是
A.玻璃钢和压电陶瓷都属于新型无机非金属材料
B.燃煤中加入可以减少酸雨的形成及温室气体的排放
C.二氧化硫可用于杀菌消毒,还是一种食品添加剂
D.植物直接吸收利用空气中的和作为肥料,实现氮的固定
3.是阿伏加德罗常数的值,下列说法正确的是
A.与一定量的稀硝酸反应,转移电子数目一定为
B.沸腾炉中被完全氧化,转移电子的数目为
C.粉与足量S粉加热充分反应转移的电子数为
D.标准状况下,和混合后分子总数为
4.下列指定反应的离子方程式正确的是
A.用从酸化的海带灰浸出液中制取碘:
B.将少量通入溶液中;
C.向硫化钠溶液通入足量二氧化硫:
D.氯化铜溶液中通入硫化氢:
5.一定条件下,下列选项所示的物质间转化均能实现是
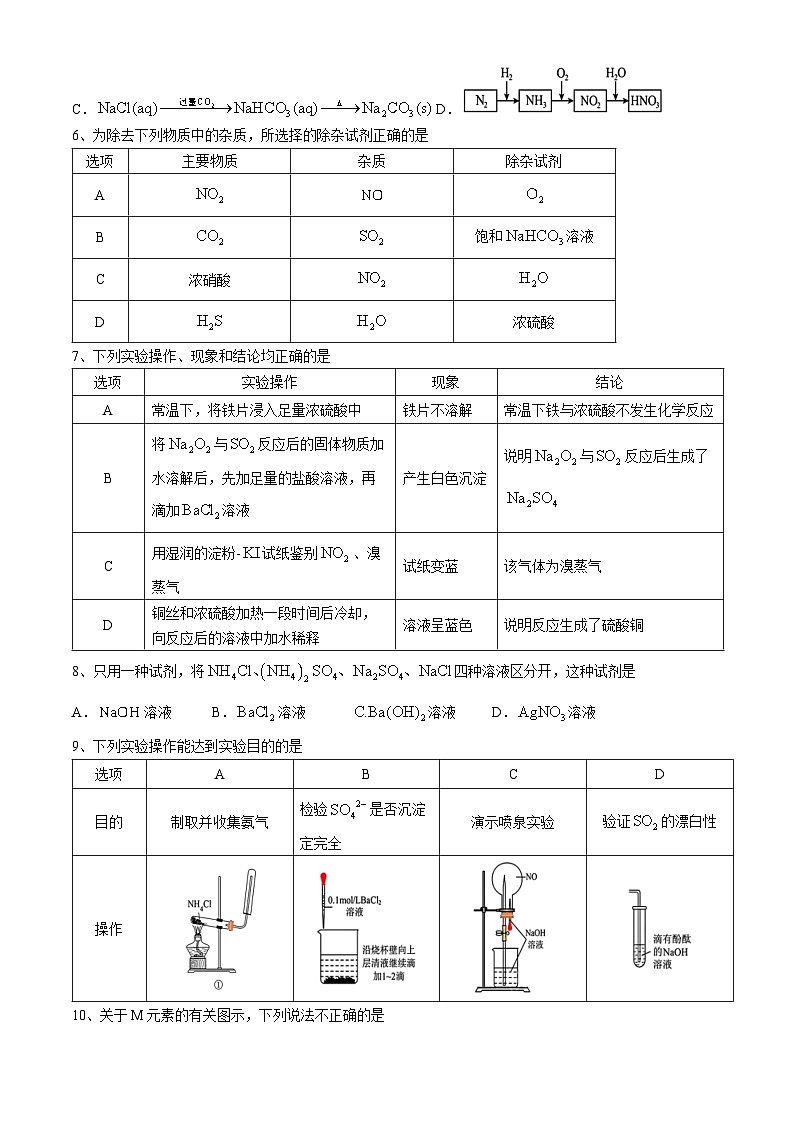
A.
C.D.
6、为除去下列物质中的杂质,所选择的除杂试剂正确的是
7、下列实验操作、现象和结论均正确的是
8、只用一种试剂,将四种溶液区分开,这种试剂是
A.溶液B.溶液溶液D.溶液
9、下列实验操作能达到实验目的的是
10、关于M元素的有关图示,下列说法不正确的是
A.依据题给价一类二维图综合分析可知元素为氮元素.
B.物质B可用作火箭燃料,其电子式为
C.D或均可在一定条件下与反应得到C
D.物质F的浓溶液具有强氧化性,可以用铁制或铝制容器盛放
11、和的混合气体通入倒立在水槽中盛满水的玻璃筒(带刻度)中,充分反应后,筒内剩余气体,则原混合气体中与的体积比可能为
A.12:1B.9:1C.6:1D.3:1
12、实验室用还原(沸点:)制备高纯硅的装置如图所示(夹持装置和尾气处理装置略去),下列说法正确的是
A.装置Ⅱ、Ⅲ中依次盛装的是浓、冰水B.实验时,应先加热管式炉,再打开活塞
C.为鉴定制得的硅中是否含微量铁单质,需要用到的试剂为盐酸、双氧水、硫氰化钾溶液
D.该实验中制备氢气的装置也可用于稀氢氧化钠溶液与氯化铵固体反应制备氨
13、某同学做“被氧化”的实验,发现溶液变为深棕色.猜想可能是生成的或与或反应,使溶液变为深棕色,设计下列装置探究.下列说法错误的是
A.先检查装置气密性,加入药品后,关闭,打开和,再通入一段时间
B.关闭,打开及分液漏斗活塞,反应后丙中溶液变为深棕色,丁中溶液无明显变化,证明与反应
C.甲中反应一段时间后,更新丙、丁中试剂,关闭和,打开,反应后丙中溶液变为深棕色,丁中溶液无明显变化,证明也可与反应
D.该实验的缺陷是缺少尾气处理装置
14、在中学常见的物质中,选择合适的物质和条件按以下流程进行转化。
下列表格中所选的物质或试剂(所需条件已略去),不能完全满足以上转化流程的是
15、向含和的混合稀溶液中缓慢加入铁粉,其氧化产物与所加铁粉的物质的量关系如图所示,下列有关说法正确的是
A.B.点之前反应的离子方程式为
C.向b点所得溶液中加入粉,最多可溶解
D.反应至点,可收集到气体(标准状况)
Ⅱ卷(非选择题,共55分)
16、(10分)按要求回答下列问题
(1)工业上制硫酸时接触室中反应的化学方程式:______
(2)能使氯水褪色,写出反应的离子方程式:______
(3)与水反应的化学方程式:______
(4)用化学方程式解释久置浓硝酸呈黄色的原因:______
(5)用离子方程式表示向溶液中滴入稀硫酸,溶液变为黄色的原因:______
17、(15分)如图是无机物在一定条件下的转化关系(部分产物及反应条件未标出)。
已知:为气体,都含有相同的元素。
试回答下列问题。
(1)写出下列物质的化学式:C______、F______。
(2)写出实验室制物质B的化学反应方程式:______,干燥B可用的干燥剂为______(填试剂名称),尾气吸收可选用______装置(填序号)。
(3)标准状况下,若将和的混合气体充满容积为的试管后倒扣在水中。
①假设气体不扩散,最终试管中所得溶液的物质的量浓度为______。
②为了消除的污染,可将它与在催化剂作用下反应,生成水和一种无污染物质,该反应的化学方程式是______。
③描述检验中阳离子的操作:______。
(4)工业上可用①②③由B制取E,为了提高原料的利用率并尽量减轻对环境的污染,C必须循环使用.若消耗的制取,在该过程中至少消耗的的物质的量为______。
18、(16分)亚硝酸钠广泛用于工业、建筑业及食品加工业.某课外活动小组的同学拟制备亚硝酸钠、测定其产品的纯度并验证亚硝酸钠的某些性质。
(1)甲组同学采用下图装置制取亚硝酸钠。
①仪器M的名称是______。
②A中用的硫酸而不用稀硫酸的原因是______。
③若通入装置中的与按物质的量之比1:1被溶液完全吸收,反应过程中无气体生成,则装置中发生反应的化学方程式为______。
(2)乙组同学测定甲组制得的产品中的纯度。称取试样于锥形瓶中,加入适量水溶解,与的酸性溶液恰好完全反应,则产品的纯度为______(用含c、m、V的代数式表示)。
(3)现用下图所示仪器(夹持装置已省略)及药品,探究亚硝酸钠与硫酸反应气体产物的成分。已知:气体液化的温度为为
①为了检验装置中生成的气体产物,仪器的连接顺序(按左右连接)为、______、______、______。
②装置的作用是______。
③滴入硫酸后,观察到A中有红棕色气体产生。依据______的现象,确定该气体中还有NO。
④通过上述实验探究过程,可得出装置A中反应的化学方程式是______。
19、(14分)工业上以高硫铝土矿(主要成分为及其它不溶性物质)为原料,冶炼铝和铜并制得绿矾的工艺流程如图:
(1)铝土矿焙烧前研磨粉碎的目的是______。
(2)焙烧Ⅱ过程中产生的污染性气体是______(填化学式),大量排放该气体造成的主要环境问题是______。
(3)滤渣A中除其它不溶性物质外还有:______。
(4)反应②的离子方程式为:______。
(5)操作包括______、过滤、洗涤、干燥等操作。
(6)向溶液A中少量多次加入还原性铁粉,当看到______现象时停止加入铁粉,原因是______。选项
主要物质
杂质
除杂试剂
A
B
饱和溶液
C
浓硝酸
D
浓硫酸
选项
实验操作
现象
结论
A
常温下,将铁片浸入足量浓硫酸中
铁片不溶解
常温下铁与浓硫酸不发生化学反应
B
将与反应后的固体物质加水溶解后,先加足量的盐酸溶液,再滴加溶液
产生白色沉淀
说明与反应后生成了
C
用湿润的淀粉-试纸鉴别、溴蒸气
试纸变蓝
该气体为溴蒸气
D
铜丝和浓硫酸加热一段时间后冷却,向反应后的溶液中加水稀释
溶液呈蓝色
说明反应生成了硫酸铜
选项
A
B
C
D
目的
制取并收集氨气
检验是否沉淀定完全
演示喷泉实验
验证的漂白性
操作
选项
X
试剂1
试剂2
A
B
C
D
稀盐酸
20,黑龙江省哈尔滨市第九中学校2023-2024学年高三下学期开学考试化学试题: 这是一份20,黑龙江省哈尔滨市第九中学校2023-2024学年高三下学期开学考试化学试题,共11页。试卷主要包含了单项选择题,填空题等内容,欢迎下载使用。
黑龙江省哈尔滨市第九中学校2023-2024学年高三下学期开学考试化学试题: 这是一份黑龙江省哈尔滨市第九中学校2023-2024学年高三下学期开学考试化学试题,共6页。
黑龙江省哈尔滨市第九中学校2023-2024学年高三下学期开学考试化学试题: 这是一份黑龙江省哈尔滨市第九中学校2023-2024学年高三下学期开学考试化学试题,共8页。












