









沪科技版(2020)必修第二册乙酸试讲课课件ppt
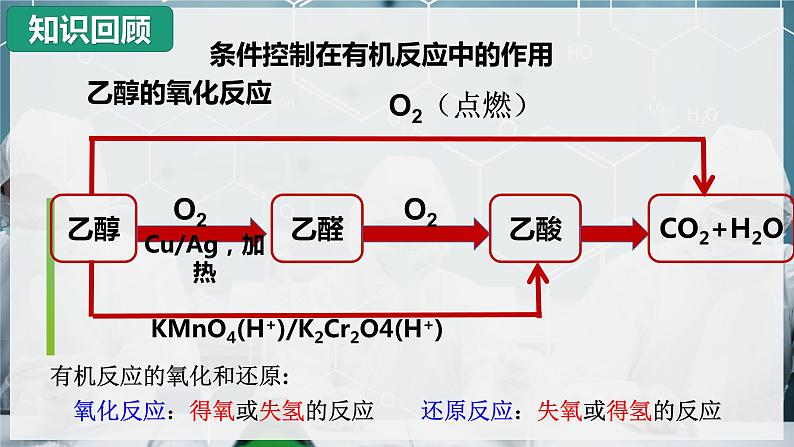
展开条件控制在有机反应中的作用
有机反应的氧化和还原: 氧化反应:得氧或失氢的反应 还原反应:失氧或得氢的反应
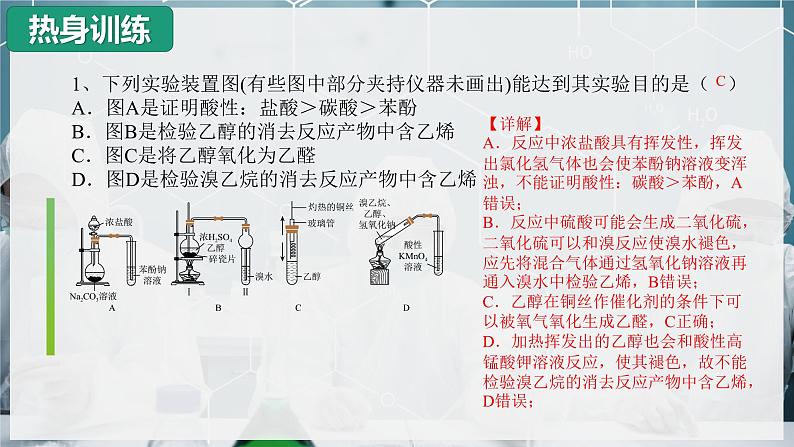
1、下列实验装置图(有些图中部分夹持仪器未画出)能达到其实验目的是( )A.图A是证明酸性:盐酸>碳酸>苯酚B.图B是检验乙醇的消去反应产物中含乙烯C.图C是将乙醇氧化为乙醛D.图D是检验溴乙烷的消去反应产物中含乙烯
【详解】A.反应中浓盐酸具有挥发性,挥发出氯化氢气体也会使苯酚钠溶液变浑浊,不能证明酸性:碳酸>苯酚,A错误;B.反应中硫酸可能会生成二氧化硫,二氧化硫可以和溴反应使溴水褪色,应先将混合气体通过氢氧化钠溶液再通入溴水中检验乙烯,B错误;C.乙醇在铜丝作催化剂的条件下可以被氧气氧化生成乙醛,C正确;D.加热挥发出的乙醇也会和酸性高锰酸钾溶液反应,使其褪色,故不能检验溴乙烷的消去反应产物中含乙烯,D错误;
1、了解乙酸的分子结构及物理性质2、理解乙酸的化学性质3、知道官能团、烃的衍生物的概念,了解羟基、羧基等官能团与性质的关系
古代山西省有个酿酒高手叫杜康。他儿子黑塔跟父亲也学会了酿酒技术。后来,从山西迁到镇江。黑塔觉得酿酒后把酒糟扔掉可惜,把酒糟浸泡在水缸里。到了第二十一日的酉时,一开缸,一股浓郁的香气扑鼻而来。黑塔忍不住尝了一口,酸酸的,味道很美。烧菜时放了一些,味道特别鲜美,便贮藏着作为“调味酱”。故醋在古代又叫“苦酒”。
知识点一:乙酸的物理性质
1、下列关于乙酸的说法不正确的是( )A.乙酸是一种重要的有机酸,是具有强烈刺激性气味的液体B.乙酸分子中含有四个氢原子,所以乙酸是四元酸C.无水乙酸又称冰醋酸,它是纯净物D.乙酸易溶于水和乙醇
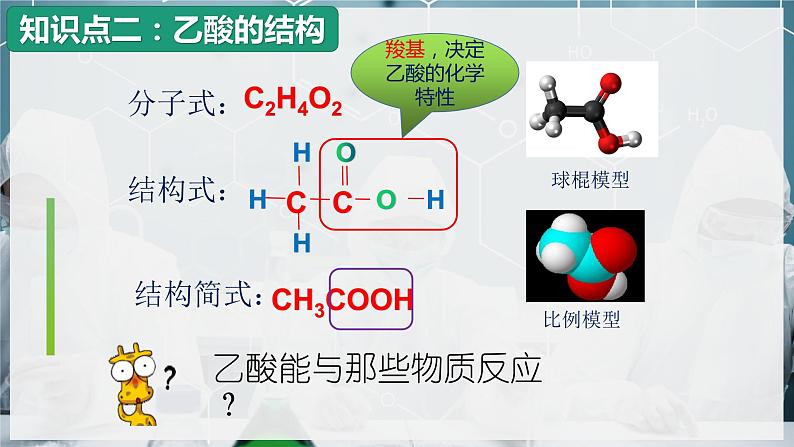
乙酸能与那些物质反应?
羧基,决定乙酸的化学特性
知识点三:乙酸的化学性质
具有酸的通性:即可与酸碱指示剂作用,与活泼金属,与碱及碱性氧化物,部分盐反应
Na2CO3+2CH3COOH →2CH3COONa+CO2↑+H2O
【酸性强弱】CH3COOH>H2CO3
Mg+2CH3COOH →(CH3COO)2Mg+H2↑
NaOH+CH3COOH →CH3COONa+H2O
乙酸、乙醇、碳酸、水分子中羟基氢的活动性比较
与Na反应时,物质的量的关系为与NaOH反应时,物质的量的关系为 与Na2CO3反应时,物质的量的关系为 与NaHCO3反应时,物质的量的关系为
2Na~2-COOH~H2
Na2CO3~2-COOH~CO2
NaHCO3~-COOH~CO2
羧基(-COOH)参与反应时量的关系
在有机化学中能和NaHCO3反应只有羧基( —COOH)
向试管中依次加入:乙醇、浓硫酸、乙酸
乙醇、乙酸、浓硫酸、饱和Na2CO3溶液
饱和Na2CO3溶液的作用:
1)由于乙酸乙酯的沸点比乙酸、乙醇都低, 因此从反应物中不断蒸出乙酸乙酯可提高其产率。
2)使用过量的乙醇,可提高乙酸转化为乙酸乙酯的产率。
根据化学平衡原理,提高乙酸乙酯产率的措施有:
3)使用浓H2SO4作吸水剂,提高乙醇、乙酸的转化率。
现象:饱和Na2CO3溶液的液面上有透明的油状液体生成,且能闻到香味
导管在饱和Na2CO3液面上:防止倒吸
加物顺序:乙醇→浓硫酸→乙酸
①溶解乙醇;②中和乙酸;③降低乙酸乙酯的溶解度,利于酯的析出
浓硫酸:催化剂、吸水剂
沸点:乙酸乙酯(77.1)乙醇(78.3 ℃ )乙酸(118℃)
化学特性:与金属钠反应、催化氧化反应、酯化反应……
化学特性:酸性、酯化反应……
化学特性:加成、氧化反应……
1.酯 羧酸分子羧基中的 —OH 被-OR'取代后的产物称为酯,简写为RCOOR',结构式为 R—C—O—R' 官能团为 酯基 —C—O— 2.物理性质低级酯密度比水小 ,难溶于水,易溶于有机溶剂,具有芳香气味。3.用途 (1)用作香料,例如 饮料、糖果、化妆品中的香料 (2)用作溶剂,例如 指甲油、胶水的溶剂
1.实验室制备乙酸乙酯和乙酸乙酯提纯的装置和操作流程图如下,下列叙述不正确的是( )A.无水碳酸钠在流程中做吸水剂B.操作①为分液C.向试管中先加入浓硫酸,然后边振荡试管边慢慢加入乙醇,再加入冰醋酸D.试管b中饱和 溶液的作用是吸收蒸出的少量乙酸和乙醇,减小乙酸乙酯的溶解
【详解】A.A是乙酸乙酯,乙酸乙酯中有水分,因此无水碳酸钠在流程中做吸水剂,起干燥作用,故A正确;B.b中是不相溶的两种液体分离,因此操作①为分液,故B正确;C.向试管中先加入乙醇,然后边振荡试管边慢慢加入浓硫酸,冷却后再加入冰醋酸,故C错误;D.试管b中饱和 溶液的作用是吸收蒸出的少量乙酸,溶解乙醇,降低乙酸乙酯溶解度,减小乙酸乙酯的溶解,故D正确。综上所述,答案为C。
知识点四:常见官能团及其代表物的主要反应
1.下列物质中含有2种官能团的是( )A.乳酸( ) B.苯乙烯( )C.丙三醇( ) D.甲苯( )
【解析】A.乳酸中含有羟基-OH和羧基-COOH 2种官能团,A正确;B.苯乙烯中含有碳碳双键 1种官能团,B错误;C.丙三醇中含有羟基-OH 1种官能团,C错误;D.甲苯中没有官能团,D错误。
1、下列说法正确的是( )①乙酸的官能团是羟基 ②可用紫色石蕊溶液鉴别乙醇和乙酸 ③乙酸的酸性比碳酸强,可用食醋除去水壶中的水垢 ④制取乙酸乙酯时,适当增大乙醇的浓度,可使乙酸完全反应A.①③④B.②③C.①④D.②③④
【解析】①乙酸的官能团是羧基,故错误;②乙酸具有弱酸性,能使紫色石蕊溶液变红,而乙醇无现象,可鉴别乙醇和乙酸,故正确;③乙酸与碳酸钙反应生成醋酸钙和二氧化碳和水,发生强酸制弱酸的反应,乙酸的酸性比碳酸强,可用食醋除去水壶中的水垢,故正确;④乙酸和乙醇发生酯化反应制取乙酸乙酯是一可逆反应,乙酸不能完全反应,故错误;
2、下列说法不正确的是( )A.臭氧的强氧化性使其可用于饮用水消毒B.甲烷是最简单的有机物C.食醋中含有乙酸D.纤维素是植物贮存能量的主要形式
【详解】A.臭氧的强氧化性可以消毒杀菌,且其还原产物污染,可用于饮用水消毒,A正确;B.甲烷时含碳元素的化合物,属于有机物,且为最简单的有机物,B正确;C.食醋是以糯米、大米、麸皮、小麦、高粱、糖或酒等酿成的含乙酸的液体,C正确;D.植物贮存能量的主要形式为淀粉,而不是纤维素,纤维素是植物细胞壁的组成成分,D错误;
3.下列关于常见有机物的性质叙述正确的是( )A.乙酸分子中含有羧基,可与NaHCO3溶液反应生成CO2B.在水溶液里,乙酸分子中的−CH3可以电离出H+C.用溴水不能鉴别苯酚溶液、2,4−己二烯和甲苯D.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH
【详解】A.乙酸分子中含有羧基,能电离出氢离子,−COOH可与NaHCO3溶液反应生成CO2,故A正确;B.在水溶液里,乙酸分子中的−CH3不能电离出H+,−COOH能电离出H+,故B错误;C.溴水和苯酚溶液反应生成2,4,6−三溴苯酚沉淀,2,4−己二烯和溴水发生加成反应,使溴水褪色,溴水与甲苯发生萃取,溶液分层,因此用溴水能鉴别苯酚溶液、2,4−己二烯和甲苯,故C错误;D.根据酯化反应断键是酸脱羟基,醇脱羟基上的氢,酯的水解反应是酯化反应的逆过程,即在酸性条件下,CH3CO18OC2H5的水解产物是CH3COOH和C2H518OH,故D错误。
4.有机物的分离和提纯是有机化学研究的重要内容,下列物质所用的方法不正确的是( )A.CO2(SO2)——用碳酸钠溶液洗气B.三氯甲烷和水一一用分液漏斗分液C.淀粉溶液中混有氯化钠——用半透膜渗析D.乙醇(乙酸)——加入 CaO后蒸馏
【详解】A.CO2、SO2都能与碳酸钠溶液反应,不能用碳酸钠溶液除CO2中的SO2,可以用碳酸氢钠溶液洗气,故A错误;B.三氯甲烷不溶于水,用分液法分离三氯甲烷和水,故B正确;C.淀粉溶液是胶体,淀粉不能透过半透膜,用渗析法除去淀粉溶液中混有的氯化钠,故C正确;D.乙酸和CaO反应生成高沸点乙酸钙,加入 CaO后蒸馏可除去乙醇中的乙酸,故D正确;
5.乙酸是一种弱酸,请回答以下问题:(1)乙酸在水中的电离方程式为_______。(2)向乙酸溶液中加入石蕊试液,产生的现象是_______;将乙酸溶液滴加到碳酸钠溶液中,产生的现象是_______,反应的方程式为_______。(3)根据以上事实,说明乙酸的酸性比碳酸的酸性_______(填“强”或“弱”)。
【答案】(1)CH3COOH CH3COO-+H+(2) 溶液变红色 有无色气体产生 2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O(3)强(1)乙酸是弱酸,在水中部分电离,电离方程式为CH3COOH CH3COO-+H+;(2)乙酸具有酸的通性,可使石蕊试液变红;乙酸与碳酸钠反应生成乙酸钠、水和二氧化碳,产生的现象是有无色气体产生;反应的方程式为2CH3COOH+Na2CO3→2CH3COONa+CO2↑+H2O;(3)根据以上事实,说明乙酸的酸性比碳酸的酸性强。
高中化学人教版 (2019)必修 第二册第三节 乙醇与乙酸精品作业课件ppt: 这是一份高中化学人教版 (2019)必修 第二册第三节 乙醇与乙酸精品作业课件ppt,文件包含732乙酸课件pptx、732乙酸分层作业含解析docx、732乙酸分层作业无答案docx等3份课件配套教学资源,其中PPT共27页, 欢迎下载使用。
高中化学沪科技版(2020)必修第二册第7章 常见的有机化合物7.3 乙醇和乙酸乙酸课文课件ppt: 这是一份高中化学沪科技版(2020)必修第二册第7章 常见的有机化合物7.3 乙醇和乙酸乙酸课文课件ppt,共19页。PPT课件主要包含了结构简式,官能团,乙酸化学性质,2酸性比较,Na2CO3,饱和NaHCO3,Na2SiO3,醋酸盐酸,醇脱氢,酯水解反应-取代反应等内容,欢迎下载使用。
必修 第二册第三节 乙醇与乙酸一等奖课件ppt: 这是一份必修 第二册第三节 乙醇与乙酸一等奖课件ppt,共36页。PPT课件主要包含了学习目标,第2课时乙酸,乙酸的物理性质,乙酸的结构,乙酸的性质,与指示剂反应,与金属反应Zn,与碱作用NaOH,酸的通性,电离方程式等内容,欢迎下载使用。












