



高中化学沪科技版(2020)必修第二册第7章 常见的有机化合物7.3 乙醇和乙酸乙酸课文课件ppt
展开1.乙酸存在:乙酸俗称醋酸,常用作调味品,食醋中含3%-5%的乙酸
2.物理性质:无色,有强烈刺激性气味液体,易溶于水、和有机溶剂,易挥发,低于熔点(16.6℃)乙酸凝结成类似冰一样的晶体,因此纯净的醋酸又叫冰醋酸(纯净物)
3.常用的物理性质:溶解性:-OH 、-COOH、-CHO为亲水基,乙醇、乙酸、乙醛与水任意比例互溶
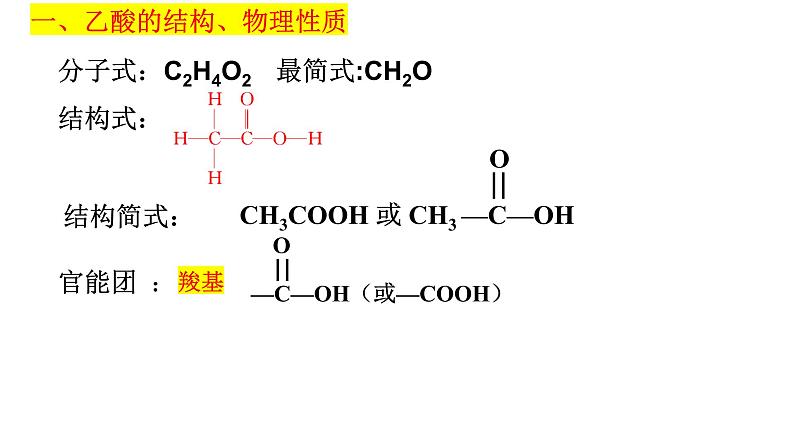
分子式:C2H4O2 最简式:CH2O 结构式:
一、乙酸的结构、物理性质
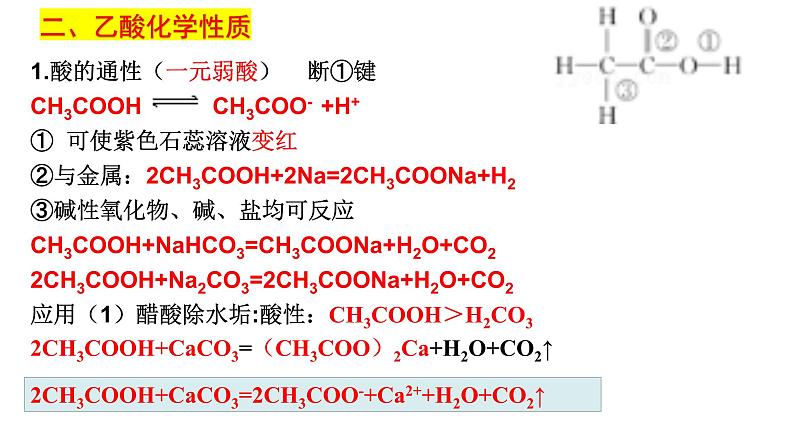
1.酸的通性(一元弱酸) 断①键CH3COOH CH3COO- +H+① 可使紫色石蕊溶液变红②与金属:2CH3COOH+2Na=2CH3COONa+H2③碱性氧化物、碱、盐均可反应CH3COOH+NaHCO3=CH3COONa+H2O+CO22CH3COOH+Na2CO3=2CH3COONa+H2O+CO2应用(1)醋酸除水垢:酸性:CH3COOH>H2CO3
2CH3COOH+CaCO3=2CH3COO-+Ca2++H2O+CO2↑
2CH3COOH+CaCO3=(CH3COO)2Ca+H2O+CO2↑
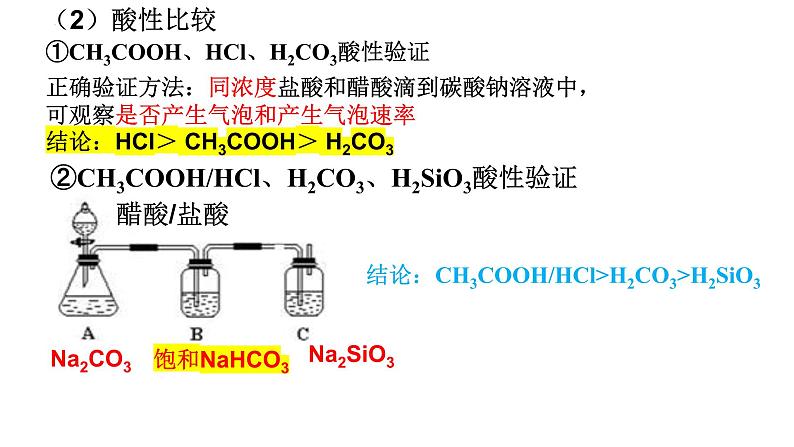
正确验证方法:同浓度盐酸和醋酸滴到碳酸钠溶液中,可观察是否产生气泡和产生气泡速率结论:HCl> CH3COOH> H2CO3
①CH3COOH、HCl、H2CO3酸性验证
②CH3COOH/HCl、H2CO3、H2SiO3酸性验证
结论:CH3COOH/HCl>H2CO3>H2SiO3
1、下列物质都能与Na反应放出H2,其产生H2的速率排列顺序正确的是( )①C2H5OH ②CH3COOH溶液 ③H2OA.①>②>③ B.③>①>②C.③>②>① D.②>③>①
2.酯化反应(取代反应)可逆反应
厨师烧鱼时常加醋并加点酒,这样鱼的味道就变得无腥、香醇,特别鲜美。
2.酯化反应(取代反应)可逆反应(1)原理:(2)方程式书写:(浓硫酸)催化剂、可逆、加热乙醇中O用18O标记反应后18O存在于什么物质中。分子量
酯化反应实验注意事项
1.药品滴加顺序:先加入3mL乙醇再加入2mL浓硫酸,冷却后加入2mL乙酸,最后加入碎瓷片 (若忘记加入,需停止加热冷却后再补加)2.现象:右侧试管内液体上层有无色透明的油状液体产生,并可以闻到香味→分液3.试剂作用①碎瓷片作用:防暴沸②浓硫酸作用: 催化剂 ,吸水剂③乙醇过量的目的:提高乙酸的转化率④饱和碳酸钠溶液作用:不用NaOHa.溶解乙醇(水的作用) b.中和乙酸(碳酸钠作用) c.降低乙酸乙酯的溶解度,便于分层
4.①试管向上倾斜45°的目的 :增大受热面积 ②长导管的作用:导气 :导乙酸乙酯 冷凝:冷却乙酸、乙醇导管末端不能插入到液面以下原因:防倒吸
(1)物理性质:相对分子质量比较小的低级酯密度比水小,易溶于有机溶剂,具有芳香气味。(很多鲜花和水果的香味来自酯)(2)用途:①作香料:如作饮料、糖果、香水中的香料。 ②作溶剂:如作高档化妆品的溶剂。
酯化反应-取代反应-可逆反应
四、常见有机物类别及其官能团
(使溴水或溴的CCl4溶液褪色)
(使酸性KMnO4溶液褪色)
氧化反应(燃烧、催化氧化、强氧化剂氧化)
取代反应(与羧酸发生酯化反应)
氧化反应(催化氧化成羧酸)
酸性(与金属、金属氧化物、碱、某些盐反应)
取代反应(与醇发生酯化反应)
取代反应(水解成酸和醇)
还原反应(与H2加成成醇)
化学必修 第二册第七章 有机化合物实验活动9 乙醇、乙酸的主要性质说课ppt课件: 这是一份化学必修 第二册第七章 有机化合物实验活动9 乙醇、乙酸的主要性质说课ppt课件,共24页。PPT课件主要包含了CH3COOH或,酒是陈的香,结构决定性质等内容,欢迎下载使用。
人教版 (2019)必修 第二册第七章 有机化合物第三节 乙醇与乙酸多媒体教学ppt课件: 这是一份人教版 (2019)必修 第二册第七章 有机化合物第三节 乙醇与乙酸多媒体教学ppt课件,共27页。PPT课件主要包含了醋的来历,黑塔传说,酯化反应实验,学习小结等内容,欢迎下载使用。
高中化学人教版 (2019)必修 第二册第三节 乙醇与乙酸教课内容ppt课件: 这是一份高中化学人教版 (2019)必修 第二册第三节 乙醇与乙酸教课内容ppt课件,共30页。PPT课件主要包含了CONTENTS,教学目标,重点难点,教学过程,课堂小结,乙酸的酯化反应,乙酸的结构和性质,教学过程-导入,酸的通性,酯化反应等内容,欢迎下载使用。













