






初中化学沪教版九年级上册第4章 认识化学变化第3节 化学方程式的书写与运用课前预习课件ppt
展开1.通过对具体反应的分析与计算,认识化学方程式能够定量地表达反应体系中物质间的微粒数目、宏观质量的比例关系;2.能根据化学反应方程式进行反应物、生成物质量关系的简单计算,深化对质量守恒定律的理解; 3.通过归纳总结活动和具体化学反应的分析,认识化学方程式(化学符号)是联系化学反应的宏观事实与微观本质、定性与定量关系的桥梁,感悟化学反应的条件性、规律性和客观性,深化对原子组合方式的改变是化学变化本质的直观认识,感悟定量处理化学变化对人类生产生活与科研的意义。
氢气是未来汽车的理想燃料。1Kg的氢气就能供一辆功率为50KW的汽车跑大约100Km。 水是生命之源,找到合适的催化剂,即可利用光能将水分解制取氢气。
要想知道汽车能跑多远,就要弄清楚小桶中18Kg的水能分解产生多少Kg的氢气?
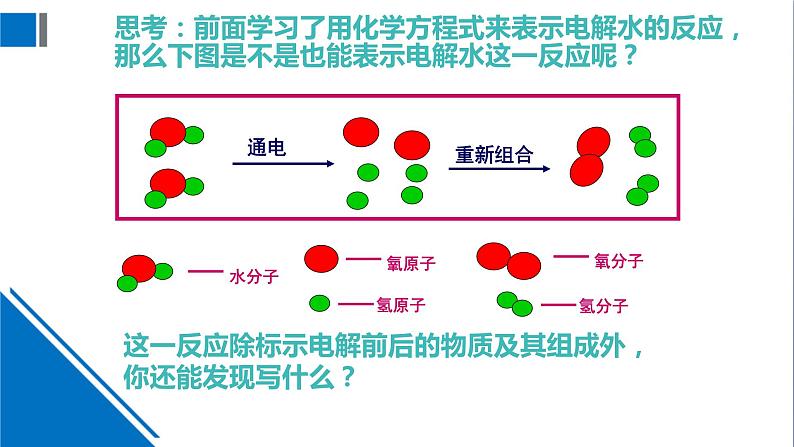
思考:前面学习了用化学方程式来表示电解水的反应,那么下图是不是也能表示电解水这一反应呢?
这一反应除标示电解前后的物质及其组成外,你还能发现写什么?
回过头来看前面给出的电解水的方程式,你对这一化学方程式有何新的认识?请从多个角度来分析。
水在通电情况下产生氢气和氧气
每36分质量的水分子在通电情况下分解生成4份质量的氢气和32份质量的氧气。
每2个水分子在通电情况下分解生成2个氢分子和1个氧分子。
2×18 : 2×2 : 16 ×2
36 : 4 : 32
①表示一氧化碳和氧气在点燃条件下生成二氧化碳
③表示每56份质量的一氧化碳与32份质量的氧气在点燃条件下生成88份质量的二氧化碳。
②表示两个一氧化碳分子与一个氧分子在点燃条件下生成一个二氧化碳分子
以水通电为例说明化学方程式中量的意义。
2×18 : 2×2 : 16×2
36 : 4 : 32
若 36 克 : ( )克 :( )克
由上可知:(1)化学反应都遵守____________。 (2)在化学反应中,各物质间的质量比成_______关系。
若 18 千克 : ?
若 108 克 : ( )克 :96克
(化学方程式计算依据)
表示每36份质量的水通电完全反应生成4份质量的氢气和32份质量的氧气。
15.5克红磷在氧气中充分燃烧,可生成五氧化二磷多少克?
请同学们参照课本107页的例题,找出下列解答中的错误
31 14215.5 X
P + O 2 P 2 O 5
解:设可生成X克五氧化二磷
2H2O 2H2↑+O2↑
解:设小桶中18Kg的水分解生成氢气的质量为x。
所以,小桶中的水能使小汽车行驶:2×100=200(Km)
答:18Kg水分解生成的氢气是2Kg。
小桶中18Kg的水能分解产生多少Kg的氢气?
(1)设未知量(不带单位)
(3)找出反应物和生成物的质量关系
电解36克水可得到多少克氢气?下面是四位同学的解题过程和结果如下,检查后回答:
设未知数带单位物质化学式写错
未注明单位未知量没找对
依据化学方程式计算的示例
例:某兴趣小组用高锰酸钾固体制取6.4g氧气,请你计算一下,该小组至少需要准备多少高锰酸钾固体?(温馨提示:K-39 O-16 Mn-55)
某兴趣小组用高锰酸钾固体制取氧气,生成氧气的质量如下图所示,(横坐标表示反应时间,纵坐标表示生成氧气的量)试计算:(1)实验中生成氧气的质量为__________;(2)反应中消耗了多少高锰酸钾固体?(温馨提示:K-39 O-16 Mn-55)
某兴趣小组用高锰酸钾固体制取氧气,生成氧气的质量如下表格所示:试计算:(1)实验中生成氧气的质量为________;(2)反应中消耗了多少高锰酸钾固体?(温馨提示:K-39 O-16 Mn-55)
化学方程式计算的三个要领和三个关键。三个要领:①步骤要完整;②格式要规范;③得数要准确。三个关键: ①准确书写化学式,化学方程式要配平; ②准确计算相对分子质量; ③计算单位不能忘
练习1 液氢、液氧常用于火箭发射升空,已知火箭升空至少要携带100kg的液氢,充分燃烧才能获得足够的能量。假如你是长征系列火箭推进器的设计师,你会在火箭助燃仓中填充多少千克的液氧来满足这些液氢的完全燃烧?(温馨提示:H-1 O-16 )
请同学们认真阅读 P107-108“观察与思考”栏目,并在对比基础上思考与交流:1.两种计算方法有什么差异?2.采用两种不同的方法进行计算,为何得到的结果相同?3.根据这两种计算方法,你对化学方程式计算的本质(依据)有什么感悟?
感悟化学方程式计算的本质(依据)
教材呈现两种解法,第一种解法是利用化学方程式进行计算,第二种解法是利用化学式计算。对于第二种解法,结合氧化铝中铝元素的质量分数,进而求出 10t 氧化铝中铝的质量。由于电解氧化铝时,铝元素全部转化为铝单质,因而 10t 氧化铝中铝元素的质量就是单质铝的质量。这一计算过程,体现了铝元素质量在冶炼前后保持不变;而第一种解法依据化学方程式进行计算,而化学反应方程式本身就是质量守恒定律的一种体现方式(书写化学方程式必须符合质量守恒定律)。换句话说,化学方程式本身就反映化学反应前后元素守恒的问题。因此,不论是解法一还是解法二,抓住的都是铝元素的守恒。因此,不难理解,化学方程式计算是以质量守恒定律为依据,突出抓元素守恒这一本质。
请同学们按第二种解法解答下面的练习:为何采用前述方法一和方法二进行求解,将得出不同的答案?
练习2:实验室要用31.6g氧气做实验。小红同学提议利用加热分解高锰酸钾的方法来制取氧气。那么,请你帮小红同学计算一下,可一以收集多少质量的氧气?(温馨提示:K-39 O-16 Mn-55)
请同学们注意:教材 P107 有这样的描述“在某些特定情况下,可以依据化学式或者化学方程式确定反应中物质的质量关系”。“在某些特定的情况下”所指的特定情况是什么?
“在某些特定的情况下”指的是反应物中的某种元素必须完全转化为产物,才可以依据化学式确定反应中物质的质量关系。
请大家思考:如果所给的反应中含有杂质,比如课本例题中的氧化铝含有 10%的杂质,是否也可以将 10t 直接带入化学方程式进行计算?如果不可以,要进行怎样的处理?为什么?
练习4 四川省汶川在5·12特大地震后,全国人民伸出了 援助之手。在重建家园的过程中很多地方需要大量的生石灰(CaO)。某石灰厂的王厂长听到消息后,决定捐赠某校需要的生石灰,现石灰厂的原料中还含有12.5t含80%碳酸钙的石灰石,请你帮助王厂长计算一下这12.5吨石灰石可为该校提供多少吨的生石灰(CaO)?温馨提示:该反应化学方程式为:
Ca -40 C-12 O-16
(1)代入化学方程式计算的量必须是纯净物的质量,若是不纯物,则需转换. 纯净物的质量=不纯物质质量×纯度 =不纯物质质量×(1-杂质的质量分数) 纯度:为该物质在混合物中的质量分数. (2)如果为气体体积,则按下式将其换算成气体质量. 气体质量(g)=气体体积(L)×密度(g/L) 同理: 液体质量(g)=液体体积(mL)×密度(g/mL)
火药是中国四大发明之一。据史料记载,火药的研究开始于古代道家炼丹术。最晚到了唐代,含硝(硝酸钾)、硫、炭三组分的火药已经在中国诞生,并有人提出了“硫二两,硝二两,马兜铃(可理解为炭)三钱半”的火药配方。
已知,火药点燃时,发生反应的化学方程式为:2KNO3 + S + 3C = K2S + N2↑ + 3CO2↑。
请分析“硫二两、硝二两”的配比是否合适呢?
根据化学方程式可知,硝酸钾和硫的质量之比应为 101:16,而不是 1:1
设、写、找、列、算、答
(1)准确书写化学方程式;
(2)准确计算相对分子质量;
(3)计算单位不能忘;
利用化学方程式的简单计算的注意事项:
(1)化学反应都遵守质量守恒定律。 (2)在化学反应中,各物质间的质量比成正比例关系。
解:设若要得到48g氧气,需过氧化钠的质量是x
答:要得到48g氧气,需过氧化钠的质量是234g。
初中化学沪教版九年级上册第3节 化学方程式的书写与运用教课课件ppt: 这是一份初中化学沪教版九年级上册第3节 化学方程式的书写与运用教课课件ppt,共17页。PPT课件主要包含了三种表达方式,化学方程式的书写步骤,化学方程式的配平,如何配平化学方程式,①最小公倍数法,③整体法,看作MnO4,②归一法,练习1,课堂训练等内容,欢迎下载使用。
初中化学沪教版九年级上册第3节 化学方程式的书写与运用课文配套ppt课件: 这是一份初中化学沪教版九年级上册第3节 化学方程式的书写与运用课文配套ppt课件,文件包含第4章第3节第4课时教学课件pptx、第4章第3节第4课时教案含练习docx等2份课件配套教学资源,其中PPT共14页, 欢迎下载使用。
初中沪教版第3节 化学方程式的书写与运用说课ppt课件: 这是一份初中沪教版第3节 化学方程式的书写与运用说课ppt课件,文件包含第4章第3节第3课时教学课件pptx、第4章第3节第3课时教案含练习docx等2份课件配套教学资源,其中PPT共13页, 欢迎下载使用。














