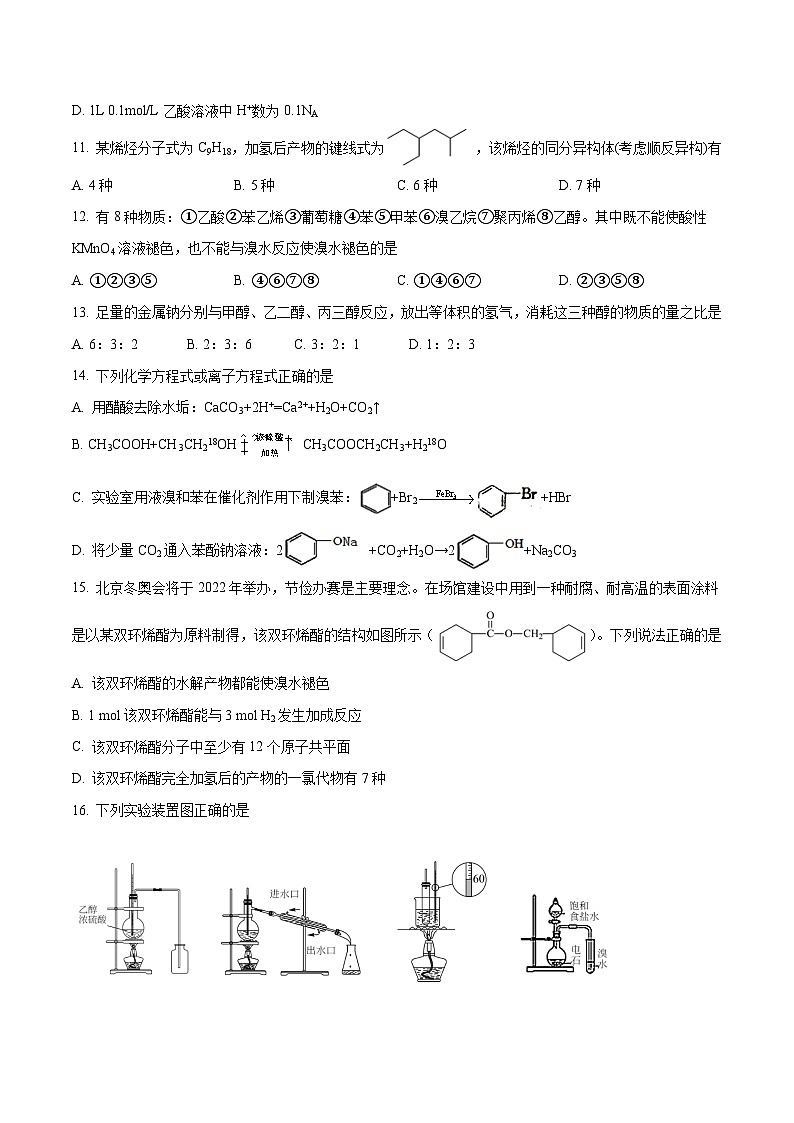






期末模拟试卷03——高二化学下学期期末模拟试卷(人教版2019选择性必修3)
展开期末模拟试卷04
说明:1.本试题分为第I卷和第II卷,第I卷选择题40分,第II卷非选择题60分。
2.考试时间为75分钟,共100分。
3.考试结束将答题卷交回。
可能用到的相对原子质量:H-1 C-12 O-16 N-14 S-32 Li-7 Cl-35.5
第I卷(选择题,共40分)
一、选择题(本题包括20小题,每小题2分,共40分。每小题只有1个选项符合题意)
1. 化学与生活息息相关,下列说法正确的是
A. 医用酒精灭杀新冠病毒是利用其氧化性
B. 我国研制的重组新冠疫苗,需要冷藏保存
C. 新冠病毒由C、H、O三种元素组成
D. 为增强“84”消毒液的消毒效果,可加入过量盐酸
2. 下列说法正确的是
A. 分馏、干馏都是物理变化,裂化、裂解都是化学变化
B. 淀粉、纤维素都是高分子化合物,水解的最终产物相同
C. 氨基酸与蛋白质遇到重金属盐均变性
D. 尼龙绳、羊绒衫和棉衬衣等生活用品都是由合成纤维制造的
3. 某烃的结构简式为,有关其结构的说法正确的是( )
A. 所有原子可能同一平面上 B. 所有原子可能在同一条直线上
C. 所有碳原子可能在同一平面上 D. 所有氢原子可能在同一平面上
4. 可用来鉴别己烯、甲苯、乙酸乙酯、苯酚溶液的一组试剂是( )
A. 氯化铁溶液、溴水 B. 碳酸钠溶液、溴水
C. 酸性高锰酸钾溶液、溴水 D. 酸性高锰酸钾溶液、氯化铁溶液
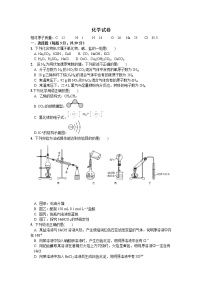
5. 利用下列装置(夹持装置略)进行实验,能达到实验目的的是
A. 用甲装置蒸馏米酒 B. 用乙装置制备溴苯并验证有HBr产生
C. 用丙装置制备无水MgCl2 D. 用丁装置在铁上镀铜
6. 有关的说法正确的是
A. 可以与氢气发生加成反应 B. 不会使溴水褪色
C. 只含二种官能团 D. 该物质与足量溶液反应,最多可消耗
7. 下列实验方案能实现相应实验目的或得出相应结论的是
选项 | 实验方案 | 实验目的或结论 |
A | 向20%蔗糖溶液中加入少量稀H2SO4,加热;再加入银氨溶液,未出现银镜 | 蔗糖未水解 |
B | 石蜡油分解实验中,将分解生成的气体通入溴的四氯化碳溶液中,溶液褪色 | 证明有不饱和烃生成 |
C | 用两支试管各取5mL0.1mol·L-1的KMnO4溶液,分别加入2mL0.1mol·L-1和2mL0.01mol/L的草酸溶液,记录溶液褪色所需的时间 | 探究浓度对化学反应速率的影响 |
D | 在相同温度下,向1mL0.2mol·L-1NaOH溶液中滴入2滴0.1mol·L-1MgCl2溶液,产生白色沉淀后,再滴加2滴0.1mol·L-1FeCl3溶液,又生成红褐色沉淀 | 溶解度:Mg(OH)2>Fe(OH)3 |
8. 芬必得是一种高效的消炎药物,主要成分为化合物布洛芬,其结构简式如图所示,下列说法正确的是
A. 布洛芬的分子式为C13H18O2 B. 布洛芬不能使酸性高锰酸钾溶液褪色
C. 布洛芬可以发生加成、氧化、取代和消去反应 D. 布洛芬苯环上的一氯取代产物有四种
9. 有机物X的结构简式是,能用该结构简式表示的X的同分异构体共有(不考虑立体异构)
A. 7种 B. 8种 C. 9种 D. 10种
4. 化学使生活更丰富,化学使生活有滋有味。下列说法不正确的是
A. 利用废弃的油脂制取脂肪酸和甘油的反应称为“皂化反应”
B. 谷氨酸通过中和反应制取味精的主要成分,关键是严格控制溶液的
C. 营养蛋白粉人体内水解断裂的肽键即酰胺键,但酰胺键不一定是肽键
D. 蛋类中的部分蛋白质、脂肪与渗入的强碱生成盐,在变性呈胶冻状蛋白质中结晶形成“松花”
10. 下列关于醛、酮和酸说法正确的是
A. 醛与银氨溶液充分反应,均能还原出银
B. 醛和酮既可还原为醇,也可氧化为酸
C. 羧酸因其官能团可与水形成氢键,所以均易溶于水
D. 仅用新制的悬浊液合理操作就能鉴别甲酸、乙醛、乙酸和丙酮
11. 如图所示某醇的化学反应过程,对该过程判断不正确的是
A. 反应中有红黑颜色交替变化的现象 B. 可能生成四种醛
C. 醇类不一定能发生图示的催化氧化反应 D. 醇发生了氧化反应
12. Cyrneine A对治疗神经系统疾病有着很好的疗效。可用香芹酮经过多步反应合成。下列说法正确的是
A. 香芹酮的分子式为C10H16O B. 香芹酮的一氯代物有7种
C. 香芹酮和Cyrneine A均能发生酯化反应 D. Cyrneine A中含有4种官能团
13. 合成某小分子抗癌药物中间产物,分子结构如图。下列说法正确的是
A. 该有机物的化学式为C14H16O6
B. 该有机物有四种表现不同性质的官能团
C. 该物质属于烯烃、多官能团有机化合物、芳香烃、烃的衍生物
D. 该有机物可属于有机酸类
14. 将乙炔通入银氨溶液,产生白色沉淀,通过该实验可以区分乙炔和乙烯。化学方程式为:HC≡CH+2[Ag(NH3)2]+ →AgC≡CAg↓+2NH4++2NH3。乙炔银遇酸可放出乙炔。下列分析或推测不正确的是
A. 乙炔与银氨溶液的反应不是氧化还原反应
B. 乙炔中C-H键的活性比乙烯中C-H键的活性强
C. 乙炔通入AgNO3溶液中也能发生类似反应
D. 2-丁炔不能与银氨溶液发生类似反应
15. 已知:己内酯和乙醇在一定条件下可以发生反应:+C2H5OH,下列说法不正确的是
A. 该反应的类型是取代反应
B 粮食经生物发酵可得到乙醇
C. HO(CH2)5COOH通过分子内酯化反应可以生成己内酯
D. 该条件下,己内酯和乙醇还可生成高分子
16. 一定条件下,烯烃分子间可发生如图所示的“复分解反应”,形象的称为“交换舞伴的反应”。这一过程可以用化学方程式表示为:R1CH=CHR2+R3CH=CHR4R1CH=CHR3+R2CH=CHR4,据此判断,下列反应的方程式不正确的是
A. +CH3CH=CH2
B. CH2=CH(CH2)4CH=CH2+CH2=CH2
C. n
D. nCH2=CHCH=CH2
17. 在有机合成中官能团的引入或改变是极为重要的,下列说法正确的是( )
A. 甲苯在光照下与Cl2反应,主反应为苯环上引入氯原子
B. 引入羟基的方法常有卤代烃和酯的水解、烯烃的加成、醛类的还原
C. 将CH2=CH—CH2OH与酸性KMnO4溶液反应即可得到CH2=CH—COOH
D. HC≡CH、(CN)2、CH3COOH三种单体在一定条件下发生加成、酯化反应即可得到
18. 某有机物W由C、H、O三种元素组成,相对分子质量为90。将9.0gW完全燃烧的产物依次通过足量的浓硫酸和碱石灰,分别增重5.4g和13.2g。W能与NaHCO3溶液发生反应,且2个W发生分子间脱水反应生成六元环化合物。有关W的说法正确的是
A. W的分子式为C3H8O3
B. W催化氧化的产物能发生银镜反应
C. 0.1molW与足量Na反应产生1.12LH2(标准状况)
D. W在一定条件下可以发生缩聚反应生成高分子材料
19. 不饱和聚酯(UP)是生产复合材料“玻璃钢”的基体树脂材料。如图是以基础化工原料合成UP流程:
下列说法不正确的是( )
A. 丙可被KMnO4酸性溶液直接氧化制单体1
B. 单体2可能是乙二醇
C. 单体1、2、3经缩聚反应制得UP
D. 调节单体的投料比,控制m和n的比值,获得性能不同的高分子材料
20. 已知乙烯醇(CH2=CHOH)不稳定,可自动转化为乙醛;二元醇脱水生成环状化合物。现有1mol乙二醇在一定条件下脱去1mol水,所得产物的结构简式有下列几种,其中不可能的是
①CH2=CH2 ② ③CH3CHO ④
A. 只有① B. 有①② C. 有①③ D. 有①④
第II卷(非选择题,共60分)
21. (15分)现有下列10种与人们生产生活相关的有机物:
①HCHO(防腐剂) ②CH3CH2CHO(化工原料) ③CH3CH2CH2CH3(打火机燃料) ④(冷冻剂) ⑤ (汽车防冻液) ⑥ (杀菌剂) ⑦(定香剂) ⑧ (汽油添加剂) ⑨CH3COOH(食醋成分) ⑩ 有机物A(可由葡萄糖发酵得到,也可从酸牛奶中提取)
请回答:
(1)属于醇的是___________(填序号)。
(2)互为同系物的是___________(填序号)。
(3)互为同分异构体的是___________(填序号)。
(4)用系统命名法给④命名,其名称为___________。
(5)写出②与银氨溶液发生银镜反应的化学方程式___________。
(6)写出⑤与⑨在浓硫酸加热的条件下,按物质的量1∶2反应的方程式___________。
(7)⑧与H2在一定条件下完全加成后所得产物的一氯代物共有___________种。
(8)A的摩尔质量为90g/mol,将18.0 g A在足量纯O2充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现分别增重10.8g和26.4 g;A的结构中含有1个甲基,1个羟基和一个羧基,则A的结构简式为___________。
22. (15分)某小组同学为研究有机物的官能团以及化学键的活性,完成下列对比实验。
| 实验I | 实验II |
实验方案与 现象 |
(1)实验I、实验II使用到的两种有机物的关系是_______。
(2)实验I中发生反应的化学方程式是_______。
(3)对比分析实验I和实验II,从结构角度解释发生不同现象的原因_______。
(4)该小组同学欲验证,进一步探究有机化合物基团之间的相互影响。完成下表实验,请将实验方案和实验现象补充完整。
实验方案 | 实验现象 |
①将过量CH4气体通入酸性高锰酸钾溶液 | 酸性高锰酸钾溶液不褪色 |
②向盛有2mL甲苯的试管中加入5滴酸性高锰酸钾溶液,用力振荡,静置 | _______ |
③_______ | 酸性高锰酸钾溶液不褪色 |
实验结论:_______。
23. (15分)三颈圆底烧瓶是一种常用的化学玻璃仪器,在有机化学实验中被广泛使用。可以用该仪器来制备苯乙酸铜,以下为实验室合成路线。
反应的原理为:
+H2O+H2SO4+NH4HSO4
2+Cu(OH)2→+2 H2O
药品 | 相对分子质量 | 熔点/℃ | 沸点/℃ | 溶解性 | 密度(g·cm-3) |
苯乙腈 | 117 | -48 | 197 | 微溶于冷水,易溶于乙醇 | 1.08 |
苯乙酸 | 136 | 76.5 | 161 | 微溶于冷水,易溶于乙醇 | 1.17 |
(1)在250 mL三颈烧瓶中加入70 mL70%硫酸。配制此硫酸时,加入蒸馏水与浓硫酸的先后顺序是__________________________。
(2)仪器b的名称________________,其作用是_____________;合成苯乙酸时,最合适的加热方法是_____________。
(3)反应结束后加适量冷水,再分离出苯乙酸粗品。加入冷水的目的是_____________。下列仪器中可用于分离苯乙酸粗品的是___________(填标号)。
A.分液漏斗 B.漏斗 C.烧杯 D.直形冷凝管 E.玻璃棒
(4)由于苯乙酸的沸点较高,在蒸馏纯化操作中最适宜选用的仪器之一是_____(填字母)。
A. B. C.
(5)在实验中原料用量:5.0 mL苯乙腈,最终称得产品质量为3.2 g,则所得的苯乙酸的产率为_________%(结果保留三位有效数字)。
(6)将苯乙酸加入到乙醇与水的混合物中,充分溶解后,加入Cu(OH)2搅拌30 min,过滤,滤液静置一段时间,析出苯乙铜晶体,混合溶剂中乙醇的作用是_________
24. (15分)有机化合物I是一种重要的有机合成中间体,合成路线如图:
已知:①+
②+
回答下列问题:
(1)A的名称为___________,B中所含官能团的名称___________。
(2)F→G过程中涉及的反应类型有___________,写出G→I的化学方程式___________。
(3)1 mol D最多可以与___________mol的NaOH反应。
(4)物质C苯环上有两个取代基,既能与NaHCO3溶液反应又能与FeCl3溶液显色的同分异构体(不考虑立体异构)且分子内只有含一个环的有___________种。写出其中一种含有手性碳原子的结构简式___________。
(5)计由和为原料制备 的合成路线(无机试剂任选) ___________。
期末模拟试卷03-04-2023-2024学年高二化学下学期期中期末考点大串讲(人教版选择性必修3): 这是一份期末模拟试卷03-04-2023-2024学年高二化学下学期期中期末考点大串讲(人教版选择性必修3),文件包含期末模拟试卷04-原卷版docx、期末模拟试卷03-原卷版docx、期末模拟试卷04-解析版docx、期末模拟试卷03-解析版docx等4份试卷配套教学资源,其中试卷共58页, 欢迎下载使用。
安徽省宣城市泾县重点中学2022-2023学年高一下学期竞赛选拔化学试题含解析: 这是一份安徽省宣城市泾县重点中学2022-2023学年高一下学期竞赛选拔化学试题含解析,共19页。试卷主要包含了单选题等内容,欢迎下载使用。
化学03卷(人教版2019选择性必修3)——2022-2023学年高二下学期期末模拟测试卷: 这是一份化学03卷(人教版2019选择性必修3)——2022-2023学年高二下学期期末模拟测试卷,文件包含化学03卷人教版2019-全解全析docx、化学03卷人教版2019-考试版A4范围选择性必修3docx、化学03卷人教版2019-参考答案docx、化学03卷人教版2019-答题卡docx等4份试卷配套教学资源,其中试卷共29页, 欢迎下载使用。