









初中化学沪教版九年级上册第2节 金属矿物 铁的冶炼公开课教学课件ppt
展开第5章 金属的冶炼与利用
5.2 金属矿物 铁的冶炼(第2课时)
1.(2022·内蒙古·扎赉特旗音德尔第三中学九年级期末)下列关于工业炼铁的叙述中错误的是( )
A.使用的设备是高炉
B.主要原料为铁矿石、石灰石、焦炭和热空气等
C.主要原理是:2Fe2O3+3C=4Fe+3CO2↑
D.主要产物为生铁
【答案】C
【解析】A、工业炼铁的设备是高炉,不符合题意;
B、工业炼铁的主要原料为铁矿石、石灰石(石灰石能将铁矿石中的二氧化硅转化为炉渣除去)、焦炭(提供高温和还原剂一氧化碳)、热空气等,不符合题意;
C、工业炼铁的主要原理是一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,该反应的化学方程式为:Fe2O3+3CO 高温 2Fe+3CO2,符合题意;
D、工业炼铁的主要产物是生铁,不符合题意。
故选C。
2.(2022·江苏江苏·模拟预测)下列关于炼铁的说法不正确的是( )
A.工业炼铁所用的设备是高炉
B.为充分利用一氧化碳要先加热试管
C.工业炼铁原料要用到石灰石
D.实验室模拟炼铁时要进行尾气处理
【答案】B
【解析】A、工业炼铁所用的设备是高炉,说法正确,不符合题意;
B、一氧化碳具有可燃性,混有一定量的空气,遇到明火,容易发生爆炸,故应先通入一氧化碳,将装置内空气排尽,然后加热试管,符合题意;
C、工业炼铁原料要用到石灰石,石灰石能将铁矿石中的二氧化硅转化为炉渣除去,不符合题意;
D、实验室模拟炼铁是一氧化碳和氧化铁在高温下反应生成铁和二氧化碳,一氧化碳有毒,扩散到空气中,会污染空气,故要进行尾气处理,不符合题意。
故选B。
3.(2022·江苏·盐城市第八中学三模)下列有关钢铁的叙述不正确的是( )
A.生铁的含碳量比钢多
B.铁丝在氧气中燃烧生成Fe2O3
C.在钢管表面镀锌可以防止锈蚀
D.炼铁的主要原料有铁矿石、焦炭、石灰石、(热空气)
【答案】B
【解析】A、生铁的含碳量为2%-4.3%,钢的含碳量为0.03%-2%,故生铁的含碳量比钢多,不符合题意;
B、铁丝在氧气中燃烧生成四氧化三铁,不是氧化铁,符合题意;
C、锌比铁活泼,铁制品表面镀锌后,会先腐蚀镀锌层,保护了铁制品,在钢管表面镀锌可以防止锈蚀,不符合题意;
D、炼铁的主要原料有铁矿石、焦炭(提供高温和还原剂一氧化碳)、石灰石(将铁矿石中的二氧化硅转化为炉渣除去)、(热空气),不符合题意。
故选B。
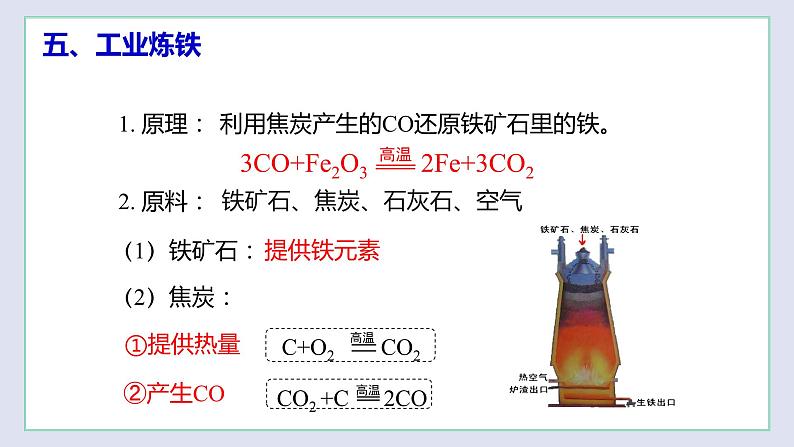
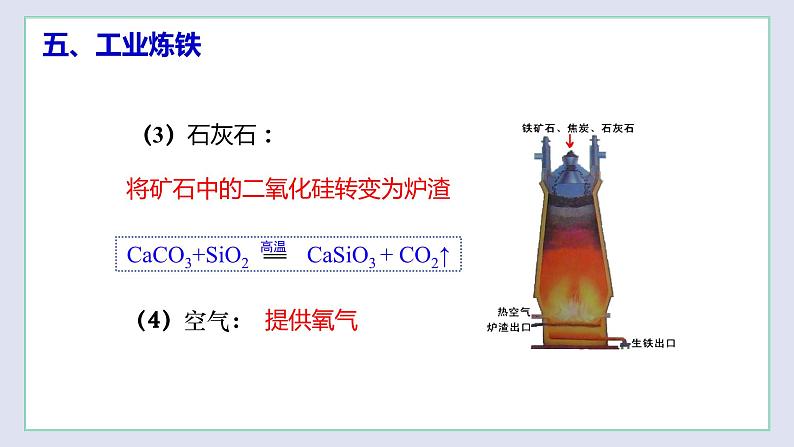
4.(2022·辽宁沈阳·二模)如图是炼铁高炉示意图,下列说法正确的是( )
A.焦炭的主要作用是提供热量、产生二氧化碳
B.石灰石的作用是与铁矿石中的杂质反应形成炉渣
C.生铁出口位置低于炉渣出口的原因是生铁密度小于炉渣
D.产生的废气无需处理,因为它不会污染空气
【答案】B
【解析】A、焦炭燃烧放出大量的热可以提供热量、焦炭与二氧化碳在高温下反应生成一氧化碳,可提供还原剂CO,错误;
B、石灰石的作用是与铁矿石中的二氧化硅反应形成炉渣,正确;
C、出铁口位置低于出渣口的原因是生铁密度大于炉渣,位于高炉的下方,错误;
D、产生的废气中含有许多有毒气体一氧化碳等气体需处理,防止污染空气,错误。
故选B。
5.(2022·广东·九年级专题练习)炼铁厂以赤铁矿石、焦炭、石灰石、空气等为主要原料炼铁,判断下列说法错误的是( )
A.炼铁的主要原料均为混合物
B.焦炭的作用是提供能量和制取一氧化碳
C.炼铁的主要反应是置换反应
D.炼铁最后得到的是合金
【答案】C
【解析】A、炼铁的主要原料是赤铁矿石、焦炭、石灰石、空气等这些物质都是混合物,此选项正确;
B、焦炭的作用是:焦炭燃烧提供能量同时焦炭在氧气不充足的条件下反应生成一氧化碳,此选项正确;
C、炼铁的主要反应是Fe2O3+3CO 高温 2Fe+3CO2,反应物是两种化合物,不属于置换反应,此选项错误;
D、炼铁最后得到的是含碳量为2%~4.3%的生铁,生铁属于合金,此选项正确。
故选C。
6.(2022·全国·九年级课时练习)工业炼铁的部分反应如图所示,则下列说法正确的是( )
A.X可以是木炭 B.X与CO都具有氧化性
C.③反应后的尾气可直接排放 D.Y中铁元素以游离态存在
【答案】A
【解析】A、木炭在氧气中充分燃烧生成二氧化碳,X可以是木炭,故选项说法正确;
B、二氧化碳与碳在高温下反应生成一氧化碳,X与CO都具有还原性,故选项说法错误;
C、一氧化碳具有毒性,会污染环境,尾气不能直接排放,故选项说法错误;
D、Y是铁的氧化物,Y中铁元素以化合态存在,故选项说法错误。
故选A。
7.(2022·陕西·西安市曲江第二中学模拟预测)用赤铁矿在高炉中炼铁过程中可能发生下列化学反应:
① ②
③ ④
对于这些反应的叙述不正确的是( )
A.共涉及两种基本反应类型
B.反应②可用于实验室制备二氧化碳
C.反应④过程中可观察到红棕色粉末逐渐变为黑色
D.CO和CO2可以相互转化
【答案】B
【解析】A、反应①是炭和氧气在高温下反应生成二氧化碳,反应③是炭和二氧化碳高温下反应生成二氧化碳,都是由两种物质反应生成另一种新物质,符合“多变一”的特征,均属于化合反应,反应②是碳酸钙在高温下分解生成氧化钙和二氧化碳,由一种物质分解生成两种新物质,符合“一变多”的特征,属于分解反应, ④不属于基本反应类型,共涉及两种基本反应类型,选项说法正确;
B、反应②是在高温的条件下进行的,所以实验室中制取二氧化碳不选择此方法,而是采用大理石或石灰石与稀盐酸反应来制取,选项说法错误;
C、在高温的条件下,一氧化碳与氧化铁反应生成铁和二氧化碳,所以观察到红棕色粉末逐渐变为黑色,选项说法正确;
D、由反应③和反应④可知,CO和CO2可以相互转化,选项说法正确。
故选B。
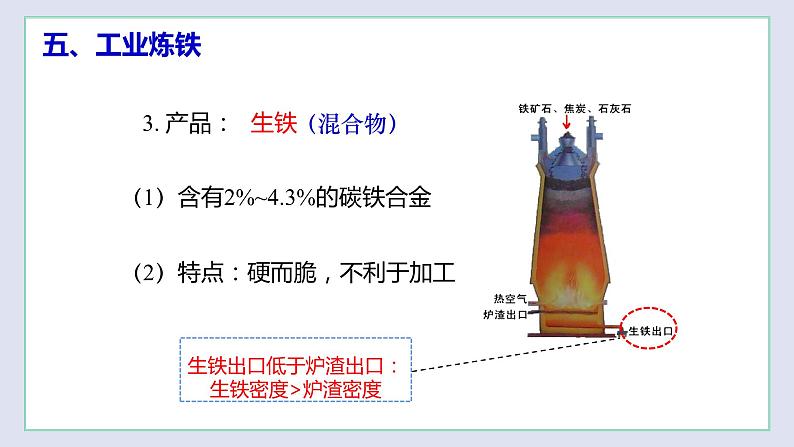
8.(2022·全国·九年级课时练习)工业上把铁矿石、焦炭和石灰石一起投放高炉内,从下方通入热空气,最后得到生铁。下列说法中正确的是( )
A.矿石中含铁就可用作炼铁原料
B.焦炭只起为反应提供还原剂作用
C.所得生铁的含碳量在2%~4.3%之间
D.高炉气体主要含有一氧化碳和二氧化碳
【答案】C
【解析】A、炼铁选用的铁矿石不仅要选含铁量高的,还要选“有害元素”少的,不然成本高还会造成空气污染,如黄铁矿(FeS2)就不适合炼铁;故A不正确;
B、炼铁过程中原料中的焦炭先燃烧生成二氧化碳的同时放出大量的热来提高高炉的温度,生成的二氧化碳再与焦炭在高温下反应生成还原剂一氧化碳气体,一氧化碳最后跟铁的氧化物在高温下反应生成铁,所以焦炭的作用是提供能量和生成还原剂一氧化碳,故B不正确;
C、铁的合金有生铁和钢两种,生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%,从高炉炼得的是生铁,所以含碳量为2%~4.3%,故C正确;
D、炼铁时,从高炉下方通入热空气,空气的主要成分是氮气,但冶炼过程并没有氮气参与反应,所以高炉气体主要含有的应该是氮气,故D不正确。
故选C。
9.(2022·黑龙江·中考真题)下图是炼铁高炉内部的物料说明和一套工业炼铁设备模型。请分析回答问题:
(1)高炉炼铁的原理是(用化学方程式表示)_____。
(2)高炉炼铁得到的产品是生铁,生铁和钢都是铁的合金,性能不同是因为_____。
(3)如图副产品中的____又回到了高炉,副产品综合利用的好处是____。
【答案】(1)Fe2O3+3CO 高温 2Fe+3CO2
(2)含碳量不同
(3) 炉气(或CO、N2、CO2) ;节约能源(或减少空气污染)
【解析】(1)高炉炼铁的原理是在高温的条件下一氧化碳和氧化铁反应生成铁和二氧化碳,反应的化学方程式是Fe2O3+3CO 高温 2Fe+3CO2。
(2)生铁的含碳量为2%~ 4.3%,钢的含碳量为0.03%~2%,因为含碳量不同,所以生铁和钢的性能不同。
(3)由图可知,副产品中的炉气又回到了高炉可循环利用,这样可不但可以节约能源还可以减少空气污染。
10.(2021·甘肃甘南·中考真题)工业上炼铁炼钢和轧制钢材的主要流程如下图:
已知生铁的含碳量为2%~4.3%,钢的含碳量为0.03%~2%。
回答下列问题:
(1)反应:①Fe2O3+3CO2Fe+3CO2,②2Fe2O3+3C4Fe+3CO2↑。属于置换反应的是______,高炉炼铁的主要反应是______(填数字序号)。
(2)炼铁的固体原料需粉碎,粉碎的目的是______。
(3)炼钢炉中,通入纯氧的目的是______。
(4)将钢锭轧成钢板,体现了金属铁的______性。
【答案】(1) ②;①
(2)增大反应物的接触面积,使反应更充分
(3)将生铁中过量的碳除去
(4)延展
【解析】(1)单质和化合物生成单质和化合物,属于置换反应,②反应属于置换反应,高炉炼铁主要反应是一氧化碳在高温条件下还原氧化铁生成铁和二氧化碳,即反应①,故选:②;①。
(2)炼铁的固体原料需粉碎,粉碎的目的是增大反应物的接触面积,使反应更充分,故填:增大反应物的接触面积,使反应更充分。
(3)碳和氧气反应生成二氧化碳,炼钢炉中,通入纯氧的目的是将生铁中过量的碳除去,故填:将生铁中过量的碳除去。
(4)将钢锭轧成钢板,体现了金属铁的延展性,故填:延展。
11.(2022·山西·交口县教师进修学校九年级期末)如图所示,甲是一氧化碳与氧化铁反应装置的示意图,乙是高炉炼铁示意图。回答下列问题。
(1)写出图甲中硬质玻璃管内反应的化学方程式:_______。
(2)实验中装有澄清石灰水的集气瓶中可观察到的现象是_______。写出该反应的化学方程式_______。
(3)图甲中尾气处理的目的是_______。
(4)实验开始时要先通入一氧化碳,把装置中的空气排尽后再加热,以防发生爆炸。检验装置中的空气已排尽的方法是_______。
(5)图乙中高炉炼铁时焦炭的作用是:①_______;②_______。
(6)图乙中炼铁的固体原料需经过粉碎,其目的是_______。
【答案】(1)Fe2O3+3CO 高温 2Fe+3CO2
(2) 澄清石灰水变浑浊;CO2+Ca(OH)2==CaCO3↓+H2O
(3)消除一氧化碳对空气的污染
(4)在右端导气管口用排水法收集一试管气体,移近火焰点燃,若发出轻微的爆鸣声,证明空气已经排尽(或点燃右端导气管中的气体,该气体能燃烧且产生蓝色火焰)
(5) 产生热量(或提高炉温);产生一氧化碳
(6)增大反应接触面积,加快反应速率(或增大接触面积,使其充分反应)
【解析】(1)一氧化碳能与氧化铁反应生成铁和二氧化碳,化学方程式为
Fe2O3+3CO 高温 2Fe+3CO2。
(2)硬质玻璃管中生成的二氧化碳能使澄清石灰水变浑浊,发生的反应是二氧化碳与澄清石灰水中的氢氧化钙反应生成碳酸钙和水,化学方程式为CO2+Ca(OH)2==CaCO3↓+H2O。
(3)尾气中含有一氧化碳,而一氧化碳有毒,会污染空气,则需要尾气处理。
(4)由于一氧化碳较纯时点燃会发出轻微的爆鸣声,则若想检验装置中的空气已排尽的方法是:在右端导气管口用排水法收集一试管气体,移近火焰点燃,若发出轻微的爆鸣声,证明空气已经排尽;或一氧化碳具有可燃性,则检验装置中的空气已排尽的方法是:点燃右端导气管中的气体,该气体能燃烧且产生蓝色火焰。
(5)高炉炼铁时需要高温,且需要还原剂一氧化碳,而碳燃烧生成二氧化碳,该反应放热,且碳与生成的二氧化碳反应生成一氧化碳,则高炉炼铁时焦炭的作用是:①产生热量(或提高炉温)、②产生一氧化碳。
(6)将固体原料粉碎,可增大接触面积,从而加快反应速率。
12.(2022·湖南娄底·中考真题)娄底市是湖南省最大的钢铁生产基地,某钢铁厂采用赤铁矿冶炼钢铁,其主要工艺流程如下,请完成下列问题。
【查阅资料】
Ⅰ.赤铁矿的主要成分是Fe2O3和SiO2
Ⅱ.石灰石的主要作用是将矿石中的SiO2转变为炉渣(主要成分是CaSiO3)和一种氧化物
(1)在步骤①中将固体反应物粉碎的目的是_____。
(2)高炉气体中除SO2、CO外,主要成分还有_____。
(3)在步骤②生成炉渣的反应中没有化合价的改变,请写出生成炉渣的化学反应方程式_____。
(4)在步骤④中吹入氩气,使钢水循环流动,使各部分均匀混合,相当于化学实验中_____的作用(填一种仪器名称)。
【答案】(1)增大反应物之间的接触面积,使反应更充分
(2)二氧化碳、氮气等
(3)
(4)玻璃棒
【解析】(1)在步骤①中将固体反应物粉碎,可以增大反应物之间的接触面积,使反应更充分;
(2)焦炭在空气中燃烧生成二氧化碳,二氧化碳和碳在高温下反应生成一氧化碳,空气中的主要成分是氮气,且没有参与反应,故高炉气体中除二氧化硫、一氧化碳外,还含有二氧化碳、氮气等;
(3)碳酸钙和二氧化硅在高温下反应生成硅酸钙和一种氧化物,且在步骤②生成炉渣的反应中没有化合价的改变,根据质量守恒定律,化学反应前后,元素的种类不变,反应物中含Ca、C、O、Si,生成物中含Ca、Si、O,故生成物中还应含碳元素,碳酸钙中碳元素显+4价,故生成的氧化物为二氧化碳,该反应的化学方程式为:;
(4)在步骤④中吹入氩气,使钢水循环流动,使各部分均匀混合,相当于化学实验中玻璃棒的作用,起到搅拌的作用。
13.(2022·江苏·徐州市铜山区新星学校九年级期末)某钢铁厂用高炉炼得生铁,再利用生铁炼钢,其主要反应过程如下图所示:
(1)高炉炼铁的原料主要是铁矿石、焦炭、_______和空气等。在高炉里,反应①的作用是获得二氧化碳,并_______。
(2)反应②的化学方程式是_______,反应③的化学方程式是_______。
(3)生铁炼钢的原理主要是用氧气等物质将生铁里过多的_______(填符号)和其他杂质除去。
【答案】(1) 石灰石;提供热量
(2) C+CO2 高温 2CO;Fe2O3+3CO 高温 2Fe+3CO2
(3)C
【解析】(1)高炉炼铁的原料主要是铁矿石、焦炭、石灰石和空气等,在高炉里,反应①的作用是获得二氧化碳,该反应放出热量,同时提供热量,故填:石灰石,提供热量;
(2)反应②是二氧化碳与焦炭在高温下反应生成一氧化碳,反应化学方程式为:
C+CO2 高温 2CO;反应③是一氧化碳在高温下与赤铁矿的主要成分氧化铁反应,生成铁和二氧化碳,反应方程式为:Fe2O3+3CO 高温 2Fe+3CO2;
(3)生铁的含碳量为2%~4.3%,生铁炼钢的原理主要是用氧气等物质将生铁里过多的碳和其他杂质除去,故填:C。
14.(2022·江苏苏州·九年级专题练习)兴趣小组同学模仿工业高炉炼铁原理,用图 1 实验装置(加热装置已省略)探究治炼铁的化学原理。
实验操作过程如下:
①将Fe2O3加水制成糊状,用毛笔刷在试管内壁,烘干;然后在试管底部加入一定量的焦炭,再向试管里通入干燥的CO2,此时用仪器测得CO2含量为a g/L,用气球密封试管口。
②高温加热试管中的氧化铁部位一段时间,无明显现象,随后熄灭酒精灯。
③高温加热焦炭部位一段时间,停止加热,用热成像仪拍摄图 1 中虚线框部位,数据输出得到图 2。恢复至与①相同的条件测得CO2含量为0.2a g/L。
④再次高温加热氧化铁部位,1分钟左右红棕色固体变成黑色。
请回答问题:
(1)高温加热试管中的固体,需要的加热仪器为_________。
(2)操作②中实验现象说明 CO2______ (选填“能”或“不能”)与 Fe2O3反应。
(3)操作③中 CO2含量减小的原因是_________。
(4)操作④中反应的化学方程式为_________。
(5)实验结束后,一般将装置内的气体灼烧处理,目的是_________。
(6)由图 2 可知,刚停止加热后焦炭区温度降低更快,可能原因是_________。
【答案】(1)酒精喷灯
(2)不能
(3)碳和二氧化碳高温反应生成一氧化碳,消耗二氧化碳
(4)Fe2O3+3CO 高温 2Fe+3CO2
(5)除去一氧化碳,防止污染空气
(6)碳和二氧化碳在高温下反应生成一氧化碳是吸热反应
【解析】(1)高温加热试管中的固体,则需要使用酒精喷灯加热。
(2)无明显现象说明没有发生反应,则操作②中实验现象说明二氧化碳和氧化铁不反应。
(3)碳和二氧化碳高温反应生成一氧化碳,消耗二氧化碳,所以操作③中二氧化碳含量减小。
(4)操作④发生的反应是氧化铁和一氧化碳高温反应生成铁和二氧化碳,化学方程式为Fe2O3+3CO 高温 2Fe+3CO2。
(5)装置内可能含有一氧化碳,是空气污染物,一氧化碳具有可燃性可通过点燃的方法除去。所以目的是除去一氧化碳,防止污染空气。
(6)因为碳和二氧化碳在高温下反应生成一氧化碳是吸热反应,刚停止加热反应还没停止,还在吸收热量,所以刚停止加热后焦炭区温度降低更快。
15.(2022·内蒙古赤峰·九年级期末)磁铁矿石(含Fe3O4)是常用的炼铁原料,请回答下列问题。
(1)Fe3O4中铁元素和氧元素的质量比为_____________。
(2)假设冶炼过程中铁没有损耗,用含有696吨Fe3O4的磁铁矿石可提炼出含铁质量分数为96%的生铁__吨?(写出具体过程)
【答案】(1)21:8
(2)设可提炼出含铁质量分数为96%的生铁的质量为x。
答:可提炼出含铁质量分数为96%的生铁是525t。
【解析】(1)Fe3O4中铁元素和氧元素的质量比为: (56×3):(16×4)=21:8。
(2)见答案。
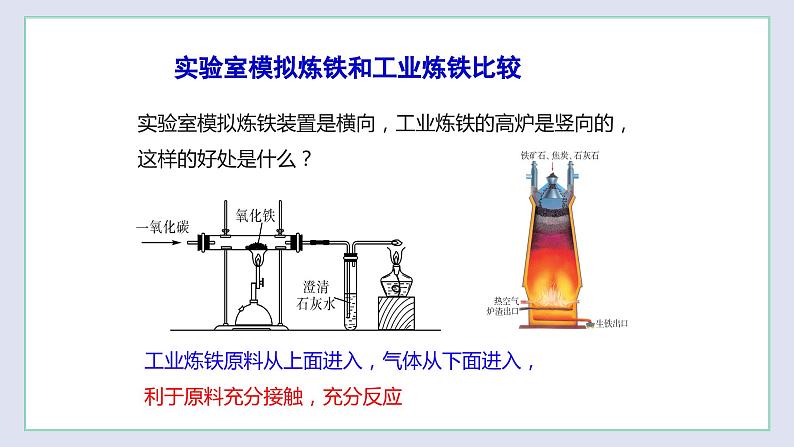
16.(2022·全国·九年级课时练习)如图甲是实验室模拟炼铁的装置图,图乙是炼铁高炉模型,下列说法不正确的是( )
A.图甲:实验开始时,应先通CO一段时间后,点燃酒精喷灯
B.图甲:实验过程中当看到红色固体变黑色,澄清石灰水变浑浊,说明有铁生成
C.图乙:高炉炼铁的原料有铁矿石、石灰石、焦炭、热空气
D.图乙:向高炉中投入含氧化铁160t的赤铁矿石,最多可得含杂质2%的生铁114.3t
【答案】B
【解析】A、实验开始时,应先通CO一段时间后,再点燃酒精喷灯,把装置中的空气排出,以免加热CO与空气的混合物时发生爆炸,说法正确,故A不符合题意;
B、一氧化碳还原氧化铁的过程中,可能生成四氧化三铁或氧化亚铁,也是黑色的,故实验过程中当看到红色固体变黑色,澄清石灰水变浑浊,不能说明有铁生成,故B不正确,符合题意;
C、高炉炼铁的原料有铁矿石、石灰石、焦炭、热空气,说法正确,故C正确,不符合题意;
D、设最多可得含杂质2%的生铁的质量为x,则
x≈114.3t
故D正确,不符合题意。
故选B。
17.(2022·广东广东·模拟预测)铁是人类历史上至今治炼得最多的金属。高炉炼铁的原料有铁矿石、焦炭、石灰石和空气等。其生产原理如图所示。
(1)反应I属于_______(填基本反应类型)反应:反应Ⅱ是______(填“放热”或“吸热”)反应。
(2)反应I和反应Ⅱ中焦炭的作用分别是提供热量和___________。
(3)主要成分为氧化铁的矿石名称为___________,氧化铁与气体Y的反应的化学方程式为___________;反应Ⅳ是铁矿石中的脉石(SiO2)跟固体R在高温下反应,生成了炉渣(CaSiO3),反应的化学方程式为___________。
(4)“铁水”的温度_____(填“高于”或“低于”)液态铁的温度,实际生产过程中,通常将铁水进一步处理可得到钢材,这样做的好处是什么?___________。
【答案】(1)化合;吸热
(2)生成还原剂一氧化碳
(3) 赤铁矿;;
(4)低于;炼钢过程中要将生铁再熔化,这样做可以避免消耗能源
【解析】(1)反应I是碳和氧气反应生成二氧化碳,是多变一的反应,是化合反应。反应Ⅱ是二氧化碳和碳高温下反应生成一氧化碳,该反应是常见的吸热反应。
(2)反应Ⅱ中,焦炭与二氧化碳反应生成一氧化碳,一氧化碳用于还原金属氧化物,所以焦炭的作用是生成还原剂一氧化碳。
(3)主要成分为氧化铁的矿石名称为赤铁矿。根据上述分析Y是生成的CO,氧化铁和一氧化碳在高温下反应生成铁和二氧化碳,化学方程式为Fe2O3+3CO 高温 2Fe+3CO2。
反应Ⅳ的反应物是SiO2与石灰石高温分解生成的氧化钙(R)反应,生成CaSiO3,则反应的化学方程式为。
(4)“铁水”冷却后是生铁,是铁合金,合金的熔点比组成它的纯金属的熔点低。所以“铁水”的温度低于液态铁的温度。生铁进一步处理得到钢需要先把生铁熔化,直接使用铁水可以减少熔化的过程,减少能源的消耗。所以这样做的好处是炼钢过程中要将生铁再熔化,这样做可以避免消耗能源。
18.(2022·青海西宁·中考真题)根据Fe3O4+4CO 高温 3Fe+4CO2反应原理,工业上可用来冶炼铁。现用100t含四氧化三铁为46.4%的某铁矿石冶炼金属铁。请完成下列问题,写出必要的计算过程。
(1)该铁矿石中含四氧化三铁质量是多少?
(2)理论上可炼出含铁96%的生铁的质量是多少?
【答案】(1)解:根据题意100t铁矿石中含四氧化三铁质量:
答:该铁矿石中含四氧化三铁质量是46.4t。
(2)解:设46.4t四氧化三铁完全反应生成纯铁的质量为 x。
理论上可炼出含铁96%的生铁的质量:33.6t÷96%=35t。
答:理论上可炼出含铁96%的生铁的质量:35t。
【解析】(1)见答案。
(2)见答案。
沪教版九年级上册第2节 金属矿物 铁的冶炼优秀ppt课件: 这是一份沪教版九年级上册第2节 金属矿物 铁的冶炼优秀ppt课件,共17页。PPT课件主要包含了COFe2O3,主要反应过程,工业炼铁的主要设备,造渣除杂,P1265,热还原法,电解法,热分解法等内容,欢迎下载使用。
初中化学第2节 金属矿物 铁的冶炼公开课教学课件ppt: 这是一份初中化学第2节 金属矿物 铁的冶炼公开课教学课件ppt,文件包含52金属矿物铁的冶炼第1课时课件pptx、52金属矿物铁的冶炼第1课时练习含答案解析docx、52金属矿物铁的冶炼第1课时练习docx、01无处不在的金属材料mp4、02一氧化碳还原氧化铁mp4等5份课件配套教学资源,其中PPT共23页, 欢迎下载使用。
初中化学沪教版九年级上册第2节 金属矿物 铁的冶炼完美版课件ppt: 这是一份初中化学沪教版九年级上册第2节 金属矿物 铁的冶炼完美版课件ppt,文件包含第5章第2节教学课件pptx、第5章第2节教案含练习docx等2份课件配套教学资源,其中PPT共34页, 欢迎下载使用。














