



沪教版 (上海)九年级第一学期第三单元 走进溶液世界3.2 溶液复习课件ppt
展开1.基础概念易错辨析:判断下列说法的正误。(1)无色、透明的液体不一定是溶液。( )(2)用汽油清洗油污和用洗洁精清洗餐具上的油污,其原理相同。( )(3)降温一定能使饱和溶液变为不饱和溶液。( )(4)溶质溶于水时,溶质的溶解度随溶剂量的增大而增大。( )
2.下列物质加入足量水中混合,能得到溶液的是( )A.植物油 B.碳酸钙固体 C.氢氧化钠固体 D.氯化银固体3.(2022云南)下列溶液中溶剂不是水的是( )A.碘酒溶液 B.生理盐水C.过氧化氢溶液D.葡萄糖注射液
4.(2022衡阳)下列关于溶液的说法正确的是( )A.溶液是具有均一性、稳定性的混合物B.饱和溶液一定是浓溶液,不饱和溶液一定是稀溶液C.打开汽水瓶盖后有气泡冒出,主要是因为温度升高,气体溶解度减小D.溶液都是无色透明的液体
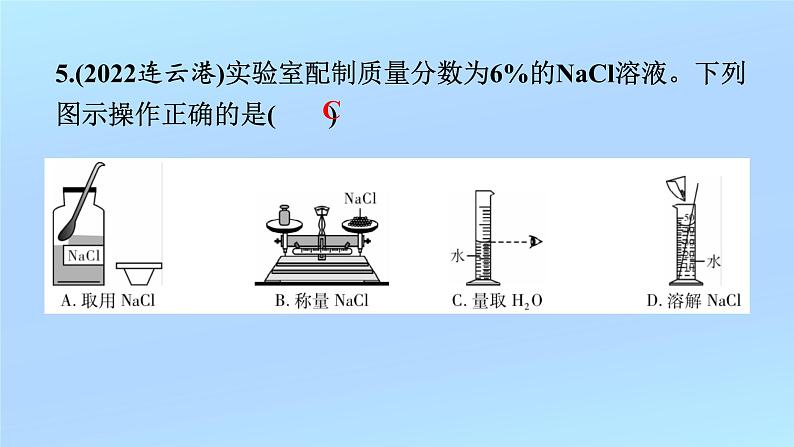
5.(2022连云港)实验室配制质量分数为6%的NaCl溶液。下列图示操作正确的是( )
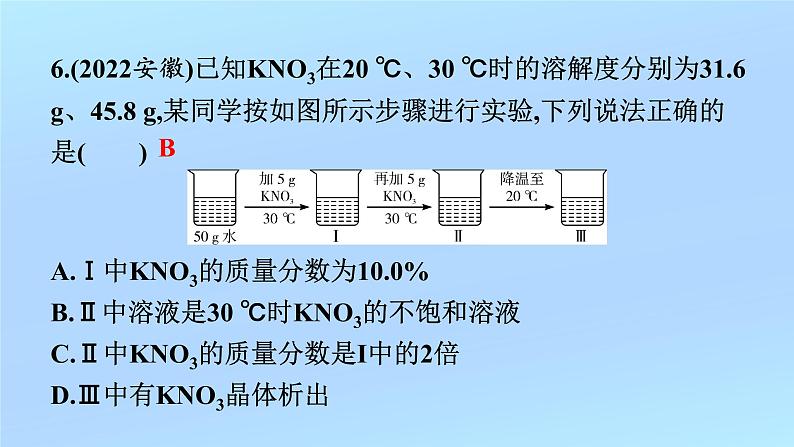
A.Ⅰ中KNO3的质量分数为10.0%B.Ⅱ中溶液是30 ℃时KNO3的不饱和溶液C.Ⅱ中KNO3的质量分数是I中的2倍D.Ⅲ中有KNO3晶体析出
6.(2022安徽)已知KNO3在20 ℃、30 ℃时的溶解度分别为31.6 g、45.8 g,某同学按如图所示步骤进行实验,下列说法正确的是( )
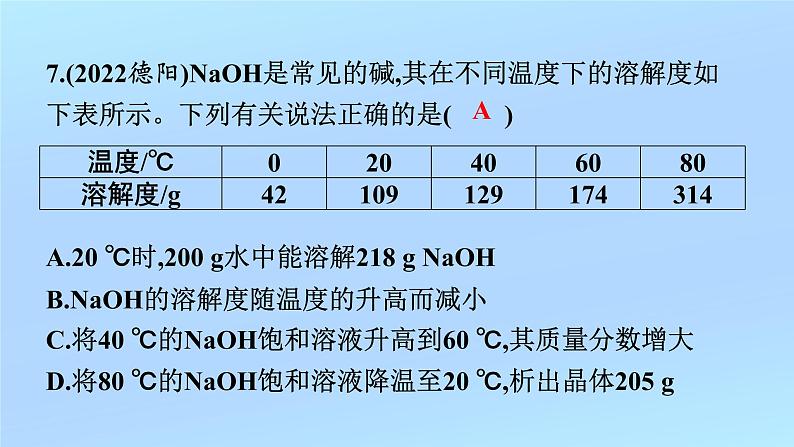
A.20 ℃时,200 g水中能溶解218 g NaOHB.NaOH的溶解度随温度的升高而减小C.将40 ℃的NaOH饱和溶液升高到60 ℃,其质量分数增大D.将80 ℃的NaOH饱和溶液降温至20 ℃,析出晶体205 g
7.(2022德阳)NaOH是常见的碱,其在不同温度下的溶解度如下表所示。下列有关说法正确的是( )
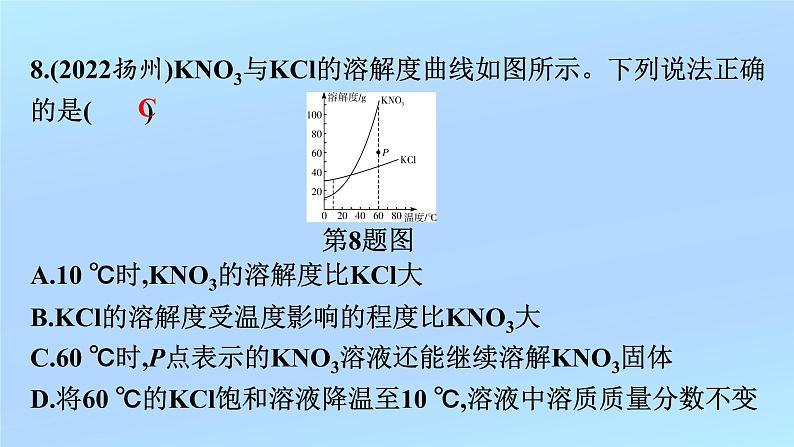
8.(2022扬州)KNO3与KCl的溶解度曲线如图所示。下列说法正确的是( )A.10 ℃时,KNO3的溶解度比KCl大B.KCl的溶解度受温度影响的程度比KNO3大C.60 ℃时,P点表示的KNO3溶液还能继续溶解KNO3固体D.将60 ℃的KCl饱和溶液降温至10 ℃,溶液中溶质质量分数不变
9.(2022香洲区模拟)硝酸钾的溶解度曲线如图所示。下列说法正确的是( )A.溶质的质量分数:a>b>cB.氢氧化钙的溶解度曲线与硝酸钾相似C.a、b、c三点对应的溶液均为饱和溶液D.从硝酸钾溶液中获得晶体的方法:冷却热的饱和溶液
10.(2022百校联考)如图为KNO3的溶解度曲线图,现有M状态下的KNO3溶液65 g,下列叙述不正确的是( )A.t2℃时,将M状态下65 g溶液倒掉32.5 g,能变成饱和溶液B.t2℃时,M状态下溶液的溶质质量分数小于30%C.t2℃时,向50 g水中加入15 g KNO3,充分搅拌后得到65 g溶液D.将M状态下65 g溶液的温度从t2℃降低到t1℃,刚好变成饱和溶液
(1)在 ℃时,A、B两种物质的溶解度相等。(2)t2℃时,A、B、C三种物质中溶解度最大的是 。 (3)若A中含有少量B时,可用 的方法提纯A。 (4)t2℃时,将35 g A固体加入100 g水中,充分溶解并恢复到原温度后,形成A物质的 (填“饱和”或“不饱和”)溶液,溶液的质量为 g,溶质的质量分数为 。
11.(2022怀化)如图是A、B、C三种固体物质的溶解度曲线,请回答下列问题。
(1)40 ℃时,KNO3、NaCl两种物质的溶解度大小关系:KNO3 (填“>”“<”或“=”)NaCl。
12.(2022遂宁)根据图中KNO3、NaCl的溶解度曲线,回答下列问题:
(2)下列说法不正确的是 (填字母)。 A.t ℃时,将45 g KNO3固体加入50 g水中充分溶解,所得溶液的质量为95 gB.NaCl溶液中含有少量KNO3,可以采用蒸发结晶的方法提纯NaClC.40 ℃时,将KNO3的饱和溶液降温至20 ℃,溶液的溶质质量分数减小(不考虑水分损失)
(3)同学们查阅NaCl的溶解度曲线后,欲配制20 ℃时100 g溶质质量分数为10%的NaCl溶液。已知配制溶液的步骤有:①溶解 ②计算 ③装瓶存放 ④称量Ⅰ.上述步骤的正确顺序为 (填序号)。 Ⅱ.溶解时,玻璃棒的作用为 。
搅拌,加快物质溶解速率
13.(2022东莞模拟)硫酸钠可用于导泻药物等,其溶解度曲线如图,下列分析正确的是( )A.随温度升高,硫酸钠的溶解度一直增大B.t1℃时,50 g水中能溶解40 g硫酸钠固体C.将c点饱和溶液降温到t1℃,有晶体析出D.d点为t1℃时的饱和溶液
14.(2022禅城区一模)如图是碳酸钠的溶解度曲线,下列说法正确的是( )A.T2℃时,将100 g Na2CO3加入200 g水中,可得到300 g溶液B.将a点的碳酸钠溶液升温至 T4℃的过程中有晶体析出C.b点碳酸钠溶液的溶质质量分数大于a点的溶质质量分数D.将b点的碳酸钠溶液降温至T1℃,溶液变成不饱和
(1)A中混有少量B应采用 的方法提纯A。 (2)t1℃时,将30 g B投入50 g水中,充分溶解,温度不变,所得溶液的质量为 g。 (3)若将t2℃时A、B、C的饱和溶液分别降温至t1℃,则所得溶液中溶质质量分数的大小关系是 。
15.(2022揭东区一模)如图1所示,A、B、C为三种物质的溶解度曲线,请根据图示信息回答下列问题。
(4)如图2所示,向放有镁片的试管中滴加稀盐酸后,锥形瓶中C的饱和溶液变浑浊。请解释原因: . 。 (5)将t2℃时溶质质量分数为25%的A的不饱和溶液降温到t1℃,所得溶液的溶质质量分数为 。
镁和稀盐酸反应放热,温度升高,导致C的溶解度减小,析
(6)实验需要用到溶质质量分数为10%的C溶液50 g,若实验室只有质量分数为20%的C溶液,要配制溶质质量分数为10%的C溶液需要用到的玻璃仪器有烧杯、量筒、 、 配制该溶液需量取水的体积为 mL。若量取C溶液时俯视读数(其他操作都正确),则最后得到的溶液浓度 (填“偏大”或“偏小”)。
中考化学 专题09 溶液【复习课件】: 这是一份中考化学 专题09 溶液【复习课件】,共24页。PPT课件主要包含了溶液的组成及特征,除污方法及原理,饱和溶液与不饱和溶液,溶解度和溶解度曲线,溶液的配制及稀释问题,第九单元溶液,混合物,均一性,稳定性,例如水等内容,欢迎下载使用。
溶液-中考化学一轮复习课件PPT: 这是一份溶液-中考化学一轮复习课件PPT,共24页。PPT课件主要包含了思维导图,溶液的形成,被溶解,能溶解,溶解时吸放热,NH4NO3,NaCl,NaOH或浓硫酸,除污方法,乳化作用等内容,欢迎下载使用。
溶液-中考化学一轮复习课件PPT: 这是一份溶液-中考化学一轮复习课件PPT,共30页。PPT课件主要包含了知识网络·思维导图,溶液的形成,知识清单·主干回顾,溶液的组成及特征,乳化现象,生活中常见的去污原理,NH4NO3,浓硫酸,蔗糖等,溶解时的能量变化等内容,欢迎下载使用。













