




化学必修 第一册第三节 物质的量获奖课件ppt
展开你能计算出这间教室中空气的质量吗?
Gas mlar vlume
决定物体体积大小的三要素
1 ml不同物质的质量是否相同?
1 ml不同物质在一定条件下的体积是否相同?
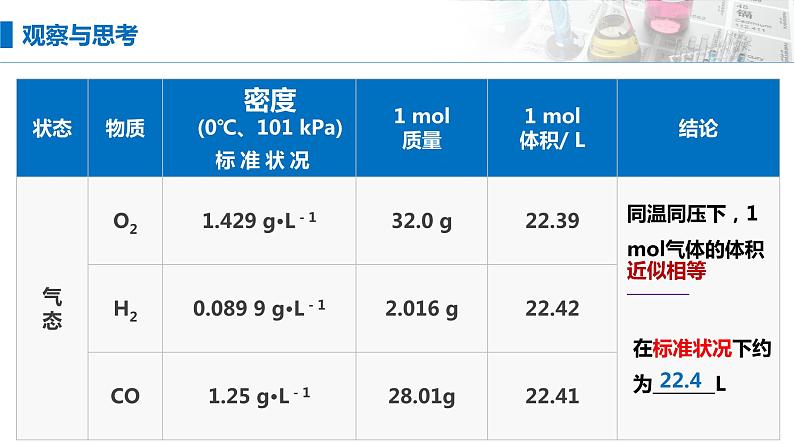
密度(0℃、101 kPa)
同温同压下,1 ml气体的体积_______
在标准状况下约为_______L
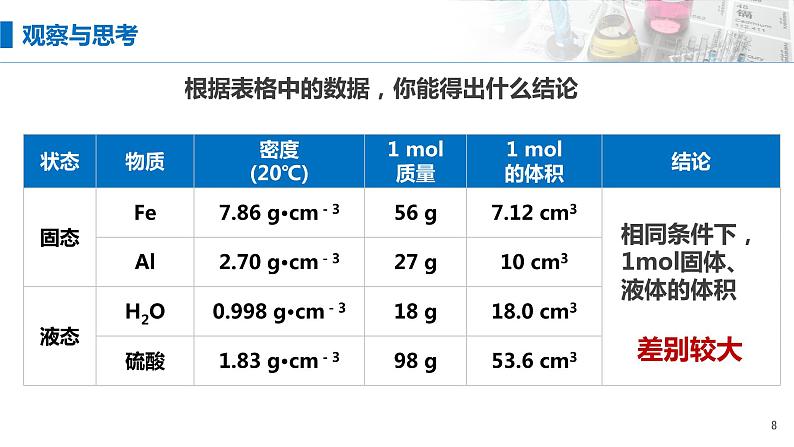
相同条件下,1ml固体、液体的体积
根据表格中的数据,你能得出什么结论
在相同状况下,1 ml不同的固体和液态物质的体积不相同!
而气体物质的体积却几乎相同!
决定物体体积大小的因素有哪些?
物质体积大小与何因素有关
1.1.1 粒子数目
微粒数(N)越多,体积越大
1. 决定物质体积的因素
1.1 物质体积与其构成微粒的关系
1.物质体积大小与何因素有关
微粒直径(d)越大,体积越大
1.1.2 粒子大小
微粒间距(l)越大,体积越大
1.1.3 粒子间距
同种物质在三种不同状态下的形态
以下状态微粒间距离有何特点?
1.2.1 固体与液体体积
1.2 决定不同状态物质体积的因素
100℃1 g H2O (气态)
(体积扩大1 700倍)
气体分子间的平均距离要比固体和液体中粒子之间的平均距离_______
通常状况时18 g H2O
气体体积与分子间距关系
气体的体积与________________有关!
气体的体积与__________无关!
气体体积与分子大小关系
1.2.2 气体体积
分子间的平均距离受哪些条件影响?
A.气体的种类B.气体的分子数C.分子本身的大小D.分子间的平均距离
同温同压下,下列与气体体积大小有关的因素是
在相同的温度和压强下,1 ml不同气体的体积在数值上有什么特点?
气体均为1 ml时的体积
在同温同压下,若两气体的体积相同
则他们的分子数有什么关系呢?
V(g)=f(N、p、T )
①1 L N2和1 L O2在同温同压下所含分子数相同
判断下列说法是否正确?为什么?
②1 g N2和1 g O2所含分子数相同
③1 ml N2和1 ml O2所占体积相同
④1 ml CO2气体在3.03×105 Pa时体积小于22.4 L
你计算出一间教室中的空气的质量?(已知空气的摩尔质量为29 g·ml-1)
单位物质的量的气体所占的体积
22.4 L·ml-1
3.3 标准状况气体摩尔体积
设教室长12 m,宽6 m高,3 m
12 m×5 m×3 m ×103 L/m3
1. 20℃、101kPa时,气体摩尔体积与标准状态时相比是大还是小?
2. 只有在标准状态下,Vm=22.4 L·ml-1 ?
非标准状况下,气体摩尔体积也可以是
气体均为1 ml时的体积/L
判断以下说法是否正确?
①标准状况下,1 ml任何物质的体积都约是22.4 L。②1 ml CO2的体积约为22.4 L。③标准状况下,1 ml O2和N2混合气体的体积约为22.4 L。④22.4 L气体所含分子数一定大于11.2 L气体所含的分子数。
⑤只有在标准状况下,气体的摩尔体积才可能约为22.4 L·ml-1。⑥在标准状况下,1 g H2和11.2 LO2的物质的量相等。⑦1 ml H2O在标准状况下的体积约为22.4 L。⑧在通常状况下,1 ml CO2占有的体积大于22.4 L。
①标准状况下,0.5 ml H2占有的体积是_______L。②标准状况下,2 ml O2占有的体积是_______L。③标准状况下,4.48 L CO2的物质的量是_______ml。④标准状况下,16 g O2的体积是_______L。⑤标准状况下,11.2 L N2分子数是_____________。
A.在标准状况下,1 ml N2的体积约为22.4 L·ml-1B.在标准状况下,H2O的摩尔体积约是22.4 L·ml-1C.1 ml N2的体积约为22.4 L,则N2的温度和压强一定是标准状况D.N2的摩尔体积可能恰好为11.2 L·ml-1
这节课我学到了什么?(用一句话表示)
决定物质体积大小的因素
0 ℃、1.01×105
气体体积由气体分子数目来决定
任何状况下任何气体均存在一个Vm
气体摩尔体积的四要素
A.Cl2 B.CO2 C.CH4 D.O2
1.在同温同压下,相同质量的下列气体中,体积最大的是
2.设阿伏加德罗常数为6.02×1023 ml-1 。关于1 ml H2O的叙述正确的是
A.含有1 ml H2B.含有6.02×1023个水分子C.质量为18 g·ml-1D.在标准状况下的体积为22.4 L
3.用NA表示阿伏加德罗常数的值。下列判断正确的是
A.标准状况下,22.4 L H2O中含有的分子数为NAB.标准状况下,22.4 L CO2含有的分子数目为NAC.常温常压下,22.4 L Cl2中含有的分子数为NAD.常温常压下,8 g O2含有4NA个电子
A.含1 ml CH3CH2OH的乙醇溶液中所含分子总数一定大于NAB.常温常压下,22.4 L的NO2和CO2混合气体含有2NA个O原子C.常温下,2.7 g铝与足量的盐酸反应,失去电子数为0.3NAD.常温常压下,14 g由N2与CO组成的混合气体含有的原子数目为NA
4.用NA表示阿伏加德罗常数的值。下列叙述不正确的是
A.分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA B.常温常压下,22.4 L氧气与足量镁粉充分反应,转移的电子数为4NAC.18 g H2O中含有的质子数为10NAD.标准状况下,11.2 L 乙醇中含有分子的数目为0.5NA
5.设NA为阿伏伽德罗常数的值。下列说法正确的是
高中化学人教版 (2019)必修 第一册第三节 物质的量精品课件ppt: 这是一份高中化学人教版 (2019)必修 第一册第三节 物质的量精品课件ppt,共36页。PPT课件主要包含了看谁做得既准又快,你知道吗,化学趣史,H+Cl=,H05Cl05,提出阿伏加德罗假说,相同数目的分子,气体摩尔体积计算,学习目标,气体摩尔体积等内容,欢迎下载使用。
高中第三节 物质的量课前预习ppt课件: 这是一份高中第三节 物质的量课前预习ppt课件,共38页。PPT课件主要包含了012kg12C,g·mol-1,相对式量,题组训练,gmol,③②④①,结束放映,返回导航页,栏目导引等内容,欢迎下载使用。
第1讲 物质的量 气体摩尔体积: 这是一份第1讲 物质的量 气体摩尔体积,共60页。PPT课件主要包含了考点一,考点二,考点三,必备知识·梳理夯实,mol,012kg,02×1023,1mol,g·mol-1,特别提醒等内容,欢迎下载使用。













