





高中化学人教版 (2019)选择性必修2第一章 原子结构与性质第一节 原子结构教学课件ppt
展开人教版选择性必修二化学
《构造原理 核外电子排布式》教学设计
课题名 | 构造原理 核外电子排布式 | ||
教学目标 | 1.通过认识原子结构及核外电子排布,辨识微观粒子的运动状态不同于宏观物体的运动状态 2.结合原子核外电子排布规律及核外电子排布的原则建立观点、结论和证据之间的逻辑关系 | ||
教学重点 | 能应用构造原理写出原子的电子排布式 | ||
教学难点 | 能应用构造原理写出原子的电子排布式 | ||
教学准备 | 教师:课件、习题 学生:复习能层与能级的知识 | ||
教师活动 | 学生活动 | 设计意图 | |
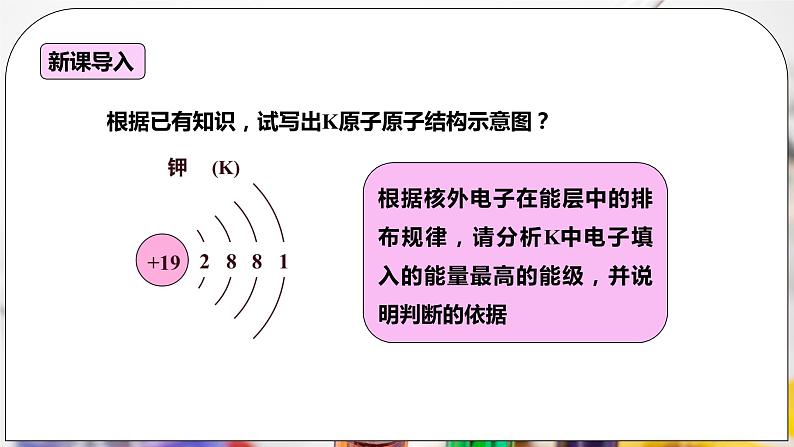
导入 根据已有知识,试写出K原子原子结构示意图? 根据核外电子在能层中的排布规律,请分析K中电子填入的能量最高的能级,并说明判断的依据
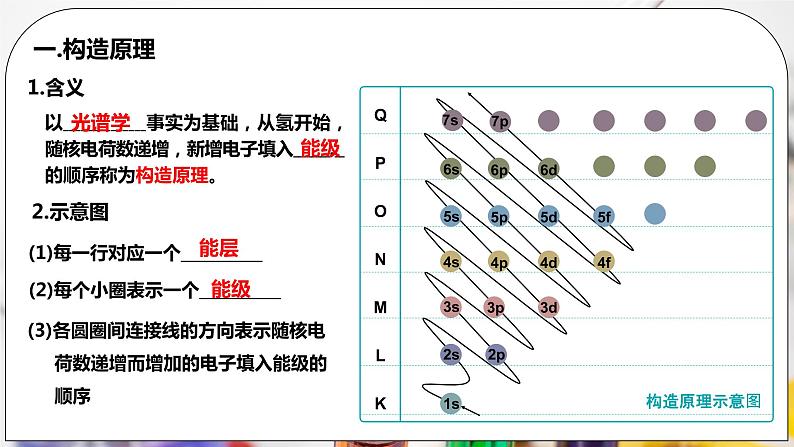
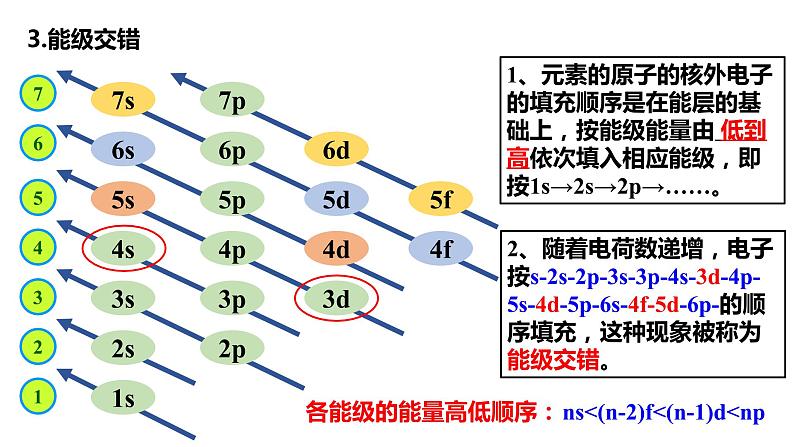
一.构造原理 1.含义 以光谱学事实为基础,从氢开始,随核电荷数递增,新增电子填入能级的顺序称为构造原理。 2.示意图 (1)每一行对应一个能层 (2)每个小圈表示一个能级 (3)各圆圈间连接线的方向表示随核电 荷数递增而增加的电子填入能级的顺序 3.能级交错 (1)元素的原子的核外电子的填充顺序是在能层的基础上,按能级能量由 低到高依次填入相应能级,即按1s→2s→2p→……。 (2)随着电荷数递增,电子按s-2s-2p-3s-3p-4s-3d-4p-5s-4d-5p-6s-4f-5d-6p-的顺序填充,这种现象被称为能级交错。 各能级的能量高低顺序:ns<(n-2)f<(n-1)d<np
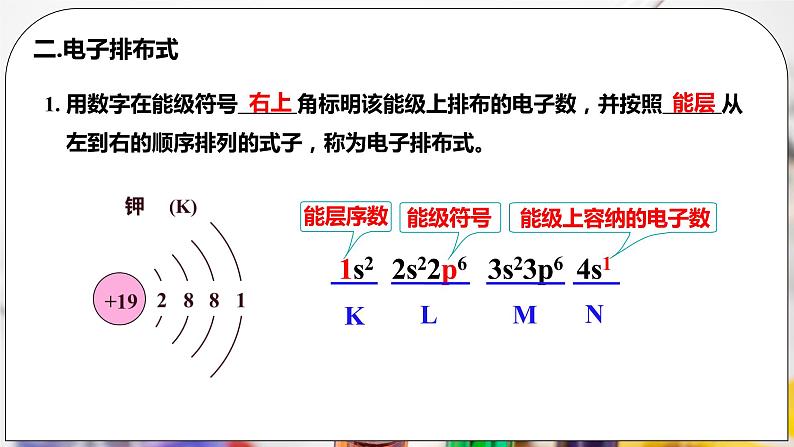
二.电子排布式 1. 用数字在能级符号右上角标明该能级上排布的电子数,并按照能层从左到右的顺序排列的式子,称为电子排布式。
练一练: 例1:根据构造原理,试比较下列能级的能量高低(填“>”或“<”)。 ①4s____3d;②6s____4f____5d。 例2:根据构造原理,写出下列基态原子的核外电子排布式 ① 8O: ; ②14Si: ; ③19K: ; ④21Sc: ; ⑤26Fe: 。 注意:并不是所有基态原子的核外电子都符合构造原理。 如:24Cr:1s22s22p63s23p63d54s1 29Cu:1s22s22p63s23p63d104s1 2.简化的电子排布式 [Ar]表示的是Ar的核外电子排布,也称为原子实;通常是该元素前一个周期的惰性气体电子排布结构 原子实表示的电子称为内层电子,通常不参与成键。 原子实外的电子称为价层电子,决定元素的化学性质。
练一练 例3:根据构造原理试写出下列基态原子的电子排布式和简化电子排布式 ①24Cr: , 。 ②29Cu: , 。 ③33As: , 。 ④35Br: , 。 3.价电子排布式 (1)“价电子层”定义: 为突出化合价与电子排布的关系,将在化学反应中可能发生电子变动的能级称为价电子层(简称价层) (2)价电子的位置: ①主族元素:最外层电子:nsx或nsxnpy ②过渡元素:最外层电子:(n-1)dxnsy
练一练 例4:写出下列元素基态原子的价层电子排布式: (1)16S: 。 (2)23V: 。 (3)30Zn: 。 (4)32Ge: 。 (5)34Se: 。
课堂小结
随堂练习: 1.下列基态原子与离子的电子排布式错误的是 ( ) A. K: 1s22s22p63s23p64s1 B. F-: 1s22s22p6 C. Fe: 1s22s22p63s23p63d54s2 D. Kr: 1s22s22p63s23p63d104s24p6 3.表示一个原子在M能层上有10个电子,可以写成( ) A.3p6 B.3d10 C.3s23p63d24s2 D.3s23p64s2 3.下列说法中正确的是( ) A.1s22s12p1表示的是激发态原子的核外电子排布 B.3p2表示3p能级有两个原子轨道 C.同一原子中,1s、2s、3s电子的能量逐渐减小 D.同一原子中,2p、3p、4p能级中的轨道数依次增
|
复习已有知识,思考钾核外电子排布为什么是2881,而不是289
结合图示学习构造原理
根据构造原理,自主探究能级交错现象
学习电子排布式的书写规则
完成练习
强调特殊原子的核外电子排布式
学习简化的核外电子排布式
完成练习
学习“价电子”的知识
自主归纳本节课内容
完成练习
|
设疑,利用已有知识的矛盾,激发学生的学习兴趣
利用图片展示,更直观的帮助学生理解知识
培养学生的探究意识
讲练结合,巩固所学知识
引导学生自主归纳
讲练结合,巩固所学知识
讲练结合,巩固所学知识
课堂小结,归纳知识点
随堂练习,及时反馈知识掌握情况 | |
布置作业 |
课时作业《构造原理 核外电子排布式》 | ||
板书设计
| 一.构造原理 1.含义 2.能级交错:ns<(n-2)f<(n-1)d<np 二.电子排布式 1.
2.简化的电子排布式: 3.价电子排布式 ①主族元素:最外层电子:nsx或nsxnpy ②过渡元素:最外层电子:(n-1)dxnsy | ||
教学反思 | 本节课的内容相对简单,引导学生理解能级交错的现象,教师应注重讲练结合,课堂上给予学生更多的练习时间。 | ||
高中化学人教版 (2019)选择性必修2第一节 原子结构教案配套ppt课件: 这是一份高中化学人教版 (2019)选择性必修2第一节 原子结构教案配套ppt课件,共25页。PPT课件主要包含了构造原理,电子排布式,能级交错现象,ns2np6,s22s22p1,s22p3,s23p63d10,s22s22p6等内容,欢迎下载使用。
人教版 (2019)选择性必修2第一节 原子结构公开课ppt课件: 这是一份人教版 (2019)选择性必修2第一节 原子结构公开课ppt课件,共24页。PPT课件主要包含了情境导入,目标一构造原理,构造原理,能级交错,电子排布式,电子数,能级符号,s22s22p3,s22s22p4,4s1等内容,欢迎下载使用。
化学人教版 (2019)第一节 原子结构教学ppt课件: 这是一份化学人教版 (2019)第一节 原子结构教学ppt课件,共60页。PPT课件主要包含了构造原理,能级交错,s4f5d6p,s2p,s3p,s3d4p,s4d5p,s5f6d7p,电子排布式,1电子排布式等内容,欢迎下载使用。














