




2022淄博高二下学期期中考试化学试题含解析
展开山东省淄博市2021-2022学年高二下学期期中考试
化学试题
本试卷分第I卷和第II卷两部分, 考试用时90分钟,满分100分。
可能用到的相对原子质量: H 1 C 12 N 14 O16
第I卷(选择题,共40分)
一、选择题(本题包括10小题,每题只有一个选项符合题意;每题2分,共20分)
1. 下列化学用语表示不正确的是
A. 甲烷的电子式: B. 氯乙烷的结构简式: CH3CH2Cl
C. 2−甲基−1−丁醇的键线式: D. 乙烯的空间填充模型:
2. 下列说法正确的是
A. 与含有相同的官能团,互为同系物
B. 属于醛类,官能团为−CHO
C. 的名称为: 2−乙基−1−丁烯
D. 乙醚与乙醇互为同分异构体
3. 下列各项中I、II两个反应不属于同一反应类型是
选项 | 反应I | 反应II |
A | CH3CH2OH→CH3COOCH2CH3 | → |
B | CH3CH2Cl→CH3CH2OH | CH3CH2OH→CH2=CH2 |
C | CH2=CH2→CH3CH2Cl | → |
D | CH3CH2OH→CH3CHO | CH3CHO→CH3COOH |
A. A B. B C. C D. D
4. 有机化合物分子中基团之间的相互影响会导致物质的化学性质不同。下列事实不可以用上述观点解释的是( )
A. 苯不能与溴水发生取代反应,而苯酚能与溴水发生取代反应
B. 乙醇不能与碱发生中和反应,而乙酸能与碱发生中和反应
C. 2-甲基-1-丙醇能发生消去反应,2,2-二甲基-1-丙醇不能发生消去反应
D 乙烷不能使高锰酸钾溶液褪色,而甲苯能使高锰酸钾溶液褪色
5. 有关晶体的结构如图所示,下 列说法中不正确的是
A. 在NaCl晶体中,每个晶胞平均占有4个Cl-
B. 在CsCl晶体中,距Cl-最近的Cs+有6个
C. 在金刚石晶体中,最小的环上有6个C原子
D. CO2 晶胞中一个分子周围有12个紧邻分子
6. 为提纯下列物质(括号内为少量杂质),所选用的除杂试剂与主要分离方法都正确的是
选项 | 混合物 | 除杂试剂 | 分离方法 |
A | 苯(苯酚) | 浓溴水 | 过滤 |
B | 溴苯(溴) | NaOH溶液 | 分液 |
C | 甲烷(乙烯) | 酸性KMnO4溶液 | 洗气 |
D | 乙酸乙酯(乙酸) | 氢氧化钠溶液 | 蒸馏 |
A. A B. B C. C D. D
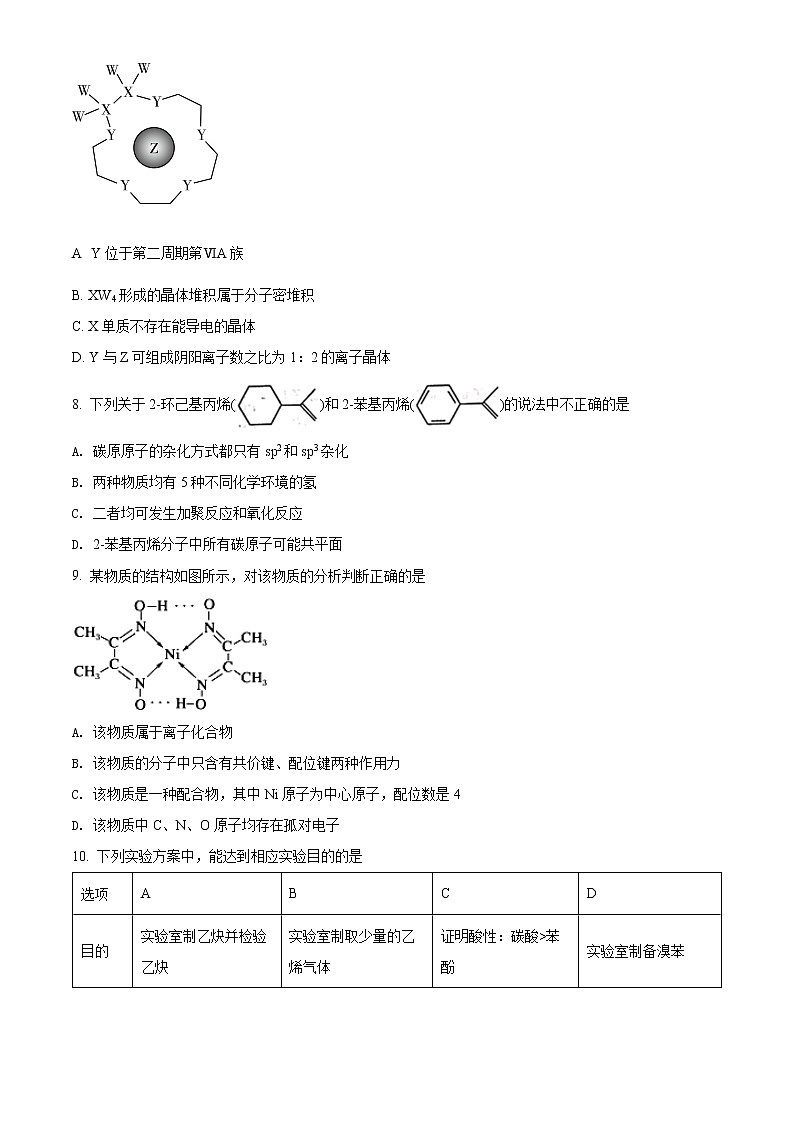
7. X、Y、Z是原子序数依次增大的短周期元素,可“组合”成一种具有高效催化性能的超分子,其结构如图(注:实线代表共价键,其他Y原子之间的重复单元中的W、X未展开标注),W、X、Z分别位于不同周期, Z是同周期中金属性最强的元素。下列说法不正确的是
A Y位于第二周期第ⅥA族
B. XW4形成的晶体堆积属于分子密堆积
C. X单质不存在能导电的晶体
D. Y与Z可组成阴阳离子数之比为1:2的离子晶体
8. 下列关于2-环己基丙烯()和2-苯基丙烯()的说法中不正确的是
A. 碳原原子的杂化方式都只有sp2和sp3杂化
B. 两种物质均有5种不同化学环境的氢
C. 二者均可发生加聚反应和氧化反应
D. 2-苯基丙烯分子中所有碳原子可能共平面
9. 某物质的结构如图所示,对该物质的分析判断正确的是
A. 该物质属于离子化合物
B. 该物质的分子中只含有共价键、配位键两种作用力
C. 该物质是一种配合物,其中Ni原子为中心原子,配位数是4
D. 该物质中C、N、O原子均存在孤对电子
10. 下列实验方案中,能达到相应实验目的的是
选项 | A | B | C | D |
目的 | 实验室制乙炔并检验乙炔 | 实验室制取少量的乙烯气体 | 证明酸性:碳酸>苯酚 | 实验室制备溴苯 |
实验方案 |
A. A B. B C. C D. D
二、选择题(本题包括5小题,每小题4分,共20分。每小题有一个或两个选项符合题意,全都选对得4分,选对但不全的得2分,有选错的得0分)
11. 下列对有关事实的解释正确的是
选项 | 事实 | 解释 |
A | SiO2的熔点比干冰高 | SiO2晶体是共价晶体,分子间作用力大 |
B | 在CS2中的溶解度:CCl4 >H2O | CS2、CCl4为非极性分子,而H2O为极性分子 |
C | 用质谱仪检测气态乙酸时,谱图中出现质荷比(相对分子质量)为120的峰 | 两个乙酸分子通过范德华力形成了二聚体 |
D | 离子液体有难挥发性 | 离子液体的粒子全都是带电荷的离子 |
A. A B. B C. C D. D
12. 某有机物分子式为C5H10O3,与饱和NaHCO3溶液反应放出气体体积与同等状况下与Na反应放出气体体积相等,该有机物有(不含立体异构)( )
A. 9种 B. 10种 C. 11种 D. 12种
13. 有机物Z是一种重要的医药中间体,可由如下反应制得。下列说法正确的是
A. 该反应另一种小分子产物是HCl
B. Z分子中的官能团有氯原子、酮基和羟基
C. Y分子中所有原子位于同一平面内,则Y中碳原子的杂化方式有2种
D. X的同分异构体中能发生银镜反应,且属于芳香族化合物的共有6种
14. 下列实验中,操作、现象及结论均正确的是
选项 | 操作 | 现象 | 结论 |
A | 将CH3CH2Br与NaOH溶液共热,冷却后,取出上层水溶液加入AgNO3溶液 | 产生淡黄色沉淀 | CH3CH2Br中含有溴原子 |
B | 向2 mL10%的NaOH溶液中滴入2%的CuSO4溶 液4至6滴,得到新制的Cu(OH)2悬浊液,然后加入乙醛溶液0.5 mL,振荡后加热 | 产生砖红色沉淀 | 醛基具有还原性 |
C | 将乙醇与浓硫酸共热至170℃所得气体直接通入酸性KMnO4溶液中 | KMnO4溶液褪色 | 乙醇发生消去反应的产物为乙烯 |
D | 向苯酚钠溶液中通入一定量CO2 | 溶液变浑浊 | 碳酸的酸性比苯酚的酸性强 |
A. A B. B C. C D. D
15. 异黄酮类化合物是药用植物的有效成分之一。一种异黄酮类化合物Z的部分合成路线如图:
下列有关化合物X、Y和Z的说法不正确的是
A. 1molZ 与过量碳酸钠溶液反应消耗2mol碳酸钠
B. 1molY 最多能与3molNaOH反应
C. X与足量H2反应后,产物分子中有4个手性碳原子
D. 等物质的量的X、Y分别与足量溴水反应,消耗单质溴的物质的量: Y=X
第Ⅱ卷(非选择题,共60分)
三、本题包括5小题,共60分。答案必须写在答题卡内相应的位置,不能写在试卷上。
16. 完成下列问题
(1)参考表中物质的熔点,问答有关问题。
物质 | NaF | NaCl | NaBr | NaI |
熔点/℃ | 995 | 801 | 755 | 651 |
物质 | SiF4 | SiCl4 | SiBr4 | SiI4 |
熔点/℃ | −90.2 | −70.4 | 5.2 | 120.0 |
钠的卤化物熔点变化的原因是 _______, 影响硅的卤化物熔点的因素是_______,钠的卤化物的熔点比相应的硅的卤化物的熔点高得多的原因是_______。
(2)向胆矾溶液中滴加氨水至过量,最终得到深蓝色的透明溶液,再加入乙醇后析出深蓝色晶体,写出生成深蓝色透明溶液的离子方程式:_______。该实验可知,与Cu2+结合生成配离子的稳定性: NH3_______ H2O(填 “>”或“<” )。
(3)含有多个配位原子的配体与同一中心离子(或原子)通过螯合配位成环而形成的配合物为螯合物。卟啉配合物叶绿素是一种,其结构如图所示。叶绿素的中心离子无论是Mg2+还是Zn2+,都能形成稳定结构,原因是_______, 其中稳定性相对较高的是_______ (填“Mg2+”或“Zn2+”) , 1mol该配合物中通过螯合作用形成的配位键的数目为_______。
17. 完成下列问题
(1)As2Se3是一种非晶态半导体,也称玻璃半导体。区分晶体与非晶体的最可靠的科学方法是_______。
(2)钴的一种化合物的立方晶胞结构如图所示,已知A点的原子坐标参数为(0,0,0),B点为(,0,),则C点的原子坐标参数为_______,钴周围等距离且最近的O2-数目为 _______,该物质的化学式为_______。
(3)以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称作原子分数坐标。CsSiB3O7属正交晶系(长方体形)。晶胞参数为a pm、b pm、c pm。如图为沿y轴投影的晶胞中所有Cs原子的分布图和原子分数坐标。据此推断该晶胞中Cs原子的数目为_______。CsSiB3O7的摩尔质量为M g∙mol−1,设NA为阿伏加德罗常数的值,则CsSiB3O7晶体的密度为_______g·cm−3(用代数式表示)。为点(0.5,0.8,0)与点(1.0,0.7,1.0)之间的距离为_______pm。
18. 苯甲酸乙酯(密度1.05g/cm3),稍有水果气味,用于配制香水香精和人造精油,也大量用于食品以及用作有机合成中间体等。制备苯甲酸乙酯的过程如下:
制备粗产品:如图所示装置中,在装置A中加入8.0g苯甲酸、20mL 乙醇(密度0. 79g/cm3)、15mL 环己烷、3mL 浓硫酸,摇匀,加沸石。在分水器中加水,接通冷凝水,水浴回流约2h,反应基本完成。记录体积,继续蒸出多余环己烷和醇(从分水器中放出)。
粗产品纯化:加水30mL,分批加入饱和NaHCO3溶液。分液,然后水层用20mL石油醚分两次萃取。合并有机层,用无水硫酸镁干燥。回收石油醚,加热精馏,收集210~213℃馏分。相关数据如下:
物质 | 苯甲酸 | 苯甲酸乙酯 | 石油醚 | 水 | 乙醇 | 环己烷 | 共沸物(环己烷-水-乙醇) |
沸点(℃) | 249 | 212.6 | 40~80 | 100 | 783 | 80.75 | 62.6 |
根据以上信息和装置图回答下述实验室制备有关问题:
(1)仪器B的名称是_______。
(2)写出制备苯甲酸乙酯反应的化学方程式_______。
(3)采用水浴加热的优点是_______。 通过分水器不断分离除去反应生成的水,目的是_______。
(4)如何利用实验现象判断反应已基本完成 _______。
(5)加入饱和NaHCO3溶液的作用除降低苯甲酸乙酯溶解度外,还有_______。
(6)经精馏得210~213℃馏分6.0 mL,则实验中苯甲酸乙酯的产率为_______。 (保留两位有效数字)
19. Ⅰ.扑热息痛是最常用的非抗炎解热镇痛药,对胃无刺激,副作用小。对扑热息痛进行结构表征,测得的相关数据和谱图如下。回答下列问题:
(1)测定实验式。
将15.1 g样品在足量纯氧中充分燃烧,并使其产物依次缓缓通过浓硫酸、碱石灰,发现两者分别增重8.1g和35.2 g,再将等量样品通入二氧化碳气流中,在氧化铜/铜的作用下氧化有机物中氮元素,测定生成气体的体积为1.12 L(已换算成标准状况)。其实验式为_______。
(2)确定分子式。测得目标化合物的质谱图如下:其分子式为_______。
(3)推导结构式。
用化学方法推断样品分子中的官能团。
①加入NaHCO3溶液,无明显变化;
②加入FeCl3溶液,显紫色;
③水解可以得到一种两性化合物。
波谱分析:通过目标化合物的红外光谱图分析可知该有机化合物分子中存在:、-OH、、
②测得目标化合物的核磁共振氢谱图如下:
该有机化合物分子含有五种不同化学环境的H原子,其峰面积之比为1:1:2:2:3,综上所述,扑热息痛的结构简式为_______。
Ⅱ.有机物M是药物合成的中间体,可用C和F在一定条件下合成。合成路线如图:
已知以下信息: i.
ii.RCOCH3+R' CHO RCOCH=CHR'
iii.F能发生银镜反应
回答下列问题:
(4)A的化学名称为_______。M中含氧官能团的名称_______。
(5)A生成B的化学方程式为_______。
(6)B生成C的反应类型为_______。E生成F的反应类型为_______。
(7)D的结构简式为_______。
(8)B的同分异构体中能与FeCl3溶液反应显紫色的共有_______种
20. 某抗癌药物G的一种合成路线如下:
回答下列问题:
(1)R名称是_______; G含官能团有碳氟键、硝基和_______。
(2)F→G的反应类型是_______。
(3)写出E→F的化学方程式:_______;吡啶的结构简式为 ,有弱碱性,吡啶在该反应中作用是_______。
(4)Y→Z、F→G都是在苯环上引入硝基,−CF3是苯环的间位控制基(即使苯环间位氢变活泼,发生取代反应时主要取代间位),−NHCOCH(CH3)2是苯环的_______位控制基。
(5)R的二氯代物有_______ (填字母)。
a.4种 b.6种 c.9种 d.10种
(6)参照上述合成路线,设计一条以苯甲醚( )和CH3COC1为原料合成甲氧基乙酰苯胺( )的路线,其他试剂自选,合成路线示例见题目。_______
2022青岛地区高二下学期期中考试化学试题含解析: 这是一份2022青岛地区高二下学期期中考试化学试题含解析,文件包含山东省青岛地区2021-2022学年高二下学期期中考试化学试题含解析docx、山东省青岛地区2021-2022学年高二下学期期中考试化学试题docx等2份试卷配套教学资源,其中试卷共31页, 欢迎下载使用。
2020淄博淄川中学高二下学期期中考试化学试题含答案: 这是一份2020淄博淄川中学高二下学期期中考试化学试题含答案,共9页。
山东省淄博市2021-2022学年高二下学期期中考试化学试题 附解析: 这是一份山东省淄博市2021-2022学年高二下学期期中考试化学试题 附解析,共23页。试卷主要包含了选择题,本题包括5小题,共60分等内容,欢迎下载使用。












